

分析 (1)根據反應前后的質量差可以計算生成二氧化碳的質量;
(2)根據二氧化碳的質量可以計算反應生成氯化鈉的質量,進一步可以計算反應后所得溶液中溶質的質量分數.
解答 解:(1)反應生成CO2氣體的質量為:100g+19.2g-117g=2.2g;
故答案為:2.2;
(2)設生成氯化鈉的質量為x,
Na2CO3+2HC1═2NaC1+H2O+CO2↑
117 44
x 2.2g
x=5.85g
反應后所得溶液中溶質的質量分數為:$\frac{5.85g}{117g}$×100%=5%
答:反應后所得溶液中溶質的質量分數為5%.答:反應后所得溶液中溶質的質量分數為5%.
點評 本題考查了溶液質量分數的求算、有關方程式的計算,題目難度不大,側重于考查學生的分析能力和計算能力.


科目:高中化學 來源: 題型:選擇題

| A. | 25℃時,NaHCO3在水中的溶解度比Na2CO3的大 | |
| B. | 石灰乳與Cl2的反應中,Cl2既是氧化劑,又是還原劑 | |
| C. | 常溫下干燥的Cl2能用鋼瓶貯運,所以Cl2在任何條件下都不與鐵反應 | |
| D. | 圖示轉化反應都是氧化還原反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 有A、B、C、D、E、F六種物質,它們的相互轉化關系如圖(反應條件及部分產物乙略).已知A、B、E均為單質,B、E在常溫下為氣體,C為淡黃色固體.回答下列問題:
有A、B、C、D、E、F六種物質,它們的相互轉化關系如圖(反應條件及部分產物乙略).已知A、B、E均為單質,B、E在常溫下為氣體,C為淡黃色固體.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 50mL 3 mol•L-1的KCl溶液 | B. | 150mL 1 mol•L-1的FeCl2溶液 | ||
| C. | 150mL 1 mol•L-1的MgCl2溶液 | D. | 300mL 1 mol•L-1的NaCl溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
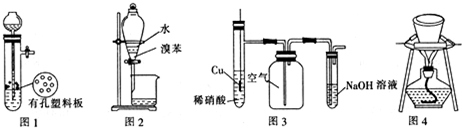
| A. | 圖1裝置用于Cu和濃H2SO4反應制取少量的SO2氣體 | |
| B. | 圖2裝置用于分離水和溴苯的混合物 | |
| C. | 圖3裝置用于制備并收集NO氣體 | |
| D. | 圖4裝置用于除去碳酸氫鈉固體中的少量碳酸鈉 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯氣通入氯化亞鐵溶液中:Cl2+Fe2+=2Cl-+Fe3+ | |
| B. | 碳酸鈉溶于醋酸溶液中:CO32-+2 H+=H2O+CO2↑ | |
| C. | 次氯酸鈣溶液中通入過量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO | |
| D. | 硫酸與氫氧化鋇溶液反應:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 實驗室常用鋁鹽溶液與氫氧化鈉溶液制備Al(OH)3沉淀 | |
| B. | 濃硫酸能干燥SO2、NO2等氣體,說明濃硫酸具有吸水性 | |
| C. | SO2 具有漂白性,通入紫色石蕊溶液中能使溶液先變紅后褪色 | |
| D. | 30%的H2O2溶液中加入MnO2可制得O2,MnO2做氧化劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
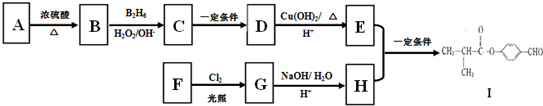
 .
.
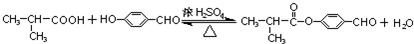
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com