
【題目】【化學——選修2:化學與技術】
某工廠用軟錳礦(含MnO2約70% 及A12O3)和閃鋅礦(含ZnS約80%及FeS)共同生產MnO2和Zn(干電池原料)。

已知:①A是![]() 的混合液。
的混合液。
②IV中的電解方程式為:![]()
(l)A中屬于還原產物的是________________________。
(2)加人MnCO3、Zn2(OH)2CO3的作用 ________________________。
II需要加熱的原因是:____________________。C的化學式是 _______________。
(3)該生產中除得到MnO2和Zn以外,還可得到的副產品是_________________。
(4)如果不考慮生產中的損耗,除礦石外,需購買的化工原料是_____________。
(5)要從Na2SO4溶液中得到芒硝(Na2SO4·10H2O),需進行的操作有蒸發濃縮、___________、過濾、洗滌、干燥等。
(6)從生產MnO2和Zn的角度計算,軟錳礦和閃鋅礦的質量比大約是__________。
【答案】(1)MnSO4 (2分)
(2)增大溶液的PH,使Fe3+和Al3+均生成沉淀(2分);促進Fe3+和Al3+的水解(2分);H2SO4(1分)
(3)Fe2O3、Al2O3、S、Na2SO4(2分)
(4)純堿和硫酸(2分)(5)冷卻結晶.(2分) (6) 1.03(2分)
【解析】
試題分析:(1)在氧化還原反應中,化合價降低元素所在的產物是還原產物;比較信息①,A與軟錳礦中元素化合價的變化可知,錳元素化合價從+4價降低為+2價,所以A中還原產物為MnSO4;
(2)根據框圖:向MnSO4、ZnSO4、Fe2(SO4)3、Al2(SO4)3的混合液中加入MnCO3、Zn2(OH)2CO3后可以獲得氧化鐵和氧化鋁,所以加入MnCO3、Zn2(OH)2CO3的作用就是調節pH,使Fe3+、Al3+沉淀完全,在加熱的環境下,金屬陽離子的水解更徹底,更易形成沉淀而分離,根據IV中的電解反應式為:MnSO4+ZnSO4+2H2O![]() MnO2+Zn+2H2SO4,可知C為硫酸;
MnO2+Zn+2H2SO4,可知C為硫酸;
(3)該實驗的目的就是制備二氧化錳與鋅,因而就需要把氧化鋁、鐵元素、硫元素除去.根據流程圖不難得出該生產中除得到MnO2和Zn以外,還可得到的副產品有硫、氧化鐵、氧化鋁;
(4)根據框圖中轉化消耗的反應物,如果不考慮生產中的損耗,除礦石外,需購買的化工原料是碳酸鈉和硫酸;
(5)要從Na2SO4溶液中得到芒硝(Na2SO4·10H2O),需進行的操作有蒸發濃縮、冷卻結晶、過濾、洗滌、干燥等;
(6)據反應MnSO4+ZnSO4+2H2O![]() MnO2+Zn+2H2SO4可知MnO2、Zn的物質的量之比為1:1,故可設軟錳礦、閃鋅礦的質量分別為x、y,得0.7x ×87:0.8y×97=1:1,解得x:y=1.03。
MnO2+Zn+2H2SO4可知MnO2、Zn的物質的量之比為1:1,故可設軟錳礦、閃鋅礦的質量分別為x、y,得0.7x ×87:0.8y×97=1:1,解得x:y=1.03。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】某興趣小組模擬企業對含鉻廢水(Cr2O72-和Cr3+)處理流程如下。
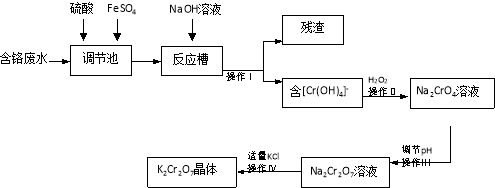
已知:2CrO42-+2H+=Cr2O72-+H2O
請回答:
(1)用離子方程式表示調節池里發生的反應: 。
(2)操作Ⅰ得到的殘渣的化學式為 。
(3)操作Ⅲ調節pH時最適合作為調節劑的是
A.4mol·L-1鹽酸 B.6mol·L-1硫酸
C.石灰乳 D.碳酸鈉
(4)為檢測處理后廢水中鉻的含量,取100mL處理后的樣品于錐形瓶中,用濃醋酸調節pH=5,并加入適量固體抗壞血酸,使Cr2O72-完全轉化為Cr3+,再用amol·L-1的EDTA(用H4Y表示)標準溶液進行滴定,其反應原理為:Cr2O72-→2Cr3+,Cr3++Y4-=CrY-
①滴定時采用右圖所示的側邊自動定零位滴定管,具有的優點 。
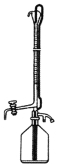
②實驗消耗EDTA標準溶液b mL,則處理后廢液中含鉻濃度為 mg·L-1(用含a、b的式子表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一個原電池的總反應的離子方程式是Zn+Cu2+===Zn2++Cu,該原電池的合理組成
正極 | 負極 | 電解質溶液 | |
A | Zn | Cu | CuCl2 |
B | Cu | Zn | H2SO4 |
C | Cu | Zn | CuSO4 |
D | Zn | Fe | CuCl2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物在空氣中完全燃燒只生成二氧化碳和水,則此有機物
A. 一定含有氧元素
B. 一定不含有氧元素
C. 一定含有碳、氫、氧三種元素
D. 一定含有碳、氫兩種元素,不能確定是否含有氧元素
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】
(1)常溫下,可用鋁和鐵質容器盛裝濃硫酸的原因是 。
(2)但是鋁制容器不能裝NaOH等堿溶液,原因是(用離子方程式表示) 。
(3)工業上冶煉鋁,反應的化學方程式為 。
(4)某實驗小組利用下圖裝置驗證鐵與水蒸氣的反應。
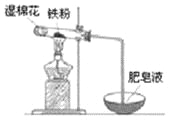
①濕棉花的作用是 ,試管中反應的化學方程式是 。
②實驗結束后,取出少量反應后的固體于試管中,加入過量鹽酸,固體完全溶解,所得溶液中存在的陽離子是 (填序號)。
a.一定有Fe2+、H+和Fe3+b.一定有Fe2+、H+,可能有Fe3+
c.一定有Fe2+、Fe3+,可能有H+d.一定有Fe3+、H+,可能有Fe2+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)用O2將HC1轉化為Cl2,可提高效益,減少污染,傳統上該轉化通過如下圖所示的催化劑循環實現,

其中,反應①為:2HCl(g)+CuO(s) ![]() H2O(g)+CuCl2(s) △H1,反應②生成1 mol Cl2 (g)的反應熱為△H2,則總反應的熱化學方程式為____________________________。(反應熱用△H1和△H2表示)。
H2O(g)+CuCl2(s) △H1,反應②生成1 mol Cl2 (g)的反應熱為△H2,則總反應的熱化學方程式為____________________________。(反應熱用△H1和△H2表示)。
(2)一定條件下測得上述反應過程中c(Cl2)的數據如下:
t(min) | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
c(Cl2)/10-3(mol/L) | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
計算2.0~6.0min內以HCl的物質的量濃度變化表示的反應速率 _________。
(3)常溫下,將除去表面氧化膜的Al、Cu片插入濃HNO3中組成原電池(圖1),測得原電池的電流強度(I)隨時間(t)的變化如圖2所示,反應過程中有紅棕色氣體產生。

0~tl時,原電池的負極是Al片,此時,正極的電極反應式是______________,溶液中的H+向______極移動,tl時,原電池中電子流動方向發生改變,其原因是_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下,容器內某一容器中M、N的物質的量隨反應時間變化的曲線如下圖,下列表述中正確的是
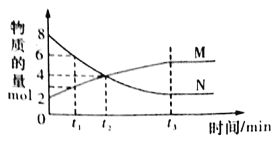
A.反應的化學方程式為:2M![]() N
N
B.t2時,正逆反應速率相等,達到平衡
C.t3時,正反應速率大于逆反應速率
D.t1時,N的濃度是M濃度的2倍
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】亞硝酸鈉被稱為工業鹽,不能用作食品工業,但在漂白、電鍍等方面應用廣泛.現以木炭、濃硝酸、水和銅為原料生成的一氧化氮與過氧化鈉反應制備亞硝酸鈉的裝置如圖所示(部分夾持裝置略).

已知:室溫下,①2NO+Na2O2=2NaNO2②3NaNO2+3HCl═3NaCl+HNO3+2NO↑+H2O;③酸性條件下,NO或NO2﹣ 都能與MnO4﹣反應生成NO3﹣ 和Mn2+
完成下列填空:
(1)寫出濃硝酸與木炭反應的化學方程式 .
(2)B中觀察到的主要現象是有無色氣體產生和 ,D裝置的作用是 .
(3)檢驗C中產物有亞硝酸鈉的方法是 .
(4)經檢驗C產物中除亞硝酸鈉外還含有副產物碳酸鈉和氫氧化鈉,為避免產生這些副產物應在B、C裝置間增加裝置,則該裝置中盛放的藥品名稱 .
(5)將7.8g過氧化鈉完全轉化成為亞硝酸鈉,理論上至少需要木炭 g.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com