
【題目】節日期間因燃放鞭炮會引起空氣中SO2含量增高,造成大氣污染。某實驗小組同學欲探究SO2的性質,并測定空氣中SO2的含量。
(1)他們設計如圖實驗裝置,請你參與探究,并回答問題:
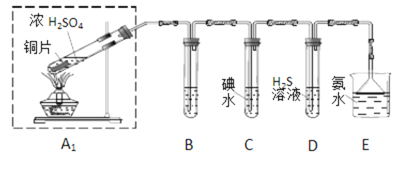
①裝置B用于檢驗SO2的漂白性,其中所盛試劑為______,裝置D用于檢驗SO2的________性質,該裝置中反應的化學方程式為_________________________;
②為了實現綠色環保的目標,甲同學欲用裝置A2代替裝置A1,你認為裝置A2的優點是(寫兩點)_____________、____________;
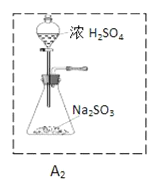
(2)他們擬用以下方法測定空氣中SO2含量(假設空氣中無其他還原性氣體)。

①你認為哪個裝置可行(填序號)_______,使用你所選用的裝置測定SO2含量時,還需要測定的物理量是__________________;
②你認為哪個裝置不可行(填序號)____,說明理由_______________。
【答案】品紅溶液 氧化 SO2+2H2S=3S↓+2H2O 不用加熱(節約能源,節約藥品) 相對安全 a 當KMnO4溶液剛褪色時,測定通入空氣的體積V b 空氣中含有的CO2也能與堿石灰反應,造成測量不準確
【解析】
(1)①SO2具有漂白性,能使品紅溶液褪色;在裝置D中SO2與硫化氫發生反應SO2+2H2S=3S↓+H2O,根據元素化合價的變化判斷物質的作用;
②使用裝置A2的優點是不用加熱,可以節約能源,相對安全,易于控制反應進行,反應更充分等;
(2)①二氧化硫能夠被酸性KMnO4溶液氧化,可以測定空氣中SO2含量;若使用這種方法只需測定當KMnO4溶液剛褪色時,測定通入空氣的體積V即可;
②由于空氣中含有的CO2也能與堿石灰反應,水蒸氣也能被吸收,因此會造成測量不準確,所以b不可行。
(1)①裝置B用于檢驗SO2的漂白性,SO2能與某些有色物質如品紅結合形成無色的物質,因此SO2有漂白性,裝置B用品紅溶液檢驗;
在裝置D中發生反應:SO2+2H2S=3S↓+H2O,反應中SO2中的S元素化合價降低,得到電子,SO2作氧化劑,表現氧化性,H2S作還原劑,表現還原性;
②為了實現綠色環保的目標,甲同學欲用裝置A2代替裝置A1,使用裝置A2的優點是不用加熱,可以節約能源,相對安全;易于控制反應進行;反應更充分等;
(2)①對于裝置a,將含有SO2的空氣通入到KMnO4溶液中,只有SO2能發生反應,所以可以測定空氣中SO2含量;若使用這種方法只需測定當KMnO4溶液恰好褪色時,測定通入空氣的體積V即可,故合理裝置序號是a;
②對于b,由于空氣中含有的CO2也能與堿石灰反應,且其中含有的水蒸氣也能被吸收,因此會造成測量不準確,不能用于測定空氣中SO2含量。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】五種主族元素X、Y、Z、M和N在周期表中的位置如圖所示。下列說法正確的是

A. M的原子半徑比N小
B. Y和Z既可形成Z2Y,也可形成Z2Y2
C. X2M的熱穩定性比X2Y強
D. M和N的氧化物的水化物均為強酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】肼(N2H4)分子中所有原子均達到稀有氣體原子的穩定結構,它的沸點高達113℃,已知肼的球棍模型如圖所示,下列有關說法不正確的是
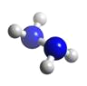
A. 肼是由極性鍵和非極性鍵構成的非極性分子
B. 肼沸點高達113℃,可推測肼分子間能形成氫鍵
C. 肼分子中N原子采用sp2雜化方式
D. 32g肼分子中含有5NA個σ鍵
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】醇脫水是合成烯烴的常用方法,實驗室合成環己烯的反應和實驗裝置如下:
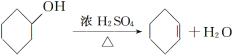

可能用到的有關數據如下:
相對分子質量 | 密度/(g·cm-3) | 沸點/℃ | 溶解性 | |
環己醇 | 100 | 0.961 8 | 161 | 微溶于水 |
環己烯 | 82 | 0.810 2 | 83 | 難溶于水 |
合成反應:在a中加入20 g環己醇和2小片碎瓷片,冷卻攪動下慢慢加入1 mL濃H2SO4,b中通入冷卻水后,開始緩慢加熱a,控制餾出物的溫度不超過90 ℃。
分離提純:反應粗產物倒入分液漏斗中分別用少量5%碳酸鈉溶液和水洗滌,分離后加入無水氯化鈣顆粒,靜置一段時間后棄去氯化鈣,最終通過蒸餾得到純凈環己烯10 g。
回答下列問題:
(1)裝置b的名稱是__________。
(2)本實驗中最容易產生的副產物的結構簡式為_______。
(3)在本實驗分離過程中,產物應該從分液漏斗的_______(填“上口倒出”或“下口放出”)。
(4)分離提純過程中加入無水氯化鈣的目的是______。
(5)在環己烯粗產物蒸餾過程中,不可能用到的儀器有____(填正確答案標號)。
A 圓底燒瓶 B 溫度計 C 吸濾瓶 D 球形冷凝管 E 接收器
(6)以下區分環己烯精品和粗品的方法,合理的是______。
a.用酸性高錳酸鉀溶液 b.用金屬鈉 c.測定沸點
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮、硫、碳的氧化物都會引起環境問題,越來越引起人們的重視。如圖是氮、硫元素的各種價態與物質類別的對應關系:
(1)根據A對應的化合價和物質類別,A為___________(寫分子式),從氮元素的化合價能否發生變化的角度判斷,圖中既有氧化性又有還原性的化合物有____________。
(2)濃、稀硝酸的性質既相似又有差別,若要除去鐵制品表面的銅鍍層應選擇________,反應的離子方程式為______________。
(3)某同學設計了如圖所示的套管實驗裝置(部分裝置未畫出)來制備SO2并利用實驗現象來檢驗其還原性,制備SO2時選用的試劑為Cu和濃H2SO4。回答下列問題:

①寫出制取SO2的化學方程式:_______________。
②該同學利用實驗現象來檢驗SO2的還原性,則選用的試劑為_____。
A. 品紅溶液 B. 酸性高錳酸鉀溶液 C. 雙氧水(H2O2)
(4)工廠里常采用NaOH溶液吸收NO、NO2的混合氣體,使其轉化為化工產品NaNO2,試寫出其化學反應方程式_______。
(5)工業上把海水先進行氧化,再吸收溴,達到富集溴的目的。吸收工藝常用的方法是先用熱空氣吹出Br2,再用SO2吸收Br2。取吸收后的溶液,向其中加入氯化鋇溶液有白色沉淀析出。寫出SO2吸收Br2反應的化學方程式為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】可逆反應A(g)+3B(g)![]() 2C(g)+2D(g) 在4種不同情況下反應速率分別如下,其中反應速率v最大的是
2C(g)+2D(g) 在4種不同情況下反應速率分別如下,其中反應速率v最大的是
A. v(A)=0.15mol/(L·min) B. v (B)=0.6 mol/(L·min)
C. v (C)=0.3 mol/(L·min) D. v (D)=0.1 mol/(L·min)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,取一定量的PbI2固體配成飽和溶液 ,T時刻改變某一條件,離子的濃度變化如圖所示,(注:第一次平衡時c(I-)=2x10-3mol/L, c(Pb2+)=1x10-3mol/L)下列有關說法正確的是

A.常溫下,Ksp=2x10-6
B.溫度不變,向PbI2飽和溶液中加入少量硝酸鉛濃溶液,PbI2的溶解度不變,c(Pb2+)不變
C.T時刻改變的條件是升高溫度,PbI2的,Ksp 增大
D.常溫下Ksp[PbS]=8x10-28,向PbI2的懸濁液中加入Na2S溶液,PbI2(s)+S2-(aq)![]() PbS(s)+2I-(aq)反應的化學平衡常數為5x1018
PbS(s)+2I-(aq)反應的化學平衡常數為5x1018
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】醋酸鎳[(CH3COO)2Ni]是一種重要的化工原料,一種以含鎳廢料(含 NiS、Al2O3、FeO、CaO、SiO2)為原料,制取醋酸鎳的工藝流程圖如下:

相關離子生成氫氧化物的pH和相關物質的溶解性如表:
金屬離子 | 開始沉淀的pH | 沉淀完全的pH | 物質 | 20℃時溶解性(H2O) | |
Fe3+ | 1.1 | 3.2 | CaSO4 | 微溶 | |
Fe2+ | 5.8 | 8.8 | NiF | 可溶 | |
Al3+ | 3.0 | 5.0 | CaF2 | 難溶 | |
Ni2+ | 6.7 | 9.5 | NiCO3 | Ksp=9.6×10﹣6 |
(1)調節pH步驟中,溶液pH的調節范圍是___________。
(2)濾渣1主要成分是_______________;濾渣2主要成分是_________________
(3)寫出氧化步驟中加入H2O2發生反應的離子方程式_________。
(4)酸浸過程中,1mol NiS失去6NA個電子,同時生成兩種無色有毒氣體。寫出該反應的化學方程式____________。
(5)沉鎳過程中,若c(Ni2+)=2.0mol/L,欲使100mL該濾液中的Ni2+沉淀物完全,[c(Ni2+)≤10﹣5 mol/L],則需要加入Na2CO3固體的質量最少為_____g(保留小數點后1位)
(6)保持其他條件不變,在不同溫度下對含鎳廢料進行酸浸。酸浸出率隨時間變化如圖。酸浸的最佳溫度與時間分別為____________。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列化學用語和化學符號使用正確的是
A.次氯酸的結構式可以表示為:H—O—Cl
B.乙醇的結構簡式為:C2H6O
C.含58個質子和82個中子的鈰(Ce)原子符號為:![]() Ce
Ce
D.硫化鈉的電子式:![]()
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com