

分析 (1)(2)根據題中提供的藥品可知,將食鹽溶于濃氨水得飽和食鹽水及濃氨水的混合溶液,用6mol/L的鹽酸與石灰石反應生成CO2,通過蒸餾水除去二氧化碳氣體中少量的氯化氫,將除雜后的二氧化碳通入飽和食鹽水及濃氨水的混合溶液,為了促使碳酸氫鈉的析出,可以將反應容器置于冰水浴中,反應中的尾氣中含有氨氣,所以可以用6mol/L的硫酸溶液吸收反應中的尾氣,據此答題;
(3)根據碳酸氫鈉和碳酸氫銨受熱分解的產物不同判斷是碳酸氫鈉還是碳酸氫銨,根據碳酸氫鈉、食鹽遇鹽酸后的現象判斷是碳酸氫鈉還是食鹽.
解答 解:(1)根據題中提供的藥品可知,將食鹽溶于濃氨水得飽和食鹽水及濃氨水的混合溶液,用6mol/L的鹽酸與石灰石反應生成CO2,通過蒸餾水除去二氧化碳氣體中少量的氯化氫,將除雜后的二氧化碳通入飽和食鹽水及濃氨水的混合溶液,為了促使碳酸氫鈉的析出,可以將反應容器置于冰水浴中,反應中的尾氣中含有氨氣,所以可以用6mol/L的硫酸溶液吸收反應中的尾氣,根據上面的分析可畫出裝置圖為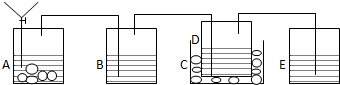 ,
,
答: ;
;
(2)結合(1)的分析,上述裝置中各物質為A.CaCO3,并由漏斗加入6mol/LHCl;B.蒸餾水(或水);C.冰水(或冷水);D.被氯化鈉飽和的濃氨水溶液;E.6mol/LH2SO4,
答:A.CaCO3,并由漏斗加入6mol/LHCl;B.蒸餾水(或水);C.冰水(或冷水);D.被氯化鈉飽和的濃氨水溶液;E.6mol/LH2SO4;
(3)根據碳酸氫鈉和碳酸氫銨受熱分解的產物不同判斷是碳酸氫鈉還是碳酸氫銨,根據碳酸氫鈉、食鹽遇鹽酸后的現象判斷是碳酸氫鈉還是食鹽,實驗操作為取少量產品放在試管中,在酒精燈加熱至不再有氣體放出時,停止加熱.試管中如有白色剩余物質,則得到的產品不是碳酸氫氨,試管冷卻后,向其中加入適量鹽酸,反應激烈,冒大量氣泡,最后剩余物全部溶解,說明得到的結晶是碳酸鈉;如果加入鹽酸后,晶體全部溶解,但沒有氣泡產生,則得到的結晶可能是食鹽,
答:取少量產品放在試管中,在酒精燈加熱至不再有氣體放出時,停止加熱.試管中如有白色剩余物質,則得到的產品不是碳酸氫氨,試管冷卻后,向其中加入適量鹽酸,反應激烈,冒大量氣泡,最后剩余物全部溶解,說明得到的結晶是碳酸鈉;如果加入鹽酸后,晶體全部溶解,但沒有氣泡產生,則得到的結晶可能是食鹽.
點評 本題考查了實驗過程設計,裝置圖連接的注意問題和原則方法,實驗測定成份等知識,掌握基礎是關鍵,題目難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:填空題
| 位置 | A與B相差質子數 | 離子半徑比較 | ||||
| 周期 | 主族 | 縱行 | ||||
| Am+與Bn-相差兩個電子層 | A | |||||
| B | ||||||
| Am+與Bn-相差一個電子層 | A | |||||
| B | ||||||
| Am+與Bn-電子層結構相同 | A | |||||
| B | ||||||
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 組成元素相同,分子結構不同 | |
| B. | 組成元素的質量分數相同,只有化學性質不同 | |
| C. | 具有相同分子量而結構不同 | |
| D. | 具有相同分子量,且組成元素及組成元素的質量分數相同,只是結構不同 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
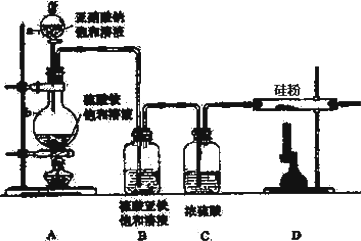
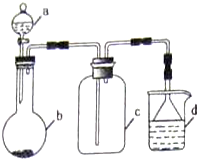
| 選項 | a物質 | b物質 | c收集的氣體 | d中的物質 |
| A | 濃氨水 | NaOH | NH3 | H2O |
| B | 濃硫酸 | Na2SO3 | SO2 | 澄清石灰水 |
| C | 稀硝酸 | Fe | NO2 | H2O |
| D | 濃鹽酸 | KMnO4 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
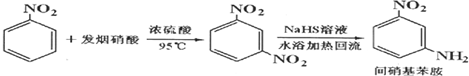
| 參考數據 | 組分 | 鄰硝基苯胺 | 間硝基苯胺 | 對硝基苯胺 | 水 | 甲醇 | 硝基苯 |
| 沸點/℃ | 284 | 305.7 | 331.7 | 100 | 64.7 | 4.75 | |
| 偶極矩/D | 4.38 | 4.91 | 6.33 | 1.85 | 1.69 | 4.75 | |
| 顏色 | 橙色 | 淡黃色 | 淡黃色 | 無色 | 無色 | 淡黃色 |

 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2.2×10-10 mol/L | B. | 2.2×10-12 mol/L | C. | 2.2×10-14 mol/L | D. | 1.1×10-21 mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
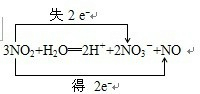 .
.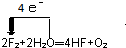 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com