
【題目】2019年諾貝爾化學獎授予約翰·古迪納夫、斯坦利·威廷漢和吉野彰,表彰他們對鋰離子電池研究的貢獻。磷酸亞鐵鋰(LiFePO4)電池是新能源汽車的動力電池之一。采用濕法冶金工藝回收廢舊磷酸亞鐵鋰電池正極片(除LiFePO4外,還含有Al箔、少量不溶于酸堿的導電劑)中的資源,部分流程如圖:

已知:Ksp ( Li2CO3)=1.6×10-3 。部分物質的溶解度(S)如下表所示:
T℃ | S(Li2CO3)/g | S(Li2SO4)/g | S(Li3PO4)/g |
20 | 1.33 | 34.2 | 0.039 |
80 | 0.85 | 30.5 | —— |
100 | 0.72 | —— |
(1)從“正極”可以回收的金屬有___。
(2)寫出堿溶時Al箔溶解的離子方程式___。
(3)磷酸亞鐵鋰電池在工作時,正極發生LiFePO4和FePO4的轉化,該電池充電時正極的電極反應式為___。
(4)酸浸時產生標準狀況下3.36LNO時,溶解 LiFePO4___mol(其他雜質不與HNO3反應),若用H2O2代替HNO3,發生反應的離子方程式為___。
(5)流程中用“熱水洗滌”的原因是___。
(6)若濾液②中c(Li+)=4mol/L,加入等體積的Na2CO3后,Li+的沉降率到90%,計算濾液③中c(CO32-)=___mol/L。
(7)“沉淀”時___(填“能”或“不能”)用Na2SO4溶液代替飽和Na2CO3溶液,原因是___。
【答案】Li、Fe、Al 2Al+2OH-+2H2O=2AlO2-+3H2↑ LiFePO4 -e-=FePO4+Li+ 0.45 H2O2+2H++2Fe2+=2Fe3++2H2O或H2O2+8H++2LiFePO4=2Fe3++2H2O+2H3PO4+2Li+ Li2CO3的溶解度隨溫度升高而減小,熱水洗滌可減少Li2CO3的溶解 0.04 不能 Li2SO4為易溶物
【解析】
正極片經堿溶可得到NaAlO2濾液,含有磷酸亞鐵鋰的濾渣加入硫酸、硝酸,可除去不溶于酸堿的導電劑,得到含有P、Fe、Li的濾液,加入堿液調節pH值,生成的沉淀為FePO4,濾液加入碳酸鈉,可生成碳酸鋰沉淀,以此解答該題。
(1)根據分析流程,堿溶可得到NaAlO2濾液,調節pH值,生成的沉淀為FePO4,加入碳酸鈉,可生成Li2CO3沉淀,可判斷從“正極”可以回收的金屬;
(2)堿溶時Al箔與氫氧化鈉反應生成偏鋁酸鈉和氫氣;
(3)磷酸亞鐵鋰電池在工作時,正極發生還原反應,電極反應式為:FePO4+e-+Li+= LiFePO4該電池充電時正極變為陽極,失電子發生氧化反應,將放電時正極反應倒寫即為陽極電極反應式;
(4)酸浸時HNO3轉化為NO,產生標準狀況下3.36LNO的物質的量為![]() =0.15mol,產生1molNO,轉移3mol電子,則生成0.15molNO轉移0.45mol電子,LiFePO4與硝酸反應轉化為FePO4,Fe的化合價由+2價變為+3價,溶解1mol LiFePO4轉移1mol電子,則轉移0.45mol電子,溶解 LiFePO40.45mol;若用H2O2代替HNO3,H2O2與LiFePO4發生氧化還原反應;
=0.15mol,產生1molNO,轉移3mol電子,則生成0.15molNO轉移0.45mol電子,LiFePO4與硝酸反應轉化為FePO4,Fe的化合價由+2價變為+3價,溶解1mol LiFePO4轉移1mol電子,則轉移0.45mol電子,溶解 LiFePO40.45mol;若用H2O2代替HNO3,H2O2與LiFePO4發生氧化還原反應;
(5)根據表格數據已知條件可得,Li2CO3的溶解度隨溫度升高而減小,熱水洗滌可減少Li2CO3的溶解;
(6)若濾液②中c(Li+)=4mol/L,加入等體積的Na2CO3后,Li+的沉降率到90%,混合后溶液中含有的c(Li+)=4mol/L×(1-90%)×![]() =0.2mol/L,已知:Ksp ( Li2CO3)= c2 (Li+)·c(CO32-)=1.6×10-3,進而計算c(CO32-);
=0.2mol/L,已知:Ksp ( Li2CO3)= c2 (Li+)·c(CO32-)=1.6×10-3,進而計算c(CO32-);
“沉淀”時不能用Na2SO4溶液代替飽和Na2CO3溶液,原因是Li2SO4為易溶物,最終得不到Li2CO3沉淀。
(1)根據分析流程,堿溶可得到NaAlO2濾液,調節pH值,生成的沉淀為FePO4,加入碳酸鈉,可生成Li2CO3沉淀,因此從“正極”可以回收的金屬有Li、Fe、Al,
答案為:Li、Fe、Al;
(2)堿溶時Al箔與氫氧化鈉反應,溶解的離子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑,
答案為:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)磷酸亞鐵鋰電池在工作時,正極發生還原反應,電極反應式為:FePO4+e-+Li+= LiFePO4該電池充電時正極變為陽極,失電子發生氧化反應,將放電時正極反應倒寫即為陽極電極反應式為LiFePO4=FePO4+Li++e-,
答案為:LiFePO4 -e-=FePO4+Li+;
(4)酸浸時HNO3轉化為NO,產生標準狀況下3.36LNO的物質的量為![]() =0.15mol,產生1molNO,轉移3mol電子,則生成0.15molNO轉移0.45mol電子,LiFePO4與硝酸反應轉化為FePO4,Fe的化合價由+2價變為+3價,溶解1mol LiFePO4轉移1mol電子,則轉移0.45mol電子,溶解 LiFePO40.45mol;若用H2O2代替HNO3,H2O2與LiFePO4發生氧化還原反應,反應的離子方程式為H2O2+2H++2Fe2+=2Fe3++2H2O或H2O2+8H++2LiFePO4=2Fe3++2H2O+2H3PO4+2Li+,
=0.15mol,產生1molNO,轉移3mol電子,則生成0.15molNO轉移0.45mol電子,LiFePO4與硝酸反應轉化為FePO4,Fe的化合價由+2價變為+3價,溶解1mol LiFePO4轉移1mol電子,則轉移0.45mol電子,溶解 LiFePO40.45mol;若用H2O2代替HNO3,H2O2與LiFePO4發生氧化還原反應,反應的離子方程式為H2O2+2H++2Fe2+=2Fe3++2H2O或H2O2+8H++2LiFePO4=2Fe3++2H2O+2H3PO4+2Li+,
答案為:0.45;H2O2+2H++2Fe2+=2Fe3++2H2O或H2O2+8H++2LiFePO4=2Fe3++2H2O+2H3PO4+2Li+;
(5)根據表格數據可得,Li2CO3的溶解度隨溫度升高而減小,熱水洗滌可減少Li2CO3的溶解,
答案為:Li2CO3的溶解度隨溫度升高而減小,熱水洗滌可減少Li2CO3的溶解;
(6)若濾液②中c(Li+)=4mol/L,加入等體積的Na2CO3后,Li+的沉降率到90%,混合后溶液中含有的c(Li+)=4mol/L×(1-90%)×![]() =0.2mol/L,已知:Ksp ( Li2CO3)= c2 (Li+)·c(CO32-)=1.6×10-3,則濾液③中c(CO32-)=
=0.2mol/L,已知:Ksp ( Li2CO3)= c2 (Li+)·c(CO32-)=1.6×10-3,則濾液③中c(CO32-)=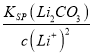 =
=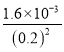 =0.04 mol/L,
=0.04 mol/L,
答案為:0.04;
(7)“沉淀”時不能用Na2SO4溶液代替飽和Na2CO3溶液,原因是Li2SO4為易溶物,最終得不到Li2CO3沉淀,
答案為:Li2SO4為易溶物。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】銅及其化合物在工業生產和日常生活中有著廣泛的應用。
某化學小組擬采用如下裝置(夾持和加熱儀器已略去)來測定銅的相對原子質量,同時檢驗氯氣的氧化性。
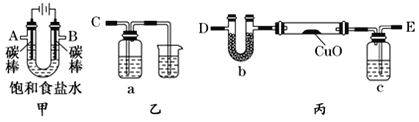
(1)裝置甲中發生反應的化學方程式是:__________。
(2)已知裝置甲中B處有黃綠色的氣體產生,且 B連C ;則A連________(填寫連接的字母)。
(3)乙裝置的a瓶中溶液可以是________(填標號)
A 酸性KMnO4溶液 B CCl4溶液 C 滴加有KSCN溶液的FeCl2溶液 D 飽和食鹽水
(4)在檢查裝置氣密性后,加熱丙裝置硬質玻璃管里的CuO粉末前,還需要進行的操作為________。
(5)準確稱量m g CuO進行實驗,當CuO完全反應后測出b中增重n g。則Cu的相對原子質量為____________(只要求列出算式)。該實驗方案的裝置有不合理之處,若不加以改進會導致測定結果__________ (填“偏大”、“偏小”或“不變”)。
(6)利用焰色反應的原理既可制作五彩繽紛的節日煙花,亦可定性鑒別某些金屬鹽。灼燒CuCl2樣品時,銅的焰色為__________(填標號)。
A 綠色 B 紅色 C 紫色 D 黃色
(7)向CuCl2溶液中通人H2S氣體,可產生CuS沉淀,反應離子方程式為:Cu2+ + H2S=CuS(s) + 2H+,則該反應的平衡常數K=_________(保留一位小數)。已知:CuS溶度積Ksp=1.0×10-36,H2S電離常數Ka1=1.3×10-7,Ka2=7.0×10-15。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】元素周期表是學習化學的重要工具,它隱含著許多信息和規律。下表所列是五種短周期元素的原子半徑及主要化合價(已知鈹的原子半徑為0.089 nm)。
元素代號 | A | B | C | D | E |
原子半徑/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
主要化合價 | +2 | +3 | +6、-2 | -1 | -2 |
(1)用元素代號標出它們在周期表中所對應的位置(以下為周期表的一部分)_________。
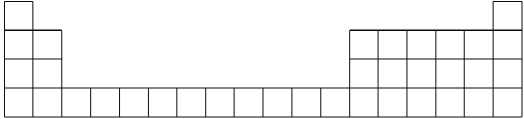
(2)畫出A的原子結構示意圖_________。
(3)B元素處于周期表中第________周期,________族。
(4)E元素處于周期表中第________周期,________族。
(5)C、D的簡單離子的半徑由大到小順序為________(用離子符號表示)。
(6)上述五種元素的最高價氧化物對應的水化物中酸性最強的是__________(填化學式)。
(7)C、E形成的化合物為________(填化學式)。
(8)寫出B單質和氫氧化鈉溶液反應的方程式__________寫出B的最高價氧化物對應水化物和氫氧化鈉溶液反應的離子方程式:________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二氧化硅是一種化工原料,可以制備一系列物質。下列說法正確的是( )
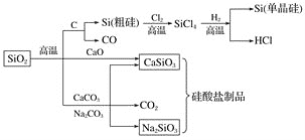
A.圖中所有反應都不屬于氧化還原反應
B.硅酸鹽的化學性質穩定,常用于制造光導纖維
C.可用鹽酸除去石英砂(主要成分為SiO2)中少量的碳酸鈣
D.普通玻璃是由純堿、石灰石和石英砂制成的,其熔點很高
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是以葡萄糖為燃料的微生物燃料電池結構示意圖。關于該電池的敘述不正確的是( )
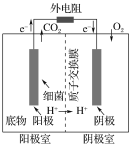
A.該電池不能在高溫下工作
B.電池的負極反應為C6H12O6+6H2O-24e-=6CO2↑+24H+
C.放電過程中,電子從正極區向負極區每轉移1 mol,便有1 mol H+從陽極室進入陰極室
D.微生物燃料電池具有高能量轉換效率、原料較廣泛、操作條件溫和、有生物相容性等優點,值得研究與推廣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組利用圖甲裝置制取氨氣并探究氨氣的有關性質。
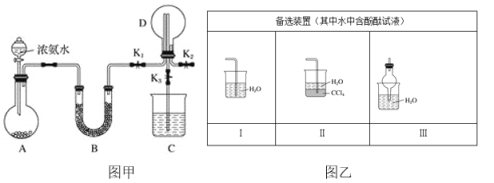
(1)裝置A中燒瓶內試劑可選用__(填序號)。
a.堿石灰 b.濃硫酸 c.五氧化二磷 d.氯化鈣
(2)若探究氨氣的溶解性,當裝置D中集滿氨氣后,關閉K1、K2,打開K3,引發噴泉的實驗操作是__。不能在K2的導管末端連接圖乙中的__裝置(填序號)。
(3)若探究氨氣的還原性,需關閉K1、K3,K2連接純凈、干燥氯氣的裝置。
①用二氧化錳與濃鹽酸制取氯氣,生成的氣體必須依次通過盛有__試劑和__試劑的洗氣瓶。
②D中氨氣與氯氣反應產生白煙,同時生成一種無色無味的氣體,該反應的化學方程式為__。
③尾氣可用C裝置處理,若尾氣中含有少量Cl2,則C裝置中應盛放__溶液(填化學式),反應的離子方程式為__。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中正確的是 ( )
A. 標準狀況下,22.4L水中所含的分子數約為6.02×1023
B. 標準狀況下,aL的氧氣和氮氣的混合物含有的分子數約為![]() ×6.02×1023
×6.02×1023
C. 22 g二氧化碳與標準狀況下11.2 L 氯化氫氣體含有的分子數不同
D. 2.24L CO2中含有的原子數為0.3×6.02×1023
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】依據氧化還原反應:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)設計的原電池如圖所示。請回答下列問題:
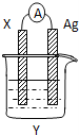
(1)電極X的材料是_______;電解質溶液Y是________;
(2)銀電極上發生的電極反應式為___________________;
(3)外電路中的電子是從______→______;
(4)當有1.6 g銅溶解時,銀棒增重______g 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硼化釩(VB2)—空氣電池是目前儲電能力最高的電池,電池示意圖如下,該電池工作時反應為:4VB2 + 11O2 = 4B2O3 + 2V2O5,下列說法正確的是
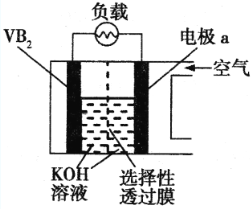
A.電極a為電池負極,發生還原反應
B.每消耗1molVB2轉移6mol電子
C.電池工作時,OH向電極a移動
D.VB2極發生的電極反應為:2VB2+22OH-22e=V2O5+2B2O3+11H2O
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com