
【題目】周期表前四周期的元素A、B、C、D、E、F,原子序數依次增大,A是周期表中原子半徑最小的元素,B的基態原子中只有1個未成對電子,C基態原子中有7種不同運動狀態的電子,D的最外層電子數是其所處周期數的3倍,E與D同主族,F的一價陽離子最外層有18個電子。回答下列問題:
(1)F在周期表中的位置是_____________
(2)A元素與其他元素形成的含氧酸中,酸根呈三角錐結構的酸是_________,該酸的中心原子的雜化方式為_________
(3)CA3極易溶于水,試從下圖中判斷CA3溶于水后形成CA3·H2O的合理結構為_____(填字母代號),推理依據是___________
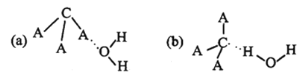
(4)元素B可形成H3BO3,已知H3BO3的電離方程式為H3BO3+2 H2O[B(OH)4]一+H3O+
①基態B、D原子的第一電離能由小到大的順序為__________(用元素符號表示)
②[B(OH)4]一中B原子的雜化類型為_______________
③寫出一種與H3O+互為等電子體的分子的化學式:___________
④H3BO3晶體在熱水中的溶解度大于冷水中的溶解度的原因為__________________
【答案】第四周期IB族 H2SO3 sp3 (b) 一水合氨電離產生銨根離子和氫氧根離子 B<O sp3 NH3、PH3、AsH3等 H3BO3晶體中H3BO3分子間存在氫鍵,加熱可以打破該氫鍵,使得H3BO3分子與水分子間形成氫鍵,從而溶解度更大
【解析】
A是周期表中原子半徑最小的元素,即A為H;C基態原子中7種不同運動狀態的電子,即C為N;D的最外層電子數是其所處周期數的3倍,即D為O;因為E與D同主族,且原子序數增大,即D為O、E為S;F的一價陽離子最外層有18個電子,即F的價電子為3d104s1,即F為Cu。B的基態原子中只有1個未成對電子,原子序數小于氮元素,則B為硼,據此解答。
根據以上分析可知A、B、C、D、E、F分別是H、B、N、O、S、Cu。則:
(1)F為Cu,位于第四周期IB族;
(2)能與H形成含氧酸的是B、N、S,酸根呈三角錐結構,應有3個σ鍵,1個孤電子對,即符合條件的是H2SO3;雜化軌道數等于價層電子對數,SO32-中心原子S的價層電子對數為4,S的雜化類型為sp3;
(3)CA3為NH3,NH3溶于水后,形成NH3·H2O,NH3·H2O為弱堿,其電離方程式為NH3·H2O![]() NH4++OH-,因此合理結構為選項(b);
NH4++OH-,因此合理結構為選項(b);
(4)①同周期從左向右第一電離能增大,因此B的第一電離能小于O;
②根據其離子結構可知,B有4個σ鍵,無孤電子對,因此B的雜化類型為sp3;
③根據等電子體的定義,H3O+原子總數為4,價電子總數為8,因此符合條件的分子為NH3、PH3、AsH3等;
④H3BO3晶體中H3BO3分子間存在氫鍵,加熱可以打破該氫鍵,使得H3BO3分子與水分子間形成氫鍵,從而溶解度更大。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】實驗室需要0.5mol/L CuSO4溶液450mL和0.5mol/L硫酸溶液500mL,根據這兩種溶液的配制情況回答下列問題:
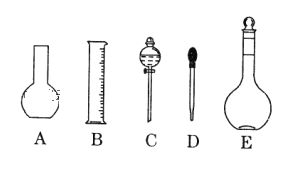
(1)如圖所示的儀器中配制溶液肯定不需要的是 _____(填序號),配制上述 CuSO4溶液需用到的玻璃儀器除了燒杯、玻璃棒、量筒還有_______(填儀器名稱)。
(2)下列操作中,容量瓶所不具備的功能有_________(填序號)。
A.配制一定體積準確濃度的標準溶液 B.貯存溶液
C.測量容量瓶規格以下的任意體積的液體 D.用來加熱溶解固體溶質
(3)配制CuSO4溶液時,如果用CuSO4固體,應該稱量固體的質量為________;如果用CuSO4· 5H2O固體配制,應該稱量固體的質量為__________。配制硫酸溶液時,需要取質量分數為98%、密度為1.84g/cm3的濃硫酸的體積為__________。
(4)下列操作對溶液的濃度有何影響?(填“偏大”、“偏小”、“無影響”)
①沒有對溶解固體時用到的燒杯洗滌_______________。
②使用前容量瓶用蒸餾水洗滌,且沒有干燥_______________。
③配制的過程中有少量的液體迸濺出來_______________。
④定容時不小心加水過量,馬上用膠頭滴管吸出_______________。
⑤定容時俯視刻度線_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】環保、安全的鋁—空氣電池的工作原理如下圖所示,下列有關敘述錯誤的是
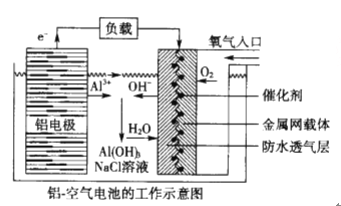
A. NaCl的作用是增強溶液的導電性
B. 正極的電極反應式為: O2+4e-+2H2O=4OH-
C. 電池工作過程中,電解質溶液的pH不斷增大
D. 用該電池做電源電解KI溶液制取1molKIO3,消耗鋁電極的質量為54g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知X、Y和Z三種元素的原子序數之和等于48。X的一種1∶1型氫化物分子中既有σ鍵又有π鍵。Z是金屬元素,Z的單質和化合物廣泛的用途。已知Z的核電荷數小于28,且次外層有2個未成對電子。工業上利用ZO2和碳酸鋇在熔融狀態下制取化合物M(M可看做一種含氧酸鹽)。M有顯著的“壓電性能”,應用于超聲波的發生裝置。經X射線分析,M晶體的最小重復單元為正方體(如圖),邊長為4.03×10-10 m,頂點位置為Z4+所占,體心位置為Ba2+所占,所有棱心位置為O2-所占。
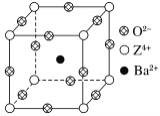
(1) Y在周期表中位于______________;Z4+的核外電子排布式為___________________。
(2)X的該種氫化物分子構型為________,X在該氫化物中以_______方式雜化。X和Y形成的化合物的熔點應該_______(填“高于”或“低于”)X氫化物的熔點。
(3)①制備M的化學方程式是_____________。
②在M晶體中,若將Z4+置于正方體的體心,Ba2+置于正方體的頂點,則O2-處于正方體的________。
③在M晶體中,Z4+的氧配位數為________。
④已知O2-半徑為1.40×10-10 m,則Z4+半徑為____ m。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銅及其化合物在生產生活中有廣泛應用
(1)工業上以黃銅礦(CuFeS2)為原料,采用火法熔煉工藝生產銅的中間過程會發生反應:2Cu2O+Cu2S![]() 6Cu+SO2↑該反應的氧化劑是________________,驗證SO2的方法是________________。
6Cu+SO2↑該反應的氧化劑是________________,驗證SO2的方法是________________。
(2)將少量銅絲放入適量的稀硫酸中,溫度控制在50℃,加入H2O2,反應一段時間后,升溫到60℃,再反應一段時間后可制得硫酸銅。溫度控制在50℃~60℃的原因有:①加快反應速率;②___________。在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加熱,可生成CuC1沉淀,寫出生成CuCl的離子方程式______________。
(3)堿式碳酸銅在有機催化劑、煙火制造和顏料、農藥生產中有廣泛的應用。某工廠以輝銅礦(主要成分為Cu2S,含少量Fe2O3、SiO2等雜質)為原料制備堿式碳酸銅的流程如下:
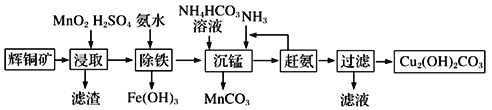
①輝銅礦在浸取前要富集與粉碎,粉碎的好處是___________。
②浸取過程中可得到一種黃色單質,寫出浸取時主要反應的化學方程式___________。
③“除鐵”這一步反應在25℃進行,加入氨水調節溶液pH為4后,溶液中銅離子最大濃度不超過_________mol/L。(已知Ksp[Cu(OH)2]=2.2×10-20)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、X、Y、B、C、D、E、M是前30號元素,原子序數依次增加。A原子是周期表中半徑最小的原子;X的基態原子次外層有2個電子,最外層有3個未成對電子;Y原子的2p軌道上有1個電子的自旋方向與其它電子相反;B的價層電子排布式為ns1,C和Y形成的化合物是引起酸雨的主要大氣污染物,常溫下,D的單質是一種黃綠色的氣體;E的+3價離子的3d軌道為半充滿狀態,M與E元素位于同一周期,且為ⅠB族元素。
(1)B、Y、C分別形成的簡單離子的半徑由大到小順序為(填離子符號)_________
(2)元素D基態原子的核外電子排布式為________,其同周期元素中,第一電離能最大的是______(寫元素符號)。
(3)M與D形成的一種化合物的立方晶胞如圖所示。
①該化合物的化學式為_______
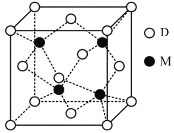
②此化合物的氨水溶液遇到空氣則被氧化為深藍色,深藍色溶液中陽離子的化學式為_______,其中配位體為_______分子(填“極性”或“非極性”),
(4)基態C原子電子占據最高能級的電子云輪廓圖為_______形。將A2C通入ED3溶液中反應的離子方程式為_______
(5)用200mL1mol·L-1的BYA溶液吸收4.48L(標準狀況)CY2所得溶液的pH<7,溶液中離子濃度由大到小的順序為___________________________。
(6)工業上用電化學法治理酸性廢液中XY3的原理如圖,陰極的電極反應式為_______。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)在標準狀況下,取甲、乙、丙各30.0mL相同濃度的鹽酸,然后分別慢慢加入組成相同的鎂鋁合金粉末,得下表中有關數據(假設反應前后溶液體積不發生變化):請回答:
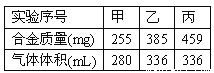
①甲組實驗中,鹽酸(選填“過量”、“適量”或“不足量”,下同)___,乙組實驗中鹽酸___。
②鹽酸的物質的量濃度為___。
③合金中Mg、Al的物質的量之比為___。
(2)甲、乙兩燒杯中各盛1L0.6mol/L的鹽酸和NaOH溶液,向兩燒杯中分別加入等質量的鋁粉,反應結束后測得生成的氣體的體積比V(甲):V(乙)=3:4,則加入鋁粉的質量為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于同溫同壓下等質量的CO和CO2,下列敘述正確的是( )
A. 體積之比為2∶1 B. 體積之比為7∶1
C. 所含原子數之比為22∶21 D. 密度之比為11∶7
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學習小組用圖示裝置測定鋁鎂合金中鋁的質量分數和鋁的相對原子質量。
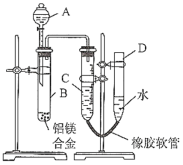
(1)A中試劑為__________________
(2)實驗前,先將鋁鎂合金在稀酸中浸泡片刻,其目的是_______________________________
(3)檢查氣密性,將藥品和水裝入各儀器中,連接好裝置后,需進行的操作還有:①記錄C的液面位置;②將B中剩余固體過濾,洗滌,干燥,稱重;③待B中不再有氣體產生并恢復至室溫后,記錄C的液面位置;④由A向B滴加足量試劑。上述操作的順序是_______________________(填序號)。
(4)B中發生反應的化學方程式為_____________________________________________________
(5)若實驗用鋁鎂合金的質量為ag,測得氫氣體積為bmL(已換算為標準狀況),B中剩余固體的質量為cg,則鋁的相對原子質量為____________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com