
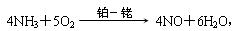
回答下列問題。
(1)合成氨的原料通常各來自何處?_______________________。
(2)已知N2(g)+3H2(g)![]() 2NH3(g),ΔH=-92 kJ。請解釋:
2NH3(g),ΔH=-92 kJ。請解釋:
為有效提高氨的產率,實際生產中宜采取哪些措施?_______________________。
(3)寫出氨催化氧化的化學方程式。鉑銠合金網有何作用?為什么鉑銠合金網未預熱也會發熱?
(4)生產硝酸的過程中常會產生一些氮的氧化物,如何消除它們對大氣的污染?寫出反應的化學方程式。
(5)舉出硝酸銨的兩種主要用途。請解釋為什么該用途對現代社會非常重要。
(6)在一定溫度和壓強的密閉容器中,將平均相對分子質量為8.5的H2和N2混合,當該反應達到平衡時,測出平衡混合氣的平均相對分子質量為10,此時N2的轉化率為________,平衡混合氣體中NH3的體積分數為________。
(7)請你為硝酸廠的選址提出合理化建議。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com