
煙氣中含有一種能與血液中血紅蛋白結合的有毒氣體CO.市場上出現過一種一氧化碳檢測器,其外觀像一張塑料信用卡,正中有一個直徑不到2 cm的小窗口,露出橙紅色固態物質.若發現橙紅色轉為黑色而在短時間內不復原,表明室內一氧化碳濃度超標,有中毒危險.一氧化碳不超標時,橙紅色雖也會變黑卻能很快復原.已知檢測器的化學成分:親水性的硅膠、氯化鈣、固體酸H8[Si(Mo2O7)6]·28H2O、CuCl2·2H2O和PdCl2·2H2O(注:橙紅色為復合色,不必細究).
(1)CO與PdCl2·2H2O的反應方程式為________.
(2)題(1)的產物之一與CuCl2·2H2O反應而復原,化學方程式為________.
(3)題(2)的產物之一復原的反應方程式為________.
|
答案:(1)CO+PdCl2·2H2O (2)Pd+2CuCl2·2H2O 或Pd+CuCl2·2H2O (3)4CuCl+4HCl+6H2O+O2 解析:第一個問題的關鍵是:CO和PdCl2·2H2O誰是氧化劑?當然有兩種正好相反的假設.假設1,得到C和某種高價鈀化合物,假設2,得到CO2和金屬鈀.哪一個假設正確?要從第2問得到啟示.顯然,第2問需要應試者自己得出結論,首先是CuCl2·2H2O不可能是還原劑,只可能是氧化劑,因為在水體系里銅的價態不能再升高.如果應試者沒有這種基本思路,就無法對第1問的兩種假設作出抉擇.有了這種思路,必然對準“(1)中的產物之一”對準C或Pd.問:其中哪一個可以跟CuCl2·2H2O反應?中學課本上討論過碳的氧化,使用的都是強氧化劑,如空氣中的氧氣、濃硫酸、濃硝酸等,而且都需加熱,可見碳不是強還原劑,把它氧化不那么容易,應當排除,于是“定音”,假設2是正確的,這是一箭雙雕,既答了第1問,又答了第2問.當然,第2問又存在兩種可能,銅被還原得銅(1)呢還是得銅(0).怎樣判斷?需要第3問來幫助,第3問要求寫出第2問中產物之一被復原,自然是指銅(1)或銅(0)的復原.先不必問氧化劑是誰,應試者就清楚,銅(1)比銅(0)易復原,即容易被氧化.由此選擇了銅(1)為第2問的答案,完成第2問的解答.再接著思考第3問:使銅(1)復原為銅(2)使用了什么試劑?首先要明確,它一定是氧化劑,然后從檢測器化學組成中去找,找不到,于是被逼到“華容道”上去了,只能選擇空氣中的氧氣,別無他路,全題得解. |


科目:高中化學 來源: 題型:閱讀理解
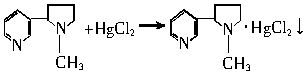 (四)一氧化碳是煙草不完全燃燒的產物。(五)醛類:支氣管受到此類物質的刺激,黏液分泌增多,從而引起呼吸困難,最終會發展成慢性支氣管炎和肺氣腫。
(四)一氧化碳是煙草不完全燃燒的產物。(五)醛類:支氣管受到此類物質的刺激,黏液分泌增多,從而引起呼吸困難,最終會發展成慢性支氣管炎和肺氣腫。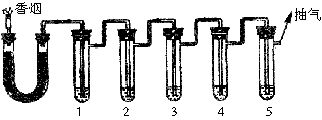
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com