
按要求填空:
A B
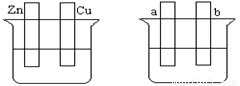
(1)在A圖中,稀硫酸為電解質溶液,用導線連接后,銅片電極反應式 。
(2)在B圖中外接直流電源,若要在a極鍍銅,加以必要的連接后,該裝置叫 ,b極電極反應式 。
(3)在B圖中外接直流電源,若電極為惰性電極,電解質溶液是CuSO4溶液(足量),電解總反應離子方程式為 ,陰極增重3.2 g,則陽極上放出的氣體在標準狀況下的體積是_____L,加入一定量的 后(填化學式),溶液能恢復至與電解前完全一致。
(1)2H+ +2e=H2↑
(2)電鍍池或電鍍,Cu - 2e- = Cu2+。
(3)2Cu2++2H2O 2Cu+O2↑+4H+ 0.56 CuO 。
2Cu+O2↑+4H+ 0.56 CuO 。
【解析】
試題分析:(1)A反應為鋅銅原電池,鋅被氧化成Zn2+進入溶液,電子由鋅片通過導線流向銅片,溶液中的H+從銅片獲得電子,被還原成氫原子。氫原子結合成氫分子從銅片上放出。兩極發生如下反應:負極:Zn-2e-=Zn2+ 正極: 2H+ +2e=H2↑ 銅片上的反應為:2H+ +2e=H2↑
(2)電鍍的條件為:電源、電極、電解質、閉合回路,,而且題中指出要在a極鍍銅,所以此裝置為電鍍池。要在a極鍍銅,那么a極發生的是還原反應,b極發生的是氧化反應,電極反應方程式為:Cu - 2e- = Cu2+.
(3) 在B圖中外接直流電源,若電極為惰性電極,電解質溶液是CuSO4溶液(足量),則此反應的離子反應方程式為2Cu2++2H2O 2Cu+O2↑+4H+,陰極反應方程式為:Cu2++2e-= Cu,又陰極增重3.2g,則增加銅的物質的量為0.05mol,則生成氧氣的物質的量為0.05
mol/2=0.025 mol, 生成氧氣的體積為0.025 mol×22.4L/ mol=0.56L。該反應析出了單質銅和氧氣,根據元素守恒,應向其添加一定量的CuO,溶液能恢復至與電解前完全一致。
2Cu+O2↑+4H+,陰極反應方程式為:Cu2++2e-= Cu,又陰極增重3.2g,則增加銅的物質的量為0.05mol,則生成氧氣的物質的量為0.05
mol/2=0.025 mol, 生成氧氣的體積為0.025 mol×22.4L/ mol=0.56L。該反應析出了單質銅和氧氣,根據元素守恒,應向其添加一定量的CuO,溶液能恢復至與電解前完全一致。
考點:本題著重考查了原電池、電解池、電鍍池的相關知識。


科目:高中化學 來源:2011-2012學年湖南醴陵二中、四中高二下學期期中聯考文科化學試卷(帶解析) 題型:填空題
(6分)根據硝酸和硫酸所具有的性質,選擇適當的字母按要求填空。
| A.吸水性 | B.脫水性 | C.強氧化性 | D.強氧化性和酸性 |
查看答案和解析>>
科目:高中化學 來源:2013屆江西省豐城中學高三階段測試化學試卷(帶解析) 題型:填空題
(8分)現有A、B兩種有機化合物,已知:
①它們的分子中含有相同數目的碳原子和氧原子,B可以看成A中一個氫原子被氨基取代得到;
②它們的分子中氫元素的質量分數相同,相對分子質量都不超過170,A中碳元素的質量分數為72.00%;
③它們都是一取代苯,分子中都沒有甲基,都有一個羧基。
請按要求填空:
⑴A、B的分子中氫元素的質量分數都是___________;
⑵A的結構簡式是________________________;
⑶A有一同分異構體C是對位二取代苯,能發生銀鏡反應也能與金屬鈉反應,但官能團不直接與苯環相連,C的結構簡式是________________________;
⑷B有一同分異構體D是苯環上的一硝基化合物,其苯環和側鏈上的一溴代物各有兩種,D的結構簡式是__________________________。
查看答案和解析>>
科目:高中化學 來源:2012-2013學年浙江省金華一中高二10月月考化學試卷(帶解析) 題型:填空題
已知:⑴環己烯可以通過丁二烯與乙烯發生環化加成反應得到:
⑵實驗證明,下列反應中反應物分子的環外雙鍵比環內雙鍵更容易被氧化:
⑶R-CHO +H2 → R-CH2OH
現僅以丁二烯為有機原料,無機試劑任選,按下列途徑合成甲基環己烷: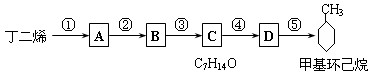
請按要求填空:
⑴A的結構簡式是 ;B的結構簡式是 。
⑵寫出下列反應的化學方程式和反應類型:
反應④ ,反應類型 。
反應⑤ ,反應類型 。
查看答案和解析>>
科目:高中化學 來源:2010年湖南省業水平考試化學卷 題型:填空題
(6分)根據硝酸和硫酸所具有的性質,選擇適當的字母按要求填空。
A、吸水性 B、脫水性 C、強氧化性 D、強氧化性和酸性
(1)濃硫酸常用作干燥劑,說明濃硫酸具有 ;
(2)用玻璃棒蘸濃硫酸滴在紙上,發現變黑,說明濃硫酸具有 ;
(3)濃硫酸和濃硝酸都可以與銅反應,反應中濃硫酸和濃硝酸顯示出 ;
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com