
(本題共12分)六水合高氯酸銅 [Cu(C1O4)2 ·6H2O]是一種藍色晶體,易溶于水,120℃時開始分解。實驗室用硫酸銅的粗產品制備少量高氯酸銅晶體的流程如下:

已知:
|
離子 |
溶液pH值 |
|
|
開始沉淀 |
沉淀完全 |
|
|
Fe2+ |
7.6 |
9.6 |
|
Fe3+ |
2.7 |
3.7 |
|
Cu2+ |
5.2 |
6.4 |
(1).寫出A→B過程中發生反應的離子方程式為 。
(2).溶液C中加入稀硫酸調至pH=1的目的是________________________________________。
(3).如欲檢驗溶液C中的雜質是否除凈,其操作是 。
(4).蒸發至__________(填寫現象),然后經過冷卻結晶、過濾、洗滌、 (填寫操作),得到純凈的藍色晶體。
(5).為了測定硫酸銅的粗產品的純度,某同學稱量硫酸銅的粗產品2.000g、 、 、(填寫實驗步驟)過濾、洗滌沉淀、在空氣中灼燒,至質量不再改變時,稱得質量為0.58816 g。
(6).該樣品的純度為___________。如果樣品的實際純度為93.2%,則測定的相對誤差為__________。
(1).2Fe2++2H++H2O2→2Fe3++2H2O (2分)
(2).防止硫酸銅溶液在蒸發濃縮過程中Cu2+發生水解而得不到純凈的晶體 (2分)
(3).取少量溶液,加入KSCN溶液(NH4SCN溶液),觀察溶液是否仍然為藍色。(2分)
(4).有晶膜出現 低溫烘干 (或自然干燥) (2分)
(5).加水溶解 、加入過量NaOH(aq) (共2分,各1分)
(6).91.9% -1.4%(或-1.39%) (共2分,各1分)
【解析】(1).加入雙氧水的目的是氧化亞鐵離子,方程式為2Fe2++2H++H2O2→2Fe3++2H2O。
(2).由于銅離子水解顯酸性,所以加入稀硫酸可防止硫酸銅溶液在蒸發濃縮過程中Cu2+發生水解而得不到純凈的晶體。
(3)如果雜質沒有除凈,則濾液中一定含有鐵離子,所以用KSCN溶液檢驗即可。
(4).當蒸發有晶膜出現時,即應停止加熱。洗滌之后必須烘干。
(5).要檢驗純度,需要通過沉淀法將銅離子轉化為氫氧化銅沉淀,所以操作是加水溶解、然后加入過量NaOH(aq)即可生成氫氧化銅沉淀。
(6)最后得到的物質是氧化銅,所以根據銅原子守恒可知,硫酸銅晶體的質量是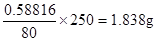 ,所以純度是1.8385÷2×100%=91.9%,所以相對誤差是(91.9%-93.2%)÷93.2%×100%=-1.4%。
,所以純度是1.8385÷2×100%=91.9%,所以相對誤差是(91.9%-93.2%)÷93.2%×100%=-1.4%。


科目:高中化學 來源:2012屆上海市普陀區高三4月質量調研(二模)化學試卷(帶解析) 題型:填空題
(本題共12分)六水合高氯酸銅 [Cu(C1O4)2 ·6H2O]是一種藍色晶體,易溶于水,120℃時開始分解。實驗室用硫酸銅的粗產品制備少量高氯酸銅晶體的流程如下: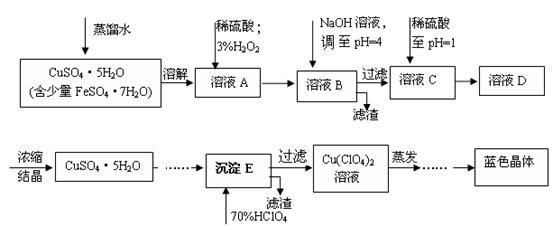
已知:
| 離子 | 溶液pH值 | |
| 開始沉淀 | 沉淀完全 | |
| Fe2+ | 7.6 | 9.6 |
| Fe3+ | 2.7 | 3.7 |
| Cu2+ | 5.2 | 6.4 |
查看答案和解析>>
科目:高中化學 來源:2012屆三校上海市(復旦、交大、華師大二附中)高三聯考化學試卷(帶解析) 題型:填空題
(本題共12分)
化合物A是石油化工的一種重要原料,用A和水煤氣為原料經下列途徑合成化合物D(分子式為C3H6O3)。
已知:




請回答下列問題;
(1)寫出有關物質的結構簡式:A: ;B: ;C: ;D: 。
(2)指出反應⑤的反應類型 。
(3)寫出反應③的化學方程式 。
(4)反應④的目的是 。
化合物D’是D的一種同分異構體,它最早發現于酸牛奶中,是人體內糖類代謝的中間產物。D’在濃硫酸存在的條件下加熱,既可生成能使溴水褪色的化合物E(C3H4O2),又可生成六原子環狀化合物F(C6H8O4)。
請分別寫出D’生成E和F的化學方程式:
(5)D’→E:
(6)D’→F:
查看答案和解析>>
科目:高中化學 來源:2011-2012學年三校上海市)高三聯考化學試卷(解析版) 題型:填空題
(本題共12分)
化合物A是石油化工的一種重要原料,用A和水煤氣為原料經下列途徑合成化合物D(分子式為C3H6O3)。
已知:

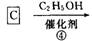


請回答下列問題;
(1)寫出有關物質的結構簡式:A: ;B: ;C: ;D: 。
(2)指出反應⑤的反應類型 。
(3)寫出反應③的化學方程式 。
(4)反應④的目的是 。
化合物D’是D的一種同分異構體,它最早發現于酸牛奶中,是人體內糖類代謝的中間產物。D’在濃硫酸存在的條件下加熱,既可生成能使溴水褪色的化合物E(C3H4O2),又可生成六原子環狀化合物F(C6H8O4)。
請分別寫出D’生成E和F的化學方程式:
(5)D’→E:
(6)D’→F:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com