
對于A+2B(g)![]() nC(g),在一定條件下達到平衡后,改變下列條件,請回答:
nC(g),在一定條件下達到平衡后,改變下列條件,請回答:
(1)A量的增減,平衡不移動,則A為________態。
(2)增大壓強,平衡不移動,當n=2時,A為____ 態;當n=3時,A為______態。
(3)若A為固態,增大壓強,C的組分含量減少,則n_________。
(4)升溫,平衡向右移動,則該反應的逆反應為_______熱反應。
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:閱讀理解
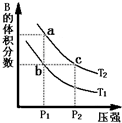 對于反應A(g)?2B(g)△H>0,在溫度為T1、T2時,平衡體系中B的體積分數隨壓強變化的曲線如圖所示.回答下列各題.
對于反應A(g)?2B(g)△H>0,在溫度為T1、T2時,平衡體系中B的體積分數隨壓強變化的曲線如圖所示.回答下列各題.| 時間(s) | 0 | 20 | 40 | 60 | 80 |
| n(B)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(A)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源:09—10年臺州市高二下學期期末考試化學卷 題型:填空題
(14分) 對于反應A(g) 2B(g) DH>0,在溫度為T1、T2時,平衡體系中B的體積分數隨壓強變化的曲線如圖所示。回答下列各題。
2B(g) DH>0,在溫度為T1、T2時,平衡體系中B的體積分數隨壓強變化的曲線如圖所示。回答下列各題。
(1)根據曲線圖,分析下列說法正確的是 ▲ (填字母) 。
A.a、c兩點的反應速率:a 〉c
B.由狀態b到狀態a,可以通過加熱的方法
C.b、c兩點A氣體的轉化率相等
(2)上述反應在密閉容器(定容)中進行,達到平衡狀態的標志是 ▲ (填字母) 。
A.單位時間內生成n mol A的同時分解2n molB
B.兩種氣體的體積分數不再改變
C.v正(A)=2v逆(B)
D.混合氣體的密度不再發生變化
E.混合氣體的壓強不再發生變化
(3)若上述反應達平衡時,B氣體的平衡濃度為0.1 mol·L-1,通過減小體積來增大體系的壓強(溫度保持不變),重新達平衡后,B氣體的平衡濃度 ▲ 0.1 mol·L-1(填“〉”、“〈”或“=”)。
(4)在100℃時,將0.40mol的B氣體充入2L抽空的密閉容器中,每隔一定時間就對該容器內的物質進行分析,得到如下表的數據:
| 時間(s) | 0 | 20 | 40 | 60 | 80 |
| n(B)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(A)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
 2B(g)在100℃時的平衡常數K的值為 ▲ ,升高溫度后,反應2B(g)
2B(g)在100℃時的平衡常數K的值為 ▲ ,升高溫度后,反應2B(g)  A(g)的平衡常數K的值 ▲ (填“增大”、“減小”或“不變”);
A(g)的平衡常數K的值 ▲ (填“增大”、“減小”或“不變”);查看答案和解析>>
科目:高中化學 來源:09-10年臺州市高二下學期期末考試化學卷 題型:填空題
(14分) 對于反應A(g) 2B(g) DH>0,在溫度為T1、T2時,平衡體系中B的體積分數隨壓強變化的曲線如圖所示。回答下列各題。

(1)根據曲線圖,分析下列說法正確的是 ▲ (填字母) 。
A.a、c兩點的反應速率:a 〉c
B.由狀態b到狀態a,可以通過加熱的方法
C.b、c兩點A氣體的轉化率相等
(2)上述反應在密閉容器(定容)中進行,達到平衡狀態的標志是 ▲ (填字母) 。
A.單位時間內生成n mol A的同時分解2n molB
B.兩種氣體的體積分數不再改變
C.v正(A)=2v逆(B)
D.混合氣體的密度不再發生變化
E.混合氣體的壓強不再發生變化
(3)若上述反應達平衡時,B氣體的平衡濃度為0.1 mol·L-1 ,通過減小體積來增大體系的壓強(溫度保持不變),重新達平衡后,B氣體的平衡濃度 ▲ 0.1 mol·L-1(填“〉”、“〈”或“=”) 。
(4)在100℃時,將0.40mol的B氣體充入2L抽空的密閉容器中,每隔一定時間就對該容器內的物質進行分析,得到如下表的數據:
|
時間(s) |
0 |
20 |
40 |
60 |
80 |
|
n(B)/mol |
0.40 |
n1 |
0.26 |
n3 |
n4 |
|
n(A)/mol |
0.00 |
0.05 |
n2 |
0.08 |
0.08 |
① 在上述條件下,從反應開始至40s時,以A氣體表示的該反應的平均反應速率為 ▲ ;
② 上表中n3 ▲ n4(填“〉”、“〈”或“=”),反應A(g) 2B(g)在100℃時的平衡常數K的值為 ▲ ,升高溫度后,反應2B(g) A(g)的平衡常數K的值 ▲ (填“增大”、“減小”或“不變”);
③ 若在相同情況下最初向該容器中充入的是A氣體,要達到上述同樣的平衡狀態,A氣體的起始濃度為 ▲ mol·L-1 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com