
分析 常溫下0.0001mol/LKOH溶液中c(OH-)=c(KOH)=0.0001mol/L,則c(H+)=$\frac{{K}_{w}}{c(O{H}^{-})}$,pH=-lgc(H+).
解答 解:常溫下0.0001mol/LKOH溶液中c(OH-)=c(KOH)=0.0001mol/L,則c(H+)=$\frac{{K}_{w}}{c(O{H}^{-})}$=$\frac{1{0}^{-14}}{1{0}^{-4}}$mol/L=10-10mol/L,pH=-lgc(H+)=-lg10-10=10,
答:常溫下0.0001mol/LKOH溶液的pH=10.
點評 本題考查溶液pH計算,為高頻考點,明確pH值計算方法是解本題關鍵,注意酸堿混合溶液pH的計算方法.


科目:高中化學 來源: 題型:選擇題
| A. | 光導纖維中所用材料為晶體硅 | B. | 水玻璃可用作木材防火劑 | ||
| C. | 氯氣可用于自來水的殺菌消毒 | D. | Fe2O3可以做油漆的顏料 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
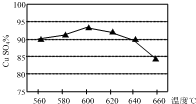 將某黃銅礦(主要成分為CuFeS2)和O2在一定溫度范圍內(nèi)發(fā)生反應,反應所得固體混合物X中含有CuSO4、FeSO4、Fe2(SO4)3及少量SiO2等,除雜后可制得純凈的膽礬晶體(CuSO4•5H2O).
將某黃銅礦(主要成分為CuFeS2)和O2在一定溫度范圍內(nèi)發(fā)生反應,反應所得固體混合物X中含有CuSO4、FeSO4、Fe2(SO4)3及少量SiO2等,除雜后可制得純凈的膽礬晶體(CuSO4•5H2O).| 粒子 | Cu2+ | Fe2+ | Fe3+ |
| 開始沉淀時的pH | 4.7 | 5.8 | 1.9 |
| 完全沉淀時的pH | 6.7 | 9.0 | 3.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溫度 | 973K | 1173K |
| K1 | 1.47 | 2.15 |
| K2 | 2.33 | 1.67 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
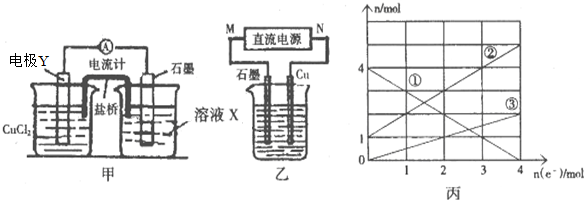
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 10g CO和10g N2 | B. | 10g C2H4和10g C3H6 | ||
| C. | 5.6L O2(標準狀況)和0.5mol H2O | D. | 224mL He(標準狀況)和1.6g CH4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3.0mol•L-1 | B. | 3.5mol•L-1 | C. | 4.0mol•L-1 | D. | 8.0mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③⑦ | B. | ②⑤⑥ | C. | ②③⑦ | D. | ④⑤⑥ |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com