
【題目】鋁及其合金在生活、生產中有廣泛應用。
(1)最新研究表明:氫氧化鋁溶于氫氧化鈉溶液中生成Na[Al(OH)4]。則氫氧化鋁在水中發生酸式電離的電離方程式為________________________________。
(2)目前,國內對真空碳熱還原-氯化法冶煉鋁的研究較多,利用該方法冶煉金屬鋁,既節能又環保。
已知:①Al2O3(s)+AlCl3(g)+3C(s)=====3AlCl(g)+3CO(g) △H1
②3AlCl(g)====2Al(l)+AlCl3(g) △H2
③Al(l)====Al(s) △H3
則Al2O3(s)+3C(s)====2Al(s)+3CO(g) △H4=___________(用含△H1、△H2、△H3的代數式表示)。
(3)已知:Al4C3是真空碳熱還原-氯化法冶煉鋁的中間產物,它與水反應生成氣體Y,Y是含氫量最大的烴。向2L恒容密閉容器中充入2mol Y和2mol水蒸氣,一定條件下發生反應a Y(g)+bH2O(g) ![]() c CO(g)+dH2(g) △H。測得Y的平衡轉化率α(Y)與溫度、壓強的關系如圖所示。
c CO(g)+dH2(g) △H。測得Y的平衡轉化率α(Y)與溫度、壓強的關系如圖所示。

①上述反應的△H_______0(填“>”“<”或“=”)。
②圖象中,x_________0.1(填“>”“<”或“=”)。
③在T0K、0.1MPa時,上述反應的平衡常數K=____________。
④提高上述反應的反應速率的措施有_______________________________ (任填二項)。
⑤從上述反應體系中分離出H2(還含有少量CO)作為合成氨的原料氣,為避免CO使催化劑中毒,原料氣在通入合成塔之前需與適量NH3混合,并用[Cu(NH3)2]Ac溶液吸收CO,反應原理為[Cu(NH3)2]Ac(aq)+CO(g)+NH3(g) ![]() [Cu(NH3)3]Ac·CO(aq) △H<0。若從溫度、壓強兩方面考慮,用[Cu(NH3)2]Ac溶液吸收CO的適宜條件是________________________。
[Cu(NH3)3]Ac·CO(aq) △H<0。若從溫度、壓強兩方面考慮,用[Cu(NH3)2]Ac溶液吸收CO的適宜條件是________________________。
(4)我國首創的海水電池以鋁板為負極,以接觸空氣的鐵鉑合金網為正極,以弱堿性的海水為電解質溶液,電池總反應為4Al+3O2+6H2O===4Al(OH)3。試寫出海水電池的正極反應式:________。
【答案】 Al(OH)3+H2O![]() [Al(OH)4]+H ΔH1+ΔH2+2ΔH3 > < 6.75 mol2·L2 使用催化劑、增大反應物濃度、升高溫度 低溫、高壓 O2+4e+2H2O===4OH
[Al(OH)4]+H ΔH1+ΔH2+2ΔH3 > < 6.75 mol2·L2 使用催化劑、增大反應物濃度、升高溫度 低溫、高壓 O2+4e+2H2O===4OH
【解析】(1)氫氧化鋁在水中發生酸式電離的電離方程式為 Al(OH)3+H2O![]() [Al(OH)4]+H ;(2)①Al2O3(s)+AlCl3(g)+3C(s)=====3AlCl(g)+3CO(g) △H1,②3AlCl(g)====2Al(l)+AlCl3(g) △H2,③Al(l)====Al(s) △H3,由蓋斯定律,①+②+2③,則Al2O3(s)+3C(s)====2Al(s)+3CO(g) △H4=ΔH1+ΔH2+2ΔH3 ;(3)Al4C3是真空碳熱還原-氯化法冶煉鋁的中間產物,它與水反應生成氣體Y,Y是含氫量最大的烴。Y為CH4①由圖可知:升高溫度,平衡轉化率α(Y)增大,a Y(g)+bH2O(g)
[Al(OH)4]+H ;(2)①Al2O3(s)+AlCl3(g)+3C(s)=====3AlCl(g)+3CO(g) △H1,②3AlCl(g)====2Al(l)+AlCl3(g) △H2,③Al(l)====Al(s) △H3,由蓋斯定律,①+②+2③,則Al2O3(s)+3C(s)====2Al(s)+3CO(g) △H4=ΔH1+ΔH2+2ΔH3 ;(3)Al4C3是真空碳熱還原-氯化法冶煉鋁的中間產物,它與水反應生成氣體Y,Y是含氫量最大的烴。Y為CH4①由圖可知:升高溫度,平衡轉化率α(Y)增大,a Y(g)+bH2O(g) ![]() c CO(g)+dH2(g),平衡正向移動,上述反應的△H>0;②向2L恒容密閉容器中充入2mol Y和2mol水蒸氣,一定條件下發生反應a Y(g)+bH2O(g)
c CO(g)+dH2(g),平衡正向移動,上述反應的△H>0;②向2L恒容密閉容器中充入2mol Y和2mol水蒸氣,一定條件下發生反應a Y(g)+bH2O(g) ![]() c CO(g)+dH2(g) ,該反應為 CH4(g)+1H2O(g)
c CO(g)+dH2(g) ,該反應為 CH4(g)+1H2O(g) ![]() 1CO(g)+3H2(g) ,由圖平衡轉化率α(Y)增大,平衡正向移動,再根據方程式的計量數,平衡向正向移動,應是減小壓強,故圖象中,x<0.1;
1CO(g)+3H2(g) ,由圖平衡轉化率α(Y)增大,平衡正向移動,再根據方程式的計量數,平衡向正向移動,應是減小壓強,故圖象中,x<0.1;
③在T0K、0.1MPa時,平衡轉化率α(Y)=0.5時
CH4(g)+1H2O(g) ![]() 1CO(g)+3H2(g)
1CO(g)+3H2(g)
c始 1 1
c變 0.5 0.5 0.5 1.5
c平 0.5 0.5 0.5 1.5
上述反應的平衡常數K=![]() =6.75 mol2·L2。
=6.75 mol2·L2。
④提高上述反應的反應速率的措施有使用催化劑、增大反應物濃度、升高溫度等(任填二項)。⑤[Cu(NH3)2]Ac(aq)+CO(g)+NH3(g) ![]() [Cu(NH3)3]Ac·CO(aq) △H<0。若從溫度、壓強兩方面考慮,用[Cu(NH3)2]Ac溶液吸收CO的適宜條件是:低溫和高壓,低溫和高壓條件下,氣體溶解度大。(4)氧氣在正極得電子,被還原,海水電池的正極反應式: O2+4e+2H2O===4OH。
[Cu(NH3)3]Ac·CO(aq) △H<0。若從溫度、壓強兩方面考慮,用[Cu(NH3)2]Ac溶液吸收CO的適宜條件是:低溫和高壓,低溫和高壓條件下,氣體溶解度大。(4)氧氣在正極得電子,被還原,海水電池的正極反應式: O2+4e+2H2O===4OH。


 金牌教輔培優優選卷期末沖刺100分系列答案
金牌教輔培優優選卷期末沖刺100分系列答案科目:高中化學 來源: 題型:
【題目】有關物質的轉化關系如圖所示(部分物質與條件己略去).A是最常見的無色液體,B、C是常見的金屬單質,D、E是氣體單質,且D在空氣中的含量最多,F 是一種具有磁性的化合物,H是既能與強酸反應又能與強堿反應的氧化物:I具有耐高溫、抗沖擊、導熱性好的優良性質,廣泛應用于電子工業、陶瓷工業中. 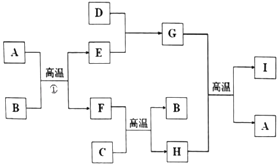
請回答下列問題:
(1)H的化學式為 .
(2)D 的電子式為 .
(3)K出反應①的化學方程式: .
(4)寫出G的水溶液與C的硝酸鹽溶液反應的方程式: .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列指定反應的離子方程式正確的是
A. 氯氣溶于水:Cl2 + H2O ![]() 2 H
2 H![]() + Cl
+ Cl![]() + ClO
+ ClO![]()
B. NH4HSO4溶液呈酸性的主要原因是:NH4++ H2O ![]() NH3·H2O+ H+
NH3·H2O+ H+
C. 酸性溶液中KIO3與KI反應生成I2:IO![]() + I
+ I![]() + 6 H
+ 6 H![]() = I2 + 3 H2O
= I2 + 3 H2O
D. NaHCO3溶液中加足量Ba(OH)2溶液:HCO![]() + Ba
+ Ba![]() + OH
+ OH![]() = BaCO3↓+ H2O
= BaCO3↓+ H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】煤燃燒排放的煙氣含有SO2和NOx,形成酸雨、污染大氣,采用NaClO2溶液作為吸收劑可同時對煙氣進行脫硫、脫硝,回答下列問題:
(1)NaClO2中氯元素的化合價為______________。
(2)在鼓泡反應器中通入含有SO2和NOx的煙氣,反應溫度為323 K,NaClO2溶液濃度為5×103mol/L,溶液呈堿性。反應一段時間后溶液中離子濃度的分析結果如下表
離子 | SO42 | SO32 | NO3 | NO2 | Cl |
c/(mol/L) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
①以NO轉化為NO3-為例,寫出NaClO2溶液脫硝過程中主要反應的離子方程式__________。增加壓強,NO的轉化率__________(填“提高”“不變”或“降低”)。
②隨著吸收反應的進行,吸收劑溶液的pH逐漸___________(填“提高”“不變”或“降低”)。
③由實驗結果可知,脫硫反應速率脫硝反應速率__________(填“大于”或“小于”)。原因是除了SO2和NO在煙氣中的初始濃度不同,還可能是________________________________。
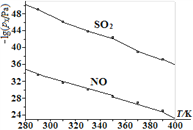
(3)在不同溫度下,NaClO2溶液脫硫、脫硝的反應中,SO2和NO的平衡分壓px如圖所示。已知圖中: ![]() 其中(nx代表各成分的物質的量,na代表氣體總物質的量)
其中(nx代表各成分的物質的量,na代表氣體總物質的量)
①由圖分析可知,反應溫度升高,脫硫、脫硝反應的平衡常數均____(填“增大”“不變”或“減小”)。
②反應ClO2+2SO32==2SO42+Cl的平衡常數K表達式為______________。
(4)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到較好的煙氣脫硫效果。從化學平衡原理分析,Ca(ClO)2相比NaClO具有的優點是______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
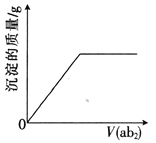
【題目】短周期主族元素a、b、c、d、e的原子序數依次增大,b是地殼中含量最高的元素,e的單質的熔點在同周期元素中最高,a、b的原子序數之和等于e的原子序數,d原子的核外電子層數等于最外層電子數:分別向cdb2溶液、c2eb3溶液中通入氣體ab2,產生沉淀的質量與通入氣體的體積的定性關系都可用右圖表示。下列說法不正確的是
A. 原子半徑:c>d>e>a>b
B. 工業上通常采用ab高溫還原d2b3的方法冶煉d的單質
C. 同溫下,0.1mol·L-1c2eb3溶液的pH大于0.1mol·L-1c2ab3溶液
D. 簡單氫化物的熱穩定性:b>a>e
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖是部分短周期元素原子半徑與原子序數的關系圖.則下列說法正確的是( )

A. 簡單離子的半徑:X<Z<M
B. 最高價氧化物對應水化物的酸性:R<N
C. Y、R兩種元素的氣態氫化物穩定性:Y>R
D. 由X與N兩種元素組成的化合物不能與任何酸反應,但能與強堿反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某探究小組設計如右圖所示裝置(夾持、加熱儀器略),模擬工業生產進行制備三氯乙醛(CCl3CHO)的實驗。查閱資料,有關信息如下:
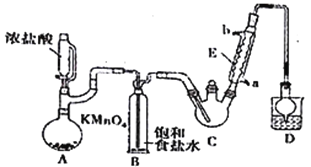
①制備反應原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能發生的副反應: C2H5OH+HCl→C2H5Cl+H2O;
CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相關物質的部分物理性質:
C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
相對分子質量 | 46 | 147.5 | 163.5 | 64.5 |
熔點/℃ | -114.1 | -57.5 | 58 | -138.7 |
沸點/℃ | 78.3 | 97.8 | 198 | 12.3 |
溶解性 | 與水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇 三氯乙醛 | 微溶于水,可溶于乙醇 |
(1)儀器A中發生反應的化學方程式為_________________________________。
(2)裝置B的作用是_________________。該實驗在裝置中有一處缺陷,即缺少氯氣的干燥裝置,缺少該裝置可能導致裝置C 中副產物______________(填化學式)的量增加;冷凝管的進水口是________(填“a”或“b”);
(3)裝置中球形冷凝管的作用是______________________,寫出D中所有可能發生的無機反應的離子方程式___________________________________。
(4)反應結束后,從C中的混合物中分離出CCl3COOH的方法是_________________________。
(5)測定產品純度:稱取產品0.50g配成待測溶液,加0.1000 molL-1碘標準溶液20.00 mL,再加入適量Na2CO3溶液,反應完全后,加鹽酸調節溶液的pH,立即用0.02000 molL-1Na2S2O3溶液滴定至終點。進行三次平行實驗,測得消耗Na2S2O3溶液20.00mL。則產品的純度為_____________;(計算結果保留兩位有效數字)滴定的反應原理:CCl3CHO+OH-==CHCl3span>+HCOO- HCOO-+I2== H++2I-+CO2↑ I2+2S2O32-==2I-+ S4O62-
(6)為證明三氯乙酸的酸性比乙酸強。某學習小組的同學設計了以下三種方案,你認為能夠達到實驗目的的是___________。
a.分別測定0.1mol·L-1兩種酸溶液的pH,三氯乙酸的pH 較小
b.用儀器測量濃度均為0.1mol·L-1 的三氯乙酸和乙酸溶液的導電性,測得乙酸溶液的導電性弱
c.測定等物質的量濃度的兩種酸的鈉鹽溶液的pH,乙酸鈉溶液的pH 較大
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com