
【題目】實驗室用密度為1.25g·mL-1,質量分數36.5%的濃鹽酸配制0.1mol·L-1的鹽酸240mL,請回答下列問題:
(1)濃鹽酸的物質的量濃度為_______。
(2)配制240 mL0.1mol·L-1的鹽酸應選用_______mL的容量瓶,需要量取濃鹽酸體積為_______mL。
(3)定容時,除了燒杯、玻璃棒、容量瓶外,還需要的玻璃儀器是_______。
(4)正確的操作順序是________(填序號)
①用膠頭滴管逐滴加水,使溶液凹液面恰好與容量瓶刻度線相切
②向容量瓶中加水至液面接近瓶頸上的刻度線1-2cm處
③根據計算,用量筒稱取一定體積的濃鹽酸
④將容量瓶蓋緊,振蕩,搖勻
⑤將濃鹽酸倒入燒杯中加水稀釋,并不斷用玻璃棒攪拌,靜置待其冷卻
⑥將溶液用玻璃棒引流注入查漏過的容量瓶中
⑦少量水洗滌燒杯及玻璃棒2至3次,并將每次的洗滌液也注入容量瓶中
(5)下列操作對所配溶液的濃度大小有何影響 (填“偏大”、“偏小”或“無影響”)。
①定容時,俯視刻度線,濃度_________;
②定容搖勻后發現溶液凹面低于刻度線,加水至刻度線,濃度________。
【答案】12.5mol/L 250 2.0 膠頭滴管 ③⑤⑥⑦②①④ 偏大 偏小
【解析】
(1)依據c=![]() 計算濃鹽酸的物質的量濃度;
計算濃鹽酸的物質的量濃度;
(2)依據配制溶液體積選擇合適規格的容量瓶;依據溶液稀釋前后所含溶質的物質的量不變計算需要濃鹽酸的體積;
(3)根據配制溶液的步驟確定使用的儀器;
(4)依據配制溶液的操作判斷操作順序;
(5)根據c=![]() 進行誤差分析。
進行誤差分析。
(1)根據物質的量濃度與質量分數換算式,可知密度為1.25gmL-1,質量分數36.5%的濃鹽酸物質的量濃度c=![]() mol/L=12.5 mol/L;
mol/L=12.5 mol/L;
(2)配制240mL0.1mol/L的鹽酸應選用250mL容量瓶;實際配制250mL溶液,設需要濃鹽酸的體積為V,依據溶液稀釋前后所含溶質的物質的量不變得V×12.5mol/L=250mL×0.1mol/L,解得V=2.0ml;
(3)配制一定體積一定物質的量濃度的溶液的步驟是計算、量取、稀釋、冷卻、移液、洗滌、定容、搖勻。在定容時,除了燒杯、玻璃棒、容量瓶外,還需要的玻璃儀器是膠頭滴管;
(4)配制一定體積一定物質的量濃度的溶液的步驟是計算、量取、稀釋、冷卻、移液、洗滌、定容、搖勻,故操作順序序號為③⑤⑥⑦②①④。
(5)①定容時,俯視刻度線,導致溶液體積偏小,則配制的溶液濃度偏大;
②定容搖勻后發現溶液凹面低于刻度線,加水至刻度線,導致部分溶質損耗溶質的物質的量偏小,使配制的溶液濃度偏小。


 字詞句段篇系列答案
字詞句段篇系列答案科目:高中化學 來源: 題型:
【題目】下列離子方程式書寫正確的是
A.稀硫酸和氫氧化鋇溶液反應:SO42-+Ba2+ =BaSO4↓
B.金屬鈉與水反應:Na+2H+=Na++H2↑
C.大理石與鹽酸反應:CaCO3+2H+ =H2O+CO2↑+ Ca2+
D.氯氣通入冷水中:Cl2+ H2O=ClO-+Cl-+2H+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H2S在金屬離子的鑒定分析、煤化工等領域都有重要應用。請回答:
Ⅰ.工業上一種制備H2S的方法是在催化劑、高溫條件下,用天然氣與SO2反應,同時生成兩種能參與大氣循環的氧化物。
(1)該反應的化學方程式為_____________。
Ⅱ.H2S可用于檢測和沉淀金屬陽離子。
(2)H2S的第一步電離方程式為________。
(3)已知:25 ℃時,Ksp(SnS)=1.0×10-25,Ksp(CdS)=8.0×10-27。該溫度下,向濃度均為0.1 mol·L-1的CdCl2和SnCl2的混合溶液中通入H2S,當Sn2+開始沉淀時,溶液中c(Cd2+)=________(溶液體積變化忽略不計)。
Ⅲ.H2S是煤化工原料氣脫硫過程的重要中間體。反應原理為
ⅰ.COS(g)+H2(g) ![]() H2S(g)+CO(g) ΔH=+7 kJ·mol-1;
H2S(g)+CO(g) ΔH=+7 kJ·mol-1;
ⅱ.CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH=-42 kJ·mol-1。
CO2(g)+H2(g) ΔH=-42 kJ·mol-1。
(4)已知:斷裂1 mol分子中的化學鍵所需吸收的能量如表所示。
分子 | COS(g) | H2(g) | CO(g) | H2S(g) | H2O(g) | CO2(g) |
能量/(kJ·mol-1) | 1 319 | 442 | x | 678 | 930 | 1 606 |
表中x=________。
(5)向10 L容積不變的密閉容器中充入1 mol COS(g)、1 mol H2(g)和1 mol H2O(g),進行上述兩個反應。其他條件不變時,體系內CO的平衡體積分數與溫度(T)的關系如圖所示。
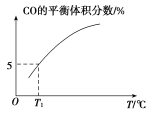
①隨著溫度升高,CO的平衡體積分數_____(填“增大”或“減小”)。原因為_______
②T1℃時,測得平衡時體系中COS的物質的量為0.80 mol。則該溫度下,COS的平衡轉化率為_____;反應ⅰ的平衡常數為_____(保留兩位有效數字)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于合成氨N2(g)+3H2(g) ![]() 2NH3(g)ΔH=-92.4 kJ·mol-1反應,達到平衡后,以下分析正確的是
2NH3(g)ΔH=-92.4 kJ·mol-1反應,達到平衡后,以下分析正確的是
A. 升高溫度,對正反應的反應速率影響更大
B. 增大壓強,對正反應的反應速率影響更大
C. 減小反應物濃度,對逆反應的反應速率影響更大
D. 加入催化劑,對逆反應的反應速率影響更大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有一包固體粉末,由CaCO3、Na2SO4、KNO3、BaCl2、CuSO4中的三種物質組成,取樣品進行如圖實驗,從實驗可以判斷:( )

A.該固體粉末中一定不含有BaCl2
B.該固體粉末中一定含有KNO3
C.它的組成可能是CaCO3、BaCl2、Na2SO4
D.它的組成一定是CaCO3、Na2SO4、KNO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在給定條件下,下列選項所示的物質間轉化均能實現的是( )
A. N2![]() NO2
NO2![]() HNO3
HNO3
B. 石油![]() CH3CH3
CH3CH3![]() CH2BrCH2Br
CH2BrCH2Br
C. Al ![]() Al(NO3)3(aq)
Al(NO3)3(aq)![]() Al(OH)3(s)
Al(OH)3(s)
D. CH2=CH2 ![]() CH3CH2OH
CH3CH2OH![]() CH3CHO
CH3CHO
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲圖是部分短周期元素的常見化合價與原子序數的關系圖:
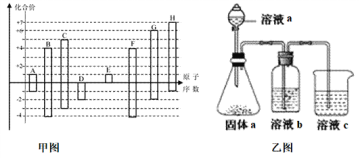
請回答下列問題:
(1)D元素在周期表中的位置為___________,D和G的簡單氫化物中沸點高的是___________(寫化學式),A和E形成的化合物的電子式為_____________。
(2)D、E、G、H的簡單離子半徑由大到小的順序為__________________________。(用化學式表示)
(3)H的最高價氧化物對應的水化物的濃溶液不穩定,受熱可分解,產物之一是H的單質,且當有28mol電子轉移時,常溫共產生9mol氣體,寫出該反應的化學方程式_________________。
(4)由上述元素中的幾種組成a、b、c各物質,某同學設計實驗用乙圖裝置證明元素B、C、F的非金屬性強弱(其中溶液b和溶液c均為足量)。
①溶液a和b分別為________,________(填化學式)。
②溶液c中的離子方程式為__________________________________________。
③請從原子結構的角度解釋非金屬性C>B的原因____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】海洋資源的利用具有廣闊前景。
(1)海水淡化的方法有_____(選填一種即可)。
(2)從海水中提取溴的主要步驟是向濃縮的海水中通入氯氣,將溴離子氧化,該反應的離子方程式是____。
(3)下圖是從海水中提取鎂的簡單流程。
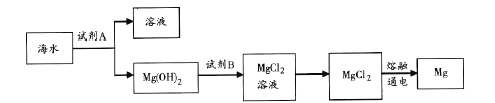
工業上常用于沉淀Mg2+的試劑A 的俗名是___,Mg(OH)2轉化為MgCl2 的離子方程式是_______。
(4)海帶灰中富含以I-形式存在的碘元素。實驗室提取I2 的途徑如下所示:
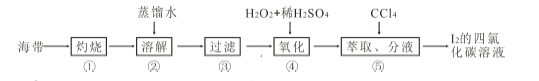
①灼燒海帶至灰燼時所用的主要儀器名稱是_______。步驟②加熱煮沸一會的目的是______________。
② 步驟④向濾液中加H2O2 和稀H2SO4 溶液,寫出該反應的離子方程式_______________。反應結束后,再加入CCl4 作萃取劑,振蕩、靜置,可以觀察到CCl4 層呈____________色。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碲化鈉(Na2Te)可用作有機合成試劑及縮合反應中的催化劑。以碲鉛礦(主要成分為PbTe)和粗鹽(含CaCl2、MgCl2及一些硫酸鹽、泥沙)為原料制備碲化鈉的工藝流程如下:
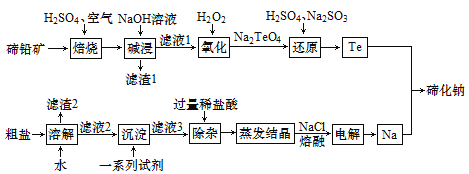
回答下列問題:
(1)Na2TeO4中Te的化合價為___。
(2)“沉淀”步驟中一系列試劑均過量,這些試劑依次包括_____(填化學式)和NaOH。
(3)“蒸發結晶”時用到的主要儀器有鐵架臺(帶鐵圈)、酒精燈、坩堝鉗、_____等。
(4)已知“焙燒”后,碲主要以TeO2形式存在,“焙燒”反應的化學方程式為____。
(5)依據“氧化”“還原”兩步反應可判知Na2TeO4、H2O2和Na2SO4氧化性由強到弱的順序為___;“還原”步驟中,還原劑與氧化劑的物質的量比為_______。
(6)若制得8.7kg碲化鈉,理論上電解產生標準狀況下氯氣的體積為______升。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com