
工業上可利用CO或CO2來生產燃料甲醇。已知甲醇制備的有關化學反應以及在不同溫度下的化學反應平衡常數如下表所示:
|
化學反應 |
平衡常數 |
溫度℃ |
||
|
500 |
700 |
800 |
||
|
①2H2(g)+CO(g) |
K1 |
2.5 |
0.34 |
0.15 |
|
②H2(g)+CO2(g) |
K2 |
1.0 |
1.70 |
2.52 |
|
③3H2(g)+CO2(g) |
K3 |
|
|
|
請回答下列問題:
(1)反應②是 (填“吸熱”或“放熱”)反應。
(2)據反應①與②可推導出K1、K2與K3之間的關系,則K3= (用K1、K2表示)。
(3)500℃時測得反應③在某時刻,H2(g)、CO2(g)、CH3OH(g)、H2O (g)的濃度(mol·L-1)分別為0.8、0.1、0.3、0.15,則此時 V正 V逆(填“ > ”、“=”或“<”)。
(4)反應①按照相同的物質的量投料,測得CO在不同溫度下的平衡轉化率與壓強的關系如下圖所示。下列說法正確的是_____________(填序號)。
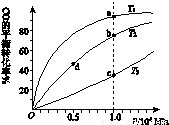
A.溫度:T1>T2>T3
B.正反應速率:υ(a)>υ(c) , υ(b)>υ(d)
C.平衡常數:K(a)>K(c) , K(b)=K(d)
D.平均摩爾質量:M(a)>M(c) , M(b)>M(d)
(1)吸熱(2分);(2)K3=K1•K2(2分);(3)>(2分);(4)CD(2分)。
【解析】
試題分析:(1)反應②,升高溫度,K值增大,正反應方向為吸熱方向。(2)反應①與②相加即可得到反應③,可推導出K3=K1•K2。(3)500℃時測得反應③在某時刻,H2(g)、CO2(g)、CH3OH(g)、H2O (g)的濃度(mol·L-1)分別為0.8、0.1、0.3、0.15,此時濃度商為Qc= =0.56<k=2.5,平衡將向正向移動,則此時 V正 >V逆。(4)A.該反應為放熱反應,溫度越低,CO的轉化率越大,則T1<T2<T3,故A錯誤;B.由圖可知,a、c兩點壓強相同,平衡時a點CO轉化率更高,該反應為放熱反應,溫度越低,CO的轉化率越大,故溫度T1<T3,溫度越高,反應速率越快,故υ(a)<υ(c).b、d兩點溫度相同,壓強越大,反應速率越大,b點大于d點壓強,則v(b)>v(d),故B錯誤;C.由圖可知,a、c兩點壓強相同,平衡時a點CO轉化率更高,該反應為放熱反應,故溫度T1<T3,降低溫度平衡向正反應方向移動,則K(a)>K(c),平衡常數只與溫度有關,b、d兩點溫度相同,平衡常數相同,則K(b)=K(d),故C正確;D.CO轉化率的越大,n總越小,由M=
=0.56<k=2.5,平衡將向正向移動,則此時 V正 >V逆。(4)A.該反應為放熱反應,溫度越低,CO的轉化率越大,則T1<T2<T3,故A錯誤;B.由圖可知,a、c兩點壓強相同,平衡時a點CO轉化率更高,該反應為放熱反應,溫度越低,CO的轉化率越大,故溫度T1<T3,溫度越高,反應速率越快,故υ(a)<υ(c).b、d兩點溫度相同,壓強越大,反應速率越大,b點大于d點壓強,則v(b)>v(d),故B錯誤;C.由圖可知,a、c兩點壓強相同,平衡時a點CO轉化率更高,該反應為放熱反應,故溫度T1<T3,降低溫度平衡向正反應方向移動,則K(a)>K(c),平衡常數只與溫度有關,b、d兩點溫度相同,平衡常數相同,則K(b)=K(d),故C正確;D.CO轉化率的越大,n總越小,由M= ,可知,a點n總小,則M(a)>M(c),M(b)>M(d),故D正確;故選CD.
,可知,a點n總小,則M(a)>M(c),M(b)>M(d),故D正確;故選CD.
考點:本題考查溫度、壓強、轉化率等之間的關系,明確外界條件對反應速率及平衡的影響是解本題的關鍵,易錯選項是D,注意根據M= 來分析解答即可.
來分析解答即可.


 舉一反三同步巧講精練系列答案
舉一反三同步巧講精練系列答案 口算與應用題卡系列答案
口算與應用題卡系列答案 名師點睛字詞句段篇系列答案
名師點睛字詞句段篇系列答案科目:高中化學 來源:2013-2014學年江西省紅色六校高三第二次聯考理綜化學試卷(解析版) 題型:填空題
甲醇是重要的化學工業基礎原料和清潔液體燃料。工業上可利用CO或CO2來生產燃料甲醇。已知甲醇制備的有關化學反應以及在不同溫度下的化學反應平衡常數如下表所示:

(1)反應②是?????? (填“吸熱”或“放熱”)反應。
(2)某溫度下反應①中H2的平衡轉化率(a)與體系總壓強(P)的關系,如圖所示。則平衡狀態由A變到B時,平衡常數K(A)????????? K(B)(填“>”、“<”或“=”)。據反應①與②可推導出K1、K2與K3之間的關系,則K3=?????? (用K1、K2表示)。

(3)在3 L容積可變的密閉容器中發生反應②,已知c(CO)與反應時間t變化曲線Ⅰ如圖所示,若在t0時刻分別改變一個條件,曲線Ⅰ變為曲線Ⅱ和曲線Ⅲ。

當曲線Ⅰ變為曲線Ⅱ時,改變的條件是??????????????? 。
當曲線Ⅰ變為曲線Ⅲ時,改變的條件是??????????????? 。
(4)甲醇燃料電池有著廣泛的用途,同時Al-AgO電池是應用廣泛的魚雷電? 池,其原理如圖所示。該電池的負極反應式是???????? 。

(5)一定條件下甲醇與一氧化碳反應可以合成乙酸。通常狀況下,將a mol/L的醋酸與b mol/LBa(OH)2溶液等體積混合,反應平衡時,2c(Ba2+)= c(CH3COO-),用含a和b的代數式表示該混合溶液中醋酸的電離常數為??????????????? 。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年天津市十二區縣重點校高三第一次模擬考試理綜化學試卷(解析版) 題型:填空題
甲醇是重要的化學工業基礎原料和液體燃料。工業上可利用CO或CO2來生產燃料甲醇。已知甲醇制備的有關化學反應以及在不同溫度下的化學反應平衡常數如下表所示:
化學反應 | 平衡常數 | 溫度(℃) | |
500 | 800 | ||
①2H2(g)+CO(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) | K2 | 1.0 | 2.50 |
③3H2(g)+ CO2(g) | K3 |
|
|
(1)反應②是?????? (填“吸熱”或“放熱”)反應。
(2)某溫度下反應①中H2的平衡轉化率(a)與體系總壓強(P)的關系如圖所示。則平衡狀態由A變到B時,平衡常數K(A)???????????? K(B)(填“>”、“<”或“=”)。
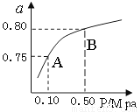
(3)判斷反應③△H?????? 0; △S?????? 0(填“>”“=”或“<”)據反應①與②可推導出K1、K2與K3之間的關系,則K3=?????????? (用K1、K2表示)。在500℃、2L的密閉容器中,進行反應③,測得某時刻H2、CO2、 CH3OH、H2O的物質的量分別為6mol、2 mol、10 mol、10 mol,此時v(正) ????? v(逆) (填“>”“=”或“<”)
(4)一定溫度下,在3 L容積可變的密閉容器中發生反應②,已知c(CO)與反應時間t變化曲線Ⅰ如圖所示,若在t0時刻分別改變一個條件,曲線Ⅰ變為曲線Ⅱ和曲線Ⅲ。
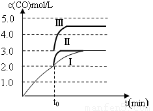
當曲線Ⅰ變為曲線Ⅱ時,改變的條件是??????????????????? 。
當曲線Ⅰ變為曲線Ⅲ時,改變的條件是?????????????????? 。
(5)甲醇燃料電池通常采用鉑電極,其工作原理如圖所示,負極的電極反應為:?????????????????????? 。
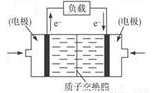
(6)一定條件下甲醇與一氧化碳反應可以合成乙酸。通常狀況下,將0.2 mol/L的醋酸與0.1 mol/LBa(OH)2溶液等體積混合,則混合溶液中離子濃度由大到小的順序為 ???????????????????????????????? 。
查看答案和解析>>
科目:高中化學 來源:2014屆云南省昆明市高三上學期第一次摸底調研測試化學試卷(解析版) 題型:填空題
甲醇是重要的化工原料和清潔液體燃料。工業上可利用CO或CO2來生產甲醇。甲醇制
備的相關信息如下表:

(1)反應②是____反應(選填“吸熱”“放熱”)。
(2)據上表信息推導出 、
、 與
與 之間的關系,
之間的關系, =______用
=______用 、
、 表示)。500℃時測得反應③在某時刻,
表示)。500℃時測得反應③在某時刻, 的濃度(mol/L)分別為0 8、0.1、0 3、0 15,此時
的濃度(mol/L)分別為0 8、0.1、0 3、0 15,此時 (選填“>”“<”“=”)。
(選填“>”“<”“=”)。
(3)若某溫度下反應①從開始到平衡CO和CH3OH的濃度變化如圖一所示,則用H2濃度變化表示此段時間內該反應的平均速.v(H2)=
若某溫度下反應①中H2的平衡轉化率(a)與體系總壓強(P)的關系如圖二所示,則平衡狀態由A變到B時,平衡常數 (選填“>”“<”“=”)。
(選填“>”“<”“=”)。

(4)一定溫度下,在體積固定的密閉容器中發生反應②,可判斷該反應已經達到平衡的是____。(用相應字母表示)
A.容器中總壓強不變
B.混臺氣體的平均摩爾質量也始終保持不變,
C.混合氣體的密度不變
D.CO2(g)或CO(g)的濃度不變
(5)一定條件下甲醇與一氧化碳反應可合成醋酸。室溫下,將a mol/L醋酸溶液與bmol/LNaOH溶液等體積混合。若溶液顯中性,則a_________b(選填“>”“<”“=”)。若c(Na+)<c(CH3COO-),則溶液顯____性(選填“酸”“堿…中”)。
查看答案和解析>>
科目:高中化學 來源:2014屆東北三省四市教研協作體高三聯合考試理綜化學試卷(解析版) 題型:填空題
甲醇是重要的化學工業基礎原料和清潔液體燃料。工業上可利用CO或CO2來生產燃料甲醇。已知甲醇制備的有關化學反應以及在不同溫度下的化學反應平衡常數如下表所示:
|
化學反應 |
平衡常數 |
溫度℃ |
|
|
500 |
800 |
||
|
①2H2(g)+CO(g) |
K1 |
2.5 |
0.15 |
|
②H2(g)+CO2(g) |
K2 |
1.0 |
2.50 |
|
③3H2(g)+CO2(g) |
K3 |
|
|
(1)反應②是 (填“吸熱”或“放熱”)反應。
(2)某溫度下反應①中H2的平衡轉化率(a)與體系總壓強(P)的關系,如圖所示。則平衡狀態由A變到B時,平衡常數K(A) K(B)(填“>”、“<”或“=”)。據反應①與②可推導出K1、K2與K3之間的關系,則K3= (用K1、K2表示)。

(3)在3 L容積可變的密閉容器中發生反應②,已知c(CO)與反應時間t變化曲線Ⅰ如圖所示,若在t0時刻分別改變一個條件,曲線Ⅰ變為曲線Ⅱ和曲線Ⅲ。

當曲線Ⅰ變為曲線Ⅱ時,改變的條件是 。
當曲線Ⅰ變為曲線Ⅲ時,改變的條件是 。
(4)甲醇燃料電池有著廣泛的用途,同時Al-AgO電池是應用廣泛的魚 雷電池,其原理如圖所示。該電池的負極反應式是

(5)一定條件下甲醇與一氧化碳反應可以合成乙酸。通常狀況下,將a mol/L的醋酸與b mol/LBa(OH)2溶液等體積混合,反應平衡時,2c(Ba2+)= c(CH3COO-),用含a和b的代數式表示該混合溶液中醋酸的電離常數為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com