
【題目】A、B、C、D四種離子化合物分別由Ba2+、NH4+、Na+、Mg2+中的一種和OH-、HSO4-、CO32-、Cl-中的一種組成。為確定其組成,某興趣小組做了以下實驗:
①配制濃度均為0.1mol/L的四種溶液,測其PH,其中B的PH大于13,C的PH大于7。
②將足量的B溶液與A溶液混合并微熱,生成了白色沉淀與刺激性氣味氣體。
據此請回答下列問題:
(1)D的化學式為____,A在水中的電離方程式為____;
(2)A與B按物質的量之比2:1在水溶液中進行反應的離子方程式為___;
(3)已知CH3COONH4溶液呈中性,如將等濃度、等體積的A溶液滴加到C溶液中,所得混合液呈____性(填“酸”、“堿”、“中”),各離子濃度由大到小的順序為____;
(4)將C和D的溶液分別蒸干并灼燒,所得固體分別是____。(填化學式)
(5)分別向含有0.15molB的溶液中加入100mL和200mL的A溶液并加熱收集生成的氣體,所得氣體在標準狀況下的體積均為VL,則V等于____,所加A溶液的物質的量濃度為____;
【答案】 MgCl2 NH4HSO4 = NH4++ H+ + SO42- SO42- + 2H+ + Ba2+ + 2OH- = BaSO4↓ + 2H2O 堿 c(Na+)>c(SO42-)>c(NH4+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-) Na2CO3、MgO 2.24 1 mol/L
【解析】①配制濃度均為0.1mol/L的四種溶液,測其PH,其中B的PH大于13,證明B為二元強堿Ba(OH)2,C的PH大于7,應該為碳酸鹽的水解所致;②將足量的B溶液與A溶液混合并微熱,生成了白色沉淀與刺激性氣味氣體,C為碳酸鹽,則A只能是NH4HSO4,與Ba(OH)2反應生成白色沉淀BaSO4和刺激性氣味氣體氨氣,故C為Na2CO3,最后確定D為MgCl2。(1)D的化學式為MgCl2;A為NH4HSO4,在水中的電離方程式為NH4HSO4 = NH4++ H+ + SO42-;(2)NH4HSO4與Ba(OH)2按物質的量之比2:1在水溶液中進行反應的離子方程式為:SO42- + 2H+ +Ba2+ + 2OH- = BaSO4↓ + 2H2O;(3)已知CH3COONH4溶液呈中性,如將等濃度、等體積的NH4HSO4溶液滴加到Na2CO3溶液中,發生反應的化學方程式為:2NH4HSO4+2Na2CO3= (NH4)2SO4+ Na2SO4+ 2NaHCO3,若不考慮水解,溶液中鹽電離的陰陽離子除鈉離子濃度最大以外,其他濃度相等;而(NH4)2SO4水解呈酸性,NaHCO3水解呈堿性,醋酸酸性強于碳酸,HCO3-的水解程度大于CH3COO-,CH3COONH4溶液呈中性,HCO3-的水解程度大于NH4+,所得混合液呈堿性,各離子濃度由大到小的順序為:c(Na+)>c(SO42-)>c(NH4+)>c(HCO3-)>c(OH-)>c(H+)>c(CO32-);(4)將Na2CO3溶液分別蒸干并灼燒,Na2CO3是多元弱酸鹽,水溶液里分步水解:Na2CO3+H2O = NaHCO3+NaOH、NaHCO3+H2O=H2CO3+NaOH,水解以第一步為主(第一步都是微弱的了,第一步還遠遠大于第二步,所以第二步水解基本忽略),加熱時,第一步水解產物NaHCO3和NaOH都不揮發,兩者濃度大了,又會相互反應生成Na2CO3,所以揮發的只是H2O,平衡向左移,最終得到Na2CO3;將MgCl2溶液分別蒸干并灼燒,MgCl2是強酸弱堿鹽,發生如下水解:MgCl2+H20![]() Mg(OH)2+HCl,HCl易揮發,加熱時揮發掉,使水解平衡向右移,MgCl2水解完全,得到Mg(OH)2(或者還有溶劑水,但繼續加熱會蒸發掉),Mg(OH)2在灼燒時分解:Mg(OH)2=MgO +H2O,水又揮發掉,則只剩MgO;(5)Ba(OH)2與NH4HSO4反應時,除硫酸鋇沉淀的生成外,離子反應為先OH-+H+=H2O,再OH-+ NH4+
Mg(OH)2+HCl,HCl易揮發,加熱時揮發掉,使水解平衡向右移,MgCl2水解完全,得到Mg(OH)2(或者還有溶劑水,但繼續加熱會蒸發掉),Mg(OH)2在灼燒時分解:Mg(OH)2=MgO +H2O,水又揮發掉,則只剩MgO;(5)Ba(OH)2與NH4HSO4反應時,除硫酸鋇沉淀的生成外,離子反應為先OH-+H+=H2O,再OH-+ NH4+![]() NH3↑,含有0.15mol Ba(OH)2的溶液中n(OH-)=0.3mol,NH4HSO4溶液中n(H+): n(NH4+)=1:1,分別向含有0.15mol Ba(OH)2的溶液中加入100mL和200mL的NH4HSO4溶液并加熱收集生成的氣體,所得氣體在標準狀況下的體積均為VL,則100mL NH4HSO4溶液反應時0.15mol Ba(OH)2的溶液過量,銨根離子全部轉化為氨氣
NH3↑,含有0.15mol Ba(OH)2的溶液中n(OH-)=0.3mol,NH4HSO4溶液中n(H+): n(NH4+)=1:1,分別向含有0.15mol Ba(OH)2的溶液中加入100mL和200mL的NH4HSO4溶液并加熱收集生成的氣體,所得氣體在標準狀況下的體積均為VL,則100mL NH4HSO4溶液反應時0.15mol Ba(OH)2的溶液過量,銨根離子全部轉化為氨氣![]() mol,
mol,
OH-+H+=H2O
![]()
![]()
OH-+ NH4+![]() NH3↑
NH3↑
![]()
![]()
![]()
200mL NH4HSO4溶液反應時NH4HSO4溶液過量,產生氨氣體積相等,故只有一半銨根離子參與反應:
OH-+H+=H2O
![]()
![]()
OH-+ NH4+![]() NH3↑
NH3↑
![]()
![]()
![]()
n(OH-)=![]() +
+![]() =
=![]() =0.3mol,V=2.24L,100mL NH4HSO4溶液中n(NH4+)= n(NH3)=
=0.3mol,V=2.24L,100mL NH4HSO4溶液中n(NH4+)= n(NH3)=![]() =0.1mol,c(NH4HSO4)=c(NH4+)=
=0.1mol,c(NH4HSO4)=c(NH4+)=![]() =1mol/L。
=1mol/L。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】在由水電離的c(H+)=10-14mol/L的溶液中,一定能大量共存的離子組是( )
A. K+、Fe2+、SO![]() 、MnO B. Na+、Cl-、NO、SO
、MnO B. Na+、Cl-、NO、SO![]()
C. Al3+、NH、Cl-、SO![]() D. Na+、AlO、Br-、Cl-
D. Na+、AlO、Br-、Cl-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)下列物質:①石墨 ②三氧化硫 ③液態氯化氫 ④氯氣 ⑤熔融的硫酸鉀 ⑥食鹽晶體 ⑦硫酸溶液 ⑧乙醇 ⑨冰醋酸 ⑩NH3·H2O,其中能夠導電的是 ,強電解質是 ,弱電解質是 ,非電解質是 。
(2)H2S溶于水的電離方程式為 。
①向H2S溶液中加入CuSO4溶液時,電離平衡向 移動,c(H+) ,c(S2-) 。
②向H2S溶液中加入NaOH固體時,電離平衡向 移動,c(H+) ,c(S2-) 。
③若將H2S溶液加熱至沸騰,c(H2S) 。
④若要增大H2S溶液中c(S2-),最好加入 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮化鋁(AlN)是一種新型無機非金屬材料。某AlN樣品僅含有Al2O3雜質,為測定AlN含量,設計如下兩種實驗方案。(已知:AlN+NaOH+ H2O==NaAlO2+ NH3↑)
【方案1】取一定量的樣品,用以下裝置測定樣品中AlN的純度(夾持裝置已略去)。
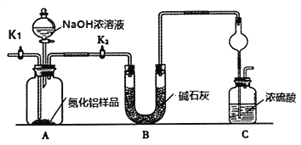
(1)上圖C裝置中球形干燥管的作用是_________________。
(2)完成以下實驗步驟:組裝好實驗裝置,檢查裝置氣密性并加入實驗藥品,關閉K1,打開K2 ,打開分液漏斗活塞,加入NaOH濃溶液,至不再產生氣體。打開K1,通入氮氣一段時間,測定C裝置反應前后的質量變化。
①檢驗裝置氣密性的方法是__________________________
②通入氮氣的目的是__________________________________________________。
(3)由于裝置存在缺陷,導致測定結果偏高,請提出改進意見__________________。
【方案2】用下圖裝置測定m g樣品中AlN的純度(部分夾持裝置已略去)。
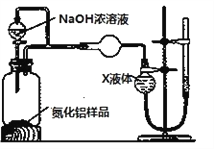
(4)為測定生成氣體的體積,量氣裝置中的X液體可以是___________
A.CCl4 B.H2O C.NH4Cl溶液 D.苯
(5)若m g樣品完全反應,測得生成氣體的體積為V mL(已轉換為標準狀況),則AlN的質量分數是_____________________。
若其他操作均正確,但反應結束后讀數時,右側量氣管中液面高于左側球型管中液面,則最后測得AlN的質量分數會_________(填“偏高”“偏低”或“無影響”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,向10 mL 1 mol/L HCl溶液中滴加等物質的量濃度的CH3COONa溶液。所得混合液的pH與加入CH3COONa溶液的體積(V)的變化如下圖所示。下列說法不正確的是

A. 常溫下,CH3COOH的電離常數約為2×10-5
B. 隨著V的增加,混合液中水的電離程度先增加后減小
C. 當V=20mL時,混合液中c(Na+) >c(CH3COO-)> c(Cl-)>c(H+) >c(OH-)
D. 當混合液的pH=7時,混合液中c(CH3COOH)=c(Cl-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向1L的密閉容器中加入1molX、3molZ和一定量的Y三種氣體。一定條件下發生反應,各物質的濃度隨時間變化如圖一所示。圖二為t2時刻后改變反應條件,平衡體系中反應速率隨時間變化的情況,且四個階段都各改變一種不同的條件。下列說法不正確的是

A. Y的起始物質的量為0.5mol
B. 該反應的化學方程式為:2X(g)+Y(g)![]() 3Z(g)ΔH<0
3Z(g)ΔH<0
C. 若t0=0,t1=10s,則t0-t1階段的平均反應速率為v(z)=0.03mol/(L﹒s)
D. 反應物X的轉化率t6點比t3點高
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗操作中錯誤的是( )
A. 分液時,分液漏斗下層液體從下口放出,上層液體從上口倒出
B. 稱量NaOH時,稱量物放在稱量紙上,置于托盤天平的左盤中
C. 過濾時,漏斗下端緊貼燒杯內壁
D. 蒸餾時,應使溫度計水銀球靠近蒸餾燒瓶支管口處
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應中,屬于加成反應的是( )
A.乙烯使酸性KMnO4溶液褪色
B.將苯滴入溴水中,振蕩后水層接近無色
C.乙烯使溴水褪色
D.甲烷與氯氣混合,光照一段時間后黃綠色變淺
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學習小組探究濃、稀硝酸氧化性的相對強弱,按下圖裝置進行試驗(夾持儀器已略去)。實驗表明濃硝酸能將NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的結論是濃硝酸的氧化性強于稀硝酸。
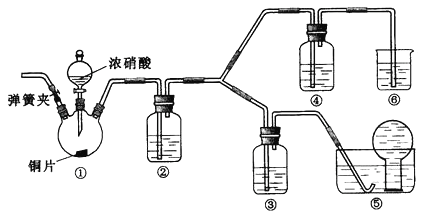
可選藥品:濃硝酸、3mol/L稀硝酸、蒸餾水、濃硫酸、氫氧化鈉溶液及二氧化碳
已知:氫氧化鈉溶液不與NO反應,能與NO2反應![]()
(1)實驗應避免有害氣體排放到空氣中,裝置③、④、⑥中盛放的藥品依次是_________
(2)滴加濃硝酸之前的操作是檢驗裝置的氣密性,加入藥品,打開彈簧夾后_________
(3)裝置①中發生反應的化學方程式是__________
(4)裝置②的作用是_________,發生反應的化學方程式是___________
(5)該小組得出的結論所依據的試驗現象是____________
(6)試驗結束后,同學們發現裝置①中溶液呈綠色,而不顯藍色。甲同學認為是該溶液中硝酸銅的質量分數較高所致,而乙同學認為是該溶液中溶解了生成的氣體。同學們分別設計了以下3個實驗來判斷兩種看法是否正確。這些方案中可行的是___(選填序號字母)
a.加熱該綠色溶液,觀察顏色變化
b.加水稀釋該綠色溶液,觀察顏色變化
c.向飽和硝酸銅溶液中通入濃硝酸與銅反應產生的氣體,觀察顏色變化
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com