
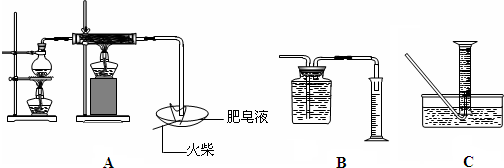
| 現象 | 結論與解釋 | |
| 可能① | ||
| 可能② |
分析 (1)爆鳴聲說明有氫氣生成,即可說明“鐵與水蒸氣”能夠進行反應;鐵在高溫下與水反應生成四氧化三鐵和氫氣,反應方程式為:3Fe+4H2O(g)$\frac{\underline{\;高溫\;}}{\;}$Fe3O4+4H2 ;
(2)①M收集裝置錯誤,導氣管位置錯誤,不可以測量生成氫氣的體積;
②根據鐵的質量求出生成氫氣的質量,根據氫氣的密度求出體積,以此選擇量筒的規格;
(3)反應后的固體中可能含有Fe和Fe3O4,溶于酸時可發生反應:Fe+2H+═Fe2++H2↑、Fe3O4+8H+═2Fe3++Fe2++4H2O、Fe+2Fe3+═3Fe2+,由于混合物中Fe的量不確定,可能有兩種情況:一是Fe較少,溶于酸后Fe3+有剩余,二是Fe較多,Fe3+完全被Fe還原為Fe2+,所以濾液中加KSCN溶液,可能變紅也可能溶液為淺綠色;
解答 解:(1)鐵與水蒸氣生成氫氣,反應一段時間后,有肥皂泡吹起時,用點燃的火柴靠近肥皂泡,不純的氫氣在點燃時會有爆鳴聲;鐵在高溫下與水反應生成四氧化三鐵和氫氣,反應方程式為:3Fe+4H2O(g)$\frac{\underline{\;高溫\;}}{\;}$Fe3O4+4H2
,故答案為:肥皂泡破裂,爆鳴聲; 3Fe+4H2O(g)$\frac{\underline{\;高溫\;}}{\;}$Fe3O4+4H2 ;
(2)①排水法收集氣體,量氣裝置的導氣管應短進長出,否則不能將水排到量筒中,無法測量氣體的體積,
故答案為:C;
②根據反應計算:
3Fe+4H2O(g)$\frac{\underline{\;高溫\;}}{\;}$Fe3O4+4H2
3×56g 8g
0.24g m(H2)
m(H2)=$\frac{0.24g×8g}{3×56g}$=0.0114g
V(H2)=$\frac{0.0114g}{0.088g/L}$=0.13L
選擇量筒時,應盡量減少誤差,所取量筒規格與量取體積接近,故應選擇規格為200ml的量筒,故答案為:B;
(3)為了證明反應后的固體混合物中含有+3價的Fe,取出少量混合物于試管中,加入足量的鹽酸,溶解,過濾.向濾液中滴加KSCN溶液,觀察溶液的顏色變化分析鐵離子的存在,鐵離子遇硫氰酸鉀溶液會變血紅色;鐵剩余會在溶液中和鐵離子反應生成亞鐵離子,依據溶液顏色分析離子存在,血紅色說明一定含三價鐵離子;淺綠色溶液可能是鐵和鐵離子反應生成亞鐵離子;
| 現象 | 結論與解釋 | |
| 可能① | 溶液變為紅色 | 反應后的固體混合物中含有+3價的Fe. 因為Fe3+遇到KSCN溶液時變成血紅色. |
可能② | 溶液仍然為淺綠色 | 反應后的固體混合物中可能含有+3價的Fe,也可能不含+3價的Fe;因為如果鐵粉有剩余,剩余鐵粉會與Fe3+反應,將溶液中Fe3+完全還原為Fe2+. |
| 現象 | 結論與解釋 | |
| 可能① | 溶液變為紅色 | 反應后的固體混合物中含有+3價的Fe. 因為Fe3+遇到KSCN溶液時變成血紅色. |
可能② | 溶液仍然為淺綠色 | 反應后的固體混合物中可能含有+3價的Fe,也可能不含+3價的Fe;因為如果鐵粉有剩余,剩余鐵粉會與Fe3+反應,將溶液中Fe3+完全還原為Fe2+. |
點評 本題考查鐵及其化合物的性質實驗,離子檢驗方法的應用,現象的分析判斷,題目難度不大,易錯點為量筒規格的選擇.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 相對平均分子質量增大 | B. | V正增大,V逆減小 | ||
| C. | A的轉化提高 | D. | 反應放出的總熱量大于原來的2倍 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| R | ||
| X | Y | Z |
| A. | X的氫化物比R的氫化物穩定 | |
| B. | 原子半徑大小順序是Z>Y>X>R | |
| C. | Z的單質能與Y的某些化合物發生置換反應 | |
| D. | X、Y、Z氫化物的穩定性:XH3>H2Y>HZ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 元素Y、Z、W具有相同電子層的離子,其半徑依次增大 | |
| B. | 元素X能與元素Y形成化合物X2Y2 | |
| C. | 元素Y、R分別與元素X形成的化合物的熱穩定性:XmY<XmR | |
| D. | 元素W、R的最高價氧化物的水化物都是強酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | HO(CH2)2CHO | B. | CH3COOH | C. | HOOCCOOH | D. | HO(CH2)2COOH |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com