

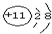 ,
,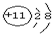 ;
; ,故答案為:
,故答案為: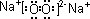 ;
; ,
,

科目:高中化學 來源: 題型:





查看答案和解析>>
科目:高中化學 來源: 題型:


| ||
| △ |
| ||
| △ |
查看答案和解析>>
科目:高中化學 來源:2012屆山西省山大附中高三第一次模擬試題理綜化學試卷(帶解析) 題型:填空題
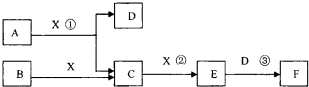
(14分)已知由短周期常見元素形成的純凈物A、B、C、D、E、F、X轉化關系如下圖所示,B、X為單質,D常溫下為無色液體,A、B含同一種元素。(某些產物可能略去)
請回答下列問題:
(1)若E是有色氣體,F是一元強酸,反應①是工業制備F的第一步反應。
①寫出A與X反應的化學方程式: 。
②有人認為“濃H2SO4可以干燥氣體E”。某同學為了驗證該觀點是否正確,用下圖裝置進行實驗。實驗過程中,濃H2SO4中未發現有氣體逸出,且濃H2SO4由無色變為紅棕色,由此你得出的結論是 。
③已知常溫下1 mol氣體E發生反應③放出46kJ熱量,寫出氣體E與H2O反應的熱化學方式 。
④在常溫下,向V1L pH=a的A溶液中加入V2L pH=b的鹽酸,且a+b=14,若反應后溶液的pH<7,則V1和V2的關系為V1 V2(填>、<、無法確定),所得溶液中各種離子的濃度由大到小的順序可能是 。(寫出一種情況即可)
(2)若E為無色無味氣體,F是二元弱酸。
①E的電子式為 ;
②將少量氣體E通入氫氧化鋇溶液中得不溶物G,G的KSP=8.1×10-9。現將該沉淀放入0.1mol/L的BaCl2溶液中,其KSP ,(填:增大、減小或不變),此時,組成不溶物G的陰離子在溶液中的濃度為 mol/L。
查看答案和解析>>
科目:高中化學 來源:2011-2012學年山西省高三第一次模擬試題理綜化學試卷(解析版) 題型:推斷題
(14分)已知由短周期常見元素形成的純凈物A、B、C、D、E、F、X轉化關系如下圖所示,B、X為單質,D常溫下為無色液體,A、B含同一種元素。(某些產物可能略去)
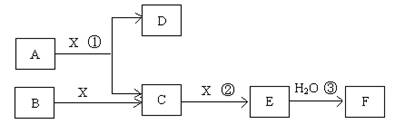
請回答下列問題:
(1)若E是有色氣體,F是一元強酸,反應①是工業制備F的第一步反應。
①寫出A與X反應的化學方程式: 。
②有人認為“濃H2SO4可以干燥氣體E”。某同學為了驗證該觀點是否正確,用下圖裝置進行實驗。實驗過程中,濃H2SO4中未發現有氣體逸出,且濃H2SO4由無色變為紅棕色,由此你得出的結論是 。
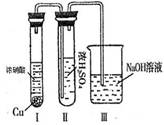
③已知常溫下1 mol氣體E發生反應③放出46kJ熱量,寫出氣體E與H2O反應的熱化學方式 。
④在常溫下,向V1L pH=a的A溶液中加入V2L pH=b的鹽酸,且a+b=14,若反應后溶液的pH<7,則V1和V2的關系為V1 V2(填>、<、無法確定),所得溶液中各種離子的濃度由大到小的順序可能是 。(寫出一種情況即可)
(2)若E為無色無味氣體,F是二元弱酸。
①E的電子式為 ;
②將少量氣體E通入氫氧化鋇溶液中得不溶物G,G的KSP=8.1×10-9。現將該沉淀放入0.1mol/L的BaCl2溶液中,其KSP ,(填:增大、減小或不變),此時,組成不溶物G的陰離子在溶液中的濃度為 mol/L。
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
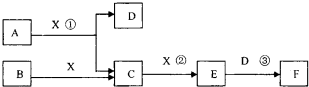
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com