
【題目】以乙炔和乙醛為原料制備1,3-丁二烯的合成路線如圖所示:下列說法不正確的是
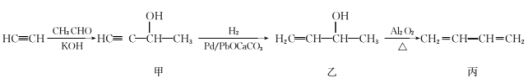
A.甲、乙兩種有機化合物中均含有手性碳原子
B.CH3CHO既可被氧化為CH3CH2OH,又可被還原為CH3COOH
C.丙(1,3-丁二烯)形成的高聚物的結構簡式為![]()
D.合成路線中涉及到的反應類型有加成反應和消去反應
 全優點練單元計劃系列答案
全優點練單元計劃系列答案科目:高中化學 來源: 題型:
【題目】(1)閱讀、分析下列兩個材料:
材料一
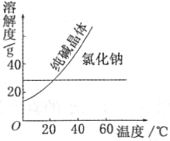
材料二
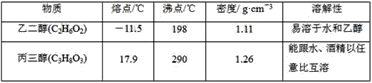
回答下列問題(填字母):
A.蒸餾法
B.萃取法
C.“溶解、結晶、過濾”的方法
D.分液法
①將純堿從氯化鈉和純堿的混合物中分離出來,最好應用___;
②將乙二醇和丙三醇相互分離的最佳方法是___。
(2)閱讀材料三回答下列問題:
材料三
在溶解性方面,Br2(溴)與I2(碘)很相似,其稀的水溶液顯黃色。在實驗室里從溴水(Br2的水溶液)中提取Br2和提取I2的方法相似。
①常用的提取方法是___,化學試劑是___,最主要的儀器是___。
②若觀察發現提取Br2以后的水還有顏色,解決該問題的方法是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國化工專家侯德榜的“侯氏制堿法”曾為世界制堿工業做出了突出貢獻。他利用NaHCO3、NaCl、NH4Cl等物質溶解度的差異,以食鹽、氨氣、二氧化碳等為原料先制得NaHCO3,進而生產出純堿。下面是在實驗室中模擬“侯氏制堿法”制取NaHCO3的實驗步驟:
第一步:連接好裝置,檢驗氣密性,在儀器內裝入藥品。
第二步:先讓一裝置發生反應,直到產生的氣體不能再在C中溶解時,再通入另一裝置中產生的氣體,片刻后,C中出現固體。繼續向C中通入兩種氣體,直到不再有固體產生。
第三步:過濾C中所得的混合物,得到NaHCO3固體。
第四步:向濾液中加入適量的NaCl粉末,有NH4Cl晶體析出。……
請回答下列問題(提示B分液漏斗中為濃氨水,滴入燒瓶可產生氨氣):
(1)裝置的連接順序是:(a)接________,________接________;(b)接________

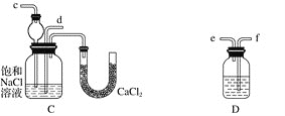
(2)A中常選用的固體反應物為______________;D中應選用的液體為________________(填化學式)。
(3)第二步驟中必須先讓__________裝置先發生反應。
(4)C中用球形干燥管而不用直導管,其作用是______________________________,C中廣口瓶內產生固體的總化學方程式為______________________ 。
(5)在第四步中分離NH4Cl晶體的操作是____________________(填操作名稱);其所得的NH4Cl晶體中常含有少量的NaCl和NaHCO3(約占5%~8%),請設計一個簡單的實驗證明所得固體的成分中含有Na+,簡要寫出操作和現象____________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知某可逆反應m A(g)+n B(g) ![]() p C(g)在密閉容器中進行,下圖表示在不同反應時間t時,溫度T和壓強p與反應物B在混合氣體中的體積分數B%的關系曲線,由曲線分析,下列判斷正確的是( )
p C(g)在密閉容器中進行,下圖表示在不同反應時間t時,溫度T和壓強p與反應物B在混合氣體中的體積分數B%的關系曲線,由曲線分析,下列判斷正確的是( )

A.T1<T2 p1>p2 m+n>p 放熱反應B.T1>T2 p1<p2 m+n>p 吸熱反應
C.T1<T2 p1>p2 m+n<p 放熱反應D.T1>T2 p1<p2 m+n<p 吸熱反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】應用下列實驗裝置或方案能達到實驗目的的是
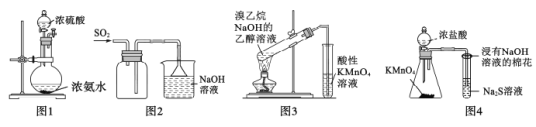
A.用圖1裝置制備少量氨氣
B.用圖2所示裝置收集SO2
C.用圖3所示裝置檢驗是否有乙烯產生
D.用圖4裝置比較KMnO4、C12、S的氧化性強弱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據下面的信息,下列敘述正確的是( )

A. 2 mol H2(g)跟 1 mol O2(g)反應生成 2 mol H2O(g)吸收能量為490 kJ
B. 化學反應中能量變化的大小與反應物的質量多少無關
C. 1 mol H2(g) 跟0.5mol O2(g) 反應生成 1 mol H2O(l)釋放能量為245 kJ
D. 2molH2O (g)的能量比2 mol H2(g)與1 mol O2(g)的能量之和低
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】酸堿中和滴定是中學化學常見實驗。
Ⅰ.下圖表示50mL酸式滴定管中液面的位置,如果液面處的讀數是a,則滴定管中剩余液體的體積是______mL。
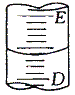
A、a B、大于a C、小于(50-a) D、大于(50-a)
Ⅱ.某同學欲測定某濃硫酸樣品的物質的量濃度,進行了以下實驗操作:
A 冷卻至室溫后,在100mL容量瓶中定容配成100mL稀硫酸。
B 量取20.00mL稀硫酸于錐形瓶中并滴入幾滴指示劑。
C 將酸式滴定管和堿式滴定管用蒸餾水洗滌干凈,并用各待盛溶液潤洗。
D 將物質的量濃度為1.50 mol·L-1的標準NaOH溶液裝入堿式滴定管,調節液面記下讀數V1。
E 繼續滴定至終點,記下讀數為V2。
F 在錐形瓶下墊一張白紙,把錐形瓶移到堿式滴定管下小心滴入NaOH標準溶液,邊滴邊搖動錐形瓶。
G 量取濃硫酸樣品5 mL,在燒杯中用蒸餾水溶解。
H 重復以上實驗。
請回答下列問題:
(1)該實驗正確操作步驟的順序為____→ A →_____→_____→D→_____→_____→ H(用編號字母填寫)。
(2)量取5mL濃硫酸的儀器是________________________;量取20.00mL稀硫酸的儀器是_________。
(3)選用的指示劑是_____________。滴定過程中,視線應注視____________________;判斷到達滴定終點的現象是________________;讀數時,視線應____________(填“高于”、“低于”或“相平于”)溶液凹液面的最低處。
(4)下表是實驗測得的有關數據:
滴定序號 | 待測稀硫酸的體積(mL) | 所消耗NaOH標準溶液液的體積(mL) | |
V1 | V2 | ||
① | 20.00 | 0.50 | 22.60 |
② | 20.00 | 6.00 | 27.90 |
請計算出該濃硫酸樣品的濃度為____________mol·L-1 (不必寫出計算過程)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】M、R均為主族元素,已知M的一個原子失去2個電子,R的一個原子得到1個電子后形成稀有氣體元素的電子層結構。下列關于M與R形成的化合物的敘述正確的是( )
A. M與R可以形成MR2型離子化合物
B. 在MR2中M的離子半徑比R的離子半徑大
C. 形成的兩種離子分別是M+和R2-
D. MR2的電子式為![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】雙羥基鋁碳酸鈉是醫療上常用的一種抑酸劑,其化學式是NaAl(OH)2CO![]() 。關于該物質的說法正確的是( )
。關于該物質的說法正確的是( )
A. 該物質屬于兩性氫氧化物
B. 該物質是Al(OH)3和Na2CO3的混合物
C. 1 mol NaAl(OH)2CO3最多可消耗3 mol H![]()
D. 該藥劑不適合于胃潰瘍患者服用
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com