(2011?奉賢區一模)苯甲醛在醫藥、染料、香料等工業有廣泛的應用.實驗室通過如圖所示的操作流程可制備苯甲醛:
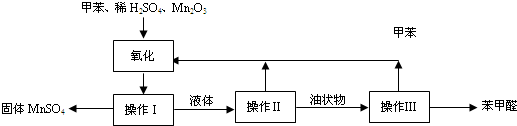
試回答下列問題:
(1)此反應中氧化劑是
Mn2O3
Mn2O3
,稀硫酸的作用是
形成酸性環境或增大Mn2O3的氧化性
形成酸性環境或增大Mn2O3的氧化性
.
(2)操作I需經三步才能完成:第一步為冷卻結晶,第二步為
過濾
過濾
,第三步為洗滌;其中冷卻的目的是
降低MnSO4的溶解度
降低MnSO4的溶解度
;第二步需用到的玻璃儀器為
漏斗、玻璃棒、燒杯
漏斗、玻璃棒、燒杯
.
(3)操作II的名稱為
分液
分液
,該操作主要適用于
分離兩種互不相溶的液體
分離兩種互不相溶的液體
.
(4)操作Ⅲ的原理是
利用被分離物質的沸點不同,通過加熱冷凝達到分離目的
利用被分離物質的沸點不同,通過加熱冷凝達到分離目的
.
(5)實驗過程中,可以循環使用的物質是
稀硫酸、甲苯
稀硫酸、甲苯
.
(6)實驗中發現,反應時間不同,苯甲醛的產率也不同(數據見表)
| 反應時間(h) |
1 |
2 |
3 |
4 |
5 |
| 苯甲醛產率(%) |
76.0 |
87.5 |
83.6 |
72.5 |
64.8 |
請結合苯甲醛的結構特點,分析當反應時間過長時,其產率下降的原因:
隨著時間的延長,苯甲醛有部分被氧化成苯甲酸
隨著時間的延長,苯甲醛有部分被氧化成苯甲酸
.




 桃李文化快樂暑假武漢出版社系列答案
桃李文化快樂暑假武漢出版社系列答案 優秀生快樂假期每一天全新寒假作業本系列答案
優秀生快樂假期每一天全新寒假作業本系列答案