
【題目】下列化合物中的所有原子可能都在同一平面上的是
A.CH3(CH2)4CH3B.CH3CH2CHO
C.CH2=CHCH=CH2D.(CH3)3C-C≡C-CH=CHCH3
 優百分課時互動系列答案
優百分課時互動系列答案科目:高中化學 來源: 題型:
【題目】根據下圖提供的信息,下列所得結論不正確的是
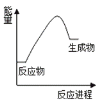
A. 該反應是吸熱反應
B. 因為生成物的總能量高于反應物的總能量,所以該反應一定需要加熱才能發生
C. 該反應反應物斷裂舊鍵所吸收的能量高于生成物形成新鍵放出的能量
D. 該反應可能是碳酸鈣分解反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)1 mol石墨轉變成金剛石需要吸收1.9 kJ的熱量該反應的熱化學方程式是__________。
(2)在25℃、101kPa下,一定質量的無水乙醇完全燃燒時放出熱量QkJ,其燃燒生成的CO2用過量飽和石灰水吸收可得100gCaCO3沉淀,則乙醇燃燒的熱化學方程式為_________。
(3)已知下列熱化學方程式
Fe2O3(s)+3CO(g)===2Fe(s)+3CO2(g) ΔH1=-25 kJ·mol-1 ①
3Fe2O3(s)+CO(g)===2Fe3O4(s)+CO2(g) ΔH2=-47 kJ·mol-1 ②
Fe3O4(s)+CO(g)===3FeO(s)+CO2(g) ΔH3=+19 kJ·mol-1 ③
寫出FeO(s)被CO還原成Fe和CO2的熱化學方程式_________________。
(4)向足量H2SO4溶液中加入100 mL 0.4 mol·L-1Ba(OH)2溶液,放出的熱量是5.12 kJ。如果向足量Ba(OH)2溶液中加入100 mL 0.4 mol·L-1鹽酸時,放出的熱量為2.2 kJ。則Na2SO4溶液與BaCl2溶液反應的熱化學方程式為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以硫鐵礦(FeS2的質量分數為60%)為原料制備氯化鐵晶體(FeCl3·6H2O,270.5g·moˉ1)的工藝流程如圖所示。

請回答下列問題:
(1)為加快焙燒反應的化學反應速率,可采取的措施為_____、_____。(任寫兩條)
(2)焙燒后得到的Fe2O3在酸溶過程中發生反應的離子方程式為________。
(3)過濾操作用到的玻璃儀器有燒杯、_______、______。
(4)焙燒過程中產生的SO2可用過量的氨水進行吸收,所得溶液中溶質的名稱為_______。
(5)先向氯化鐵溶液中加適量鹽酸的目的是______,再______、______、過濾、洗滌,最終得到氯化鐵晶體。
(6)若取1kg硫鐵礦經過上述流程(鐵元素在整個流程中損失率為4%),則可得氯化鐵晶體的質量為_______(保留一位小數)kg。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國科學家成功實現甲烷在催化劑及無氧條件下,一步高效生產乙烯、芳烴和氫氣等化學品,為天然氣化工開發了一條革命性技術。以甲烷為原料合成部分化工產品流程如下(部分反應條件已略去):

(1)E 的名稱為____,B物質的結構簡式:______;
(2)上述③~⑥轉化反應中,屬于取代反應的有______(用反應序號填寫);
(3)寫出反應⑦的反應方程式:______;
(4)如圖為實驗室制取E的裝置圖,圖中a試劑為_______;

(5)某同學在試管b中加入6.0克乙酸和足量乙醇采用適當條件使反應充分進行,結束后在試管b回收到3.0克乙酸,則該同學在本次實驗中制得乙酸乙酯的最大質量為_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究NO2、NO、CO等污染物的處理對建設美麗中國具有重要意義。
(1)利用甲烷催化還原NOx:
CH4(g)+4NO2(g) ===4NO(g)+CO2(g)+2H2O(g) ΔH1=-574 kJ·mol-1
CH4(g)+4NO(g) ===2N2(g)+CO2(g)+2H2O(g) ΔH2=-1160 kJ·mol-1
①甲烷直接將NO2還原為N2的熱化學方程式為________________________________。
②將CH4和NO2充入密閉容器中發生上述反應,該反應達到平衡后,為了提高反應速率的同時提高NO2的轉化率,可采取的措施有__________(寫一點即可)。
③利用原電池反應可實現NO2的無害化,總反應為6NO2+8NH3===7N2+12H2O,電解質溶液為NaOH溶液,工作一段時間后,該電池正極區附近溶液pH________(填“增大”、“減小”或“不變”),負極的電極反應式為___________________。
(2)光氣(COCl2)在塑料、制革、制藥等工業中有許多用途。工業上常利用廢氣CO2通過反應:C(s)+CO2(g)![]() 2CO(g) ΔH>0,制取合成光氣的原料氣CO。在體積可變的恒壓(p總)密閉容器中充入1mol CO2 與足量的碳發生上述反應,在平衡時體系中氣體體積分數與溫度的關系如圖所示:
2CO(g) ΔH>0,制取合成光氣的原料氣CO。在體積可變的恒壓(p總)密閉容器中充入1mol CO2 與足量的碳發生上述反應,在平衡時體系中氣體體積分數與溫度的關系如圖所示:
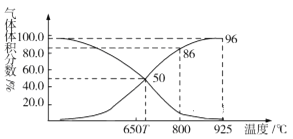
①T℃時,在容器中若充入稀有氣體,平衡______移動(填“正向”“逆向”或“不”,下同);若充入等體積的CO2和CO,平衡________移動。
②CO體積分數為40%時,CO2的轉化率為_______。
③已知:氣體分壓(p分)=氣體總壓×體積分數。800℃時用平衡分壓代替平衡濃度表示平衡常數Kp=______(用含p總的代數式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】Cr、Fe、Ni單質及化合物有重要的用途。
(1)用Cr2O3作原料,鋁粉作還原劑的鋁熱法是生產金屬鉻的主要方法之一,該反應是一個自發放熱反應,由此可判斷Cr—O鍵和Al—O鍵中____________鍵更強。研究發現氣態氯化鋁(Al2Cl6)是具有配位鍵的化合物,可溶于非極性溶劑,由此可知該分子是______(填“極性”或“非極性”)的。
(2)鐵有α、γ、δ三種晶體構型,其中α-Fe單質為體心立方晶體,δ-Fe單質為簡單立方晶體。則這兩種晶體結構中鐵原子的配位數之比是______。
(3)FeS2晶體的晶胞如下圖所示。晶胞邊長為a nm、FeS2相對式量為M,阿伏加德羅常數的值為NA,其晶體密度的計算表達式為___________g·cm3;晶胞中Fe2+位于S22—所形成的正八面體的體心,該正八面體的邊長為______nm。

(4)硫酸鎳溶于氨水形成[Ni(NH3)6]SO4藍色溶液。
①[Ni(NH3)6]SO4中陰離子的立體構型是__________。
②在[Ni(NH3)6]2+中Ni2+與NH3之間形成的化學鍵稱為__________,提供孤電子對的成鍵原子是___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學反應過程中發生物質變化的同時,常常伴有能量的變化.這種能量的變化常以熱量的形式表現出來,叫做反應熱.由于反應的情況不同,反應熱可以分為許多種,如燃燒熱和中和熱等。
(1)下列△H表示物質燃燒熱的是 ______ ;表示物質中和熱的是 ______ (填“△H1”、“△H2”、“△H3”等).
A.2H2(g)+O2(g)═2H2O(l)△H1
B.C(s)+1/2O2(g)═CO(g)△H2
C.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H3
D.C(s)+O2(g)═CO2(g)△H4
E.C6H12O6(s)+6O2(g)═6CO2(g)+6H2O(l)△H5
F.NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H6
G.2NaOH(aq)+H2SO4(aq)═Na2SO4(aq)+2H2O(l)△H7
H.CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H8
(2)依據事實,寫出下列反應的熱化學方程式.
Ⅰ、在25℃、101kPa下,1gCH3OH燃燒生成CO2和液態水時放熱22.68kJ.則表示甲醇燃燒熱的熱化學方程式為 _______________________;
Ⅱ、1.00L1.00mol/LH2SO4溶液與2.00L1.00mol/LNaOH溶液完全反應,放出114.6kJ的熱量,表示其中和熱的熱化學方程式為 ________________________;
Ⅲ、已知拆開1molH-H鍵,1molN-H鍵,1molN≡N鍵分別需要的能量是436kJ、391kJ、 946kJ,則N2與H2反應生成NH3的熱化學方程式為 _______________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com