
【題目】阿伏加德羅常數的值為NA,下列說法正確的是
A. 標準狀況下,2.24LCH3OH分子中共價鍵的數目為0.5NA
B. 1 L1 mol·L-1HCl溶液中含有NA個HCl分子
C. 12.0 g熔融的NaHSO4中含有的陽離子數為0.1NA
D. 1mol SO2與足量O2在一定條件下充分反應生成SO3,共轉移2 NA個電子
科目:高中化學 來源: 題型:
【題目】某同學用如圖所示裝置探究原電池的工作原理,并推出下列結論,其中不正確的是( )
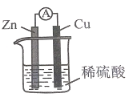
A.鋅片不斷溶解,說明Zn失去電子
B.銅片上產生氣泡,說明溶液中H+在其表面得到電子
C.電流計指針發生偏轉,說明該裝置將電能轉換為化學能
D.該裝置中發生的總反應為Zn+H2SO4=ZnSO4+H2↑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據信息回答下列問題:
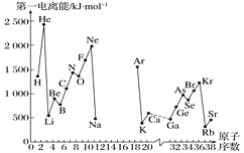
A.第一電離能I1是指氣態原子X(g)處于基態時,失去一個電子成為氣態陽離子X+(g)所需的最低能量。下圖是部分元素原子的第一電離能I1隨原子序數變化的曲線圖(其中12號至17號元素的有關數據缺失)。
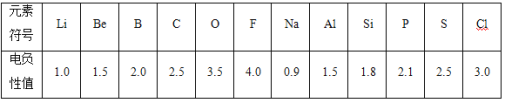
B.不同元素的原子在分子內吸引電子的能力大小可用數值表示,該數值稱為電負性。一般認為:如果兩個成鍵原子間的電負性差值大于1.7,原子之間通常形成離子鍵;如果兩個成鍵原子間的電負性差值小于1.7,通常形成共價鍵。下表是某些元素的電負性值:
(1)認真分析信息A圖中同周期元素第一電離能的變化規律,推斷第三周期Na~Ar這幾種元素中,Al的第一電離能的大小范圍為______<Al<________(填元素符號)。
(2)從信息A圖中分析可知,同一主族元素原子的第一電離能I1的變化規律是______________:
(3)信息A圖中第一電離能最小的元素在周期表中的位置是_______周期__________族。
(4)根據對角線規則,Be、Al元素最高價氧化物對應水化物的性質相似,它們都具有_______性,其中Be(OH)2顯示這種性質的離子方程式是____________。
(5)通過分析電負性值的變化規律,確定Mg元素的電負性值的最小范圍_________。
(6)請歸納元素的電負性和金屬性、非金屬性的關系是__________。
(7)從電負性角度,判斷AlCl3是離子化合物還是共價化合物___________,說出理由并寫出判斷的方法_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是
A. 24 g 鎂與27 g鋁中,含有相同的質子數
B. 同等質量的氧氣和臭氧中,電子數相同
C. 1 mol重水與1 mol水中,中子數比為2∶1
D. 1 mol乙烷和1 mol乙烯中,化學鍵數相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下面列出了幾組物質,請將物質的合適組號填寫在空格上。
①金剛石與“足球烯”、C60;②氧氣(O2)與臭氧(O3);③16O、17O和18O;④CH4和CH3CH2CH3;
⑤乙烯和乙烷;⑥![]() 和
和![]() ;⑦
;⑦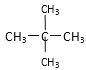 和
和![]() ;
;
(1)同位素___,
(2)同系物___,
(3)同分異構體___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,將pH均為2 的HCl與HX 的溶液分別加水稀釋,溶液pH隨溶液體積變化的曲線如圖所示。下列說法不正確的是
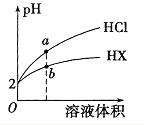
A. a、b兩點: c(X-) < c(Cl-) B. 溶液的導電性: a < b
C. 稀釋前,c(HX) > 0.01mol/L D. 溶液體積稀釋到10倍,HX 溶液的pH < 3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)對于反應:2NO(g)+O2(g)![]() 2NO2(g),在其他條件相同時,分別測得NO的平衡轉化率在不同壓強(p1、p2)下溫度變化的曲線如圖:
2NO2(g),在其他條件相同時,分別測得NO的平衡轉化率在不同壓強(p1、p2)下溫度變化的曲線如圖:


①比較p1、p2的大小關系:________。
②隨溫度升高,該反應平衡常數變化的趨勢是________(“增大”或“減小”)。
(2)在容積為1.00L的容器中,通入一定量的N2O4,發生反應N2O4(g)![]() 2NO2(g),隨溫度升高,混合氣體的顏色變深。回答下列問題:
2NO2(g),隨溫度升高,混合氣體的顏色變深。回答下列問題:
①反應的ΔH______0(填“大于”或“小于”);100℃時,體系中各物質濃度隨時間變化如上圖所示。在0~60s時段,反應速率v(N2O4)為__________________;平衡時混合氣體中NO2的體積分數為_______。
②100℃時達平衡后,向容器中迅速充入含0.08mol的NO2和0.08mol N2O4 的混合氣體,此時速率關系v(正)____v(逆)。(填“大于”,“等于”,或“小于”)
③100℃時達平衡后,改變反應溫度為T,c(N2O4)以0.0020mol·L-1·s-1的平均速率降低,經10s又達到平衡。
a.T________100℃(填“大于”或“小于”),判斷理由是____________________
b.列式計算溫度T時反應的平衡常數K2(寫計算過程):______
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,在恒容密閉容器中發生反應X(g)+2Y(g) ![]() 2Z(g)。下列敘述能判斷該反應達到化學平衡的是
2Z(g)。下列敘述能判斷該反應達到化學平衡的是
① X、Y、Z的物質的量之比是1∶2∶2 ② X、Y、Z的濃度不再發生變化③ 容器中的壓強不再發生變化 ④ 單位時間內生成n mol Z,同時消耗n mol Y
A. ①② B. ①④ C. ②③ D. ③④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關說法正確的是
A. 已知HI(g) ![]() 1/2H2(g)+1/2I2(s) ΔH=-26.5 kJ·mol-1,由此可知1 mol HI氣體在密閉容器中充分分解后可以放出26.5 kJ的熱量
1/2H2(g)+1/2I2(s) ΔH=-26.5 kJ·mol-1,由此可知1 mol HI氣體在密閉容器中充分分解后可以放出26.5 kJ的熱量
B. 已知2H2(g)+O2(g)===2H2O(g) ΔH=-571.6 kJ·mol-1,則氫氣的燃燒熱為ΔH=-285.8 kJ·mol-1
C. 已知2C(s)+2O2(g)=2CO2(g) ΔH1, 2C(s)+O2(g)=2CO(g) ΔH2,則ΔH1<ΔH2
D. 含20.0 g NaOH的稀溶液與稀鹽酸完全中和,放出28.7 kJ的熱量,則稀醋酸和稀NaOH溶液反應的熱化學方程式為:NaOH(aq)+CH3COOH(aq)===CH3COONa(aq)+H2O(l) ΔH=-57.4 kJ·mol-1
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com