
| A. | 甲烷的標準燃燒熱為-890.3kJ•mol-1,則甲烷燃燒的熱化學方程式可表示為:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| B. | 500℃、30MPa下,將0.5mol N2和1.5molH2置于密閉的容器中充分反應生成NH3(g),放熱19.3kJ 其熱化學方程式為:N2(g)+3H2(g)$?_{500℃/30MPa}^{催化劑}$2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | HCl和NaOH反應的中和熱△H=-57.3kJ/mol,則1mol稀H2SO4和足量KOH反應的反應熱為△H=2×(-57.3)kJ/mol | |
| D. | 同溫同壓下H2(g)+Cl2(g)=2HCl(g),在光照和點燃條件的△H不同 |
分析 A.燃燒熱是1mol可燃物完全燃燒生成穩定氧化物放出的熱量,液態水比氣態水穩定;
B.合成氨的反應為可逆反應,反應消耗氮氣的物質的量一定小于0.5mol;
C.熱化學方程式中,焓變與化學計量數成正比;
D.反應熱與反應條件無關,與反應物、生成物的始態和終態有關.
解答 解:A.1mol可燃物完全燃燒生成穩定的氧化物,所放出的熱量為燃燒熱,水的狀態應該為液態,正確的熱化學方程式為:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ•mol-1,故A錯誤;
B.500℃30MPa下,將0.5mol N2和1.5molH2置于密閉的容器中充分反應生成NH3(g),放熱19.3kJ,由于該反應為可逆反應,則消耗的氮氣的物質的量小于0.5mol,即0.5mol氮氣完全轉化成氨氣放出的熱量大于19.3kJ,則1mol氮氣完全反應放出熱量大于38.6kJ,正確的熱化學方程式為:N2(g)+3H2(g)$?_{500℃/30MPa}^{催化劑}$2NH3(g)△H<-38.6kJ•mol-1,故B錯誤;
C.HCl和NaOH反應的中和熱△H=-57.3kJ/mol,由于1mol稀H2SO4和足量KOH反應生成2mol水,則該反應的反應熱△H=2×(-57.3)kJ/mol,故C正確;
D.同溫同壓下的反應H2(g)+Cl2(g)=2HCl(g),根據蓋斯定律可知,在光照和點燃條件的△H相同,故D錯誤;
故選C.
點評 本題考查了反應熱與焓變的應用,題目難度中等,明確燃燒熱概念為解答關鍵,注意掌握熱化學方程式的書寫原則及表示意義,試題有利于提高學生的分析能力及靈活應用能力.


科目:高中化學 來源: 題型:解答題
| 物質 n/mol T/℃ | 活性炭 | NO | E | F |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ②③ | C. | ①④ | D. | ②④ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
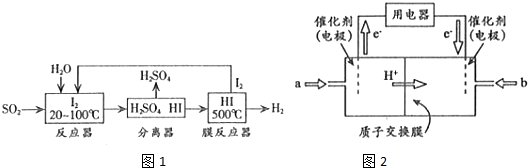
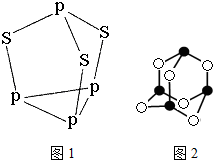 磷和砷元素形成的化合物在生活和生產中有重要的用途,回答下列問題.
磷和砷元素形成的化合物在生活和生產中有重要的用途,回答下列問題.查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
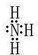 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 在75℃左右,用HgSO4做催化劑,乙炔可水化為乙醛,但HgSO4遇到某些特定物質常會發生催化劑中毒而失去催化作用,H2S就是其中一種:現用乙炔水化法,只用塊狀電石、濃硫酸、水、NaOH溶液、HgO粉末五種物質制乙醛,裝置如圖所示,請回答下列問題;
在75℃左右,用HgSO4做催化劑,乙炔可水化為乙醛,但HgSO4遇到某些特定物質常會發生催化劑中毒而失去催化作用,H2S就是其中一種:現用乙炔水化法,只用塊狀電石、濃硫酸、水、NaOH溶液、HgO粉末五種物質制乙醛,裝置如圖所示,請回答下列問題;查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
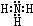 ,B的結構式為
,B的結構式為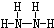 .
.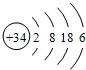 .
.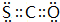 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com