
| A. | 標準狀況下1.12L Cl2中含有的質子總數為0.85NA | |
| B. | 0.12 mol•L-1 AlCl3溶液含有0.36NA個Cl- | |
| C. | 常溫常壓下,9g H2O中所含原子總數為1.5NA | |
| D. | O2與O3的混合物32g,含有分子總數為NA |
分析 A、求出氯氣的物質的量,然后根據氯氣中含34個質子來分析;
B、溶液體積不明確;
C、求出水的物質的量,然后根據水為三原子分子來分析;
D、氧氣和臭氧的摩爾質量不同.
解答 解:A、標況下1.12L氯氣的物質的量為0.05mol,而氯氣中含34個質子,故0.05mol氯氣中含0.17NA個質子,故A錯誤;
B、溶液體積不明確,故溶液中的氯離子的個數無法計算,故B錯誤;
C、9g水的物質的量為0.5mol,而水為三原子分子,故0.5mol水中含1.5NA個,故C正確;
D、氧氣和臭氧的摩爾質量不同,故32g氧氣和臭氧的混合物的物質的量無法計算,故分子個數無法計算,故D錯誤.
故選C.
點評 本題考查了阿伏伽德羅常數的有關計算,難度不大,應注意公式的運用和物質的結構特點.


 全能測控一本好卷系列答案
全能測控一本好卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 任何分子或化合物都是通過原子間形成化學鍵相結合的 | |
| B. | 物質發生化學反應時,斷開反應物中的化學鍵要吸收能量,而形成生成物中的化學鍵要放出能量 | |
| C. | 化學鍵的斷裂和形成是化學反應中能量變化的主要原因 | |
| D. | 分子的穩定性與化學鍵強弱有關 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 、
、 、
、 ;屬于芳香醚類的是C6H5OCH3.
;屬于芳香醚類的是C6H5OCH3. 、
、 或
或 (寫兩種);
(寫兩種);查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溶液的pH等于13 | |
| B. | 加入少量NH4Cl固體,c(OH-)不變 | |
| C. | c(OH-)=c(NH4+)+c(H+) | |
| D. | 與1.0 mL 0.l mol/L鹽酸混合后,溶液呈中性 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 含14g硅原子的二氧化硅晶體中含有的硅氧鍵數目為2NA | |
| B. | 3.9g Na2O2晶體中含有0.2NA個離子 | |
| C. | 常溫常壓下,5g D2O含有的質子數、電子數、中子數均為2.5NA | |
| D. | 3mol H2和1mol N2在一定條件下反應所得混合氣體分子數小于2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
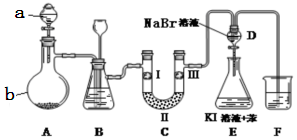
| 實驗現象 | 原因 |
| 溶液最初從紫色逐漸變為紅色 | 氯氣與水反應生成的H+使石蕊變色 |
| 隨后溶液逐漸變為無色 | 氯氣與水反應生成HClO具有漂白性 |
| 然后溶液從無色逐漸變為淺黃綠色 | 過量氯氣溶解于水中 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 當a=1時,發生的離子反應為:OH-+H+═H2O | |
| B. | 當a=2時,發生的離子反應為:OH-+CO32-+2H+═HCO3-+H2O | |
| C. | 當1<a<2,反應后的溶液中CO32-和HCO3-的物質的量之比為:(a×10-2-0.01):(0.02-a×10-2) | |
| D. | 當a≥3時,發生的離子反應:3H++OHˉ+CO32-═2H2O+CO2↑ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com