
(12分)有右圖裝置:回答下列問題:
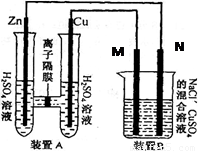
(1)裝置A是_______池,B是_______池。
(2)裝置A中的Zn極是_______極,
Cu極上的電極反應方程式為:__________________。
(3)裝置B中是濃度均為1.0mol/L的NaCl、CuSO 混合溶液,溶液體積為500mL,M、N均為石墨電極,當裝置A中Zn棒質量減少32.5g時,N上質量增加____________g;
混合溶液,溶液體積為500mL,M、N均為石墨電極,當裝置A中Zn棒質量減少32.5g時,N上質量增加____________g;
(4)欲用裝置B給用來給餐具鍍銀,N應該是 (填“銀” 或“餐具”), 電鍍液的主要成分是(填化學式) 。
((1)小題每格1分,其余2分)(1)原電池; 電解池;
(2)負;Cu極上的電極反應式 ;H2-2e-=H2↑;
(3) 32 g; (4)餐具; AgNO 3 ;
【解析】(1)根據裝置圖中電解材料的性質及電解質溶液可知,A是銅鋅原電池,B是電解池。
(2)原電池中較活潑的金屬作負極,所以鋅是負極,銅是正極,溶液中的氫離子在正極得到電子生成氫氣,反應式為H2-2e-=H2↑。
(3)A中Zn棒質量減少32.5g時,轉移電子是32.5g÷65g/mol×2=1.0mol。N和電源的負極相連,是陰極,溶液中的銅離子放電。溶液中銅離子的物質的量是1mol/L×0.5L=0.5mol,恰好需要1mol電子,生成0.5mol銅,質量是32g。
(4)電鍍時待鍍金屬作陰極,鍍層金屬作陽極,含有鍍層金屬離子的溶液作電鍍液,N是陰極,連接餐具,可以用硝酸銀作電鍍液。


 口算能手系列答案
口算能手系列答案科目:高中化學 來源:2011學年浙江省瑞安十校高二第二學期期中聯考化學試卷(帶解析) 題型:填空題
(12分)有右圖裝置:回答下列問題:
(1)裝置A是_______池,B是_______池。
(2)裝置A中的Zn極是_______極,
Cu極上的電極反應方程式為:__________________。
(3)裝置B中是濃度均為1.0mol/L的NaCl、CuSO 混合溶液,溶液體積為500mL,M、N均為石墨電極,當裝置A中Zn棒質量減少32.5g時,N上質量增加____________g;
混合溶液,溶液體積為500mL,M、N均為石墨電極,當裝置A中Zn棒質量減少32.5g時,N上質量增加____________g;
(4)欲用裝置B給用來給餐具鍍銀,N應該是 (填“銀” 或“餐具”), 電鍍液的主要成分是(填化學式) 。
查看答案和解析>>
科目:高中化學 來源:2012-2013學年江蘇省宿遷市泗洪縣洪翔中學高二下學期期中考化學卷(帶解析) 題型:填空題
(1)有一部分化學反應的反應熱測定起來很困難,我們可以根據蓋斯定律計算獲得。如同素異形體之間的轉化反應熱數值小且轉化慢,測定較困難。已知:
①4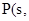 白磷
白磷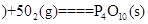 △H=-2983.2KJ/mol
△H=-2983.2KJ/mol
②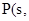 紅磷
紅磷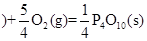 △H=-738.5KJ/mol
△H=-738.5KJ/mol
寫出白磷轉化為紅磷的熱化學方程式:__________________________。則對應下列化學反應過程中的能量變化圖,能正確反映出由白磷轉化為紅磷的是_______。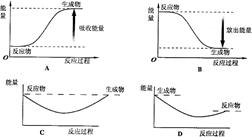
(2)(6分)有右圖裝置:回答下列問題: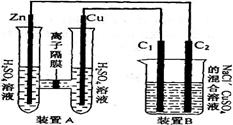
①裝置A是_______池,B是_______池。
②裝置A中的Zn極是_______極,Cu極上的電極反應方程式為:___。
③鋅與鐵組成的合金在潮濕的空氣中,鋅被腐蝕而另一種金屬被保護,這種保護方法稱為
查看答案和解析>>
科目:高中化學 來源:2014屆江蘇省宿遷市高二下學期期中考化學卷(解析版) 題型:填空題
(1)有一部分化學反應的反應熱測定起來很困難,我們可以根據蓋斯定律計算獲得。如同素異形體之間的轉化反應熱數值小且轉化慢,測定較困難。已知:
①4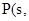 白磷
白磷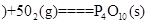 △H=-2983.2KJ/mol
△H=-2983.2KJ/mol
②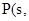 紅磷
紅磷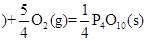 △H=-738.5KJ/mol
△H=-738.5KJ/mol
寫出白磷轉化為紅磷的熱化學方程式:__________________________。則對應下列化學反應過程中的能量變化圖,能正確反映出由白磷轉化為紅磷的是_______。

(2)(6分)有右圖裝置:回答下列問題:
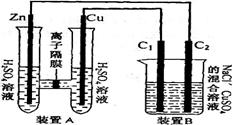
①裝置A是_______池,B是_______池。
②裝置A中的Zn極是_______極,Cu極上的電極反應方程式為:___。
③鋅與鐵組成的合金在潮濕的空氣中,鋅被腐蝕而另一種金屬被保護,這種保護方法稱為
查看答案和解析>>
科目:高中化學 來源: 題型:
(12分)(1)(4分)有一部分化學反應的反應熱測定起來很困難,我們可以根據蓋斯定律計算獲得。如同素異形體之間的轉化反應熱數值小且轉化慢,測定較困難。已知:
①![]() 白磷
白磷![]()
![]()
②![]() 紅磷
紅磷![]()
![]()
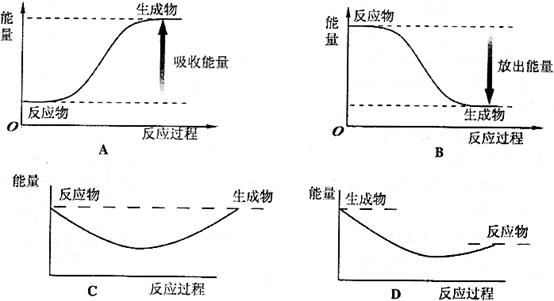
寫出白磷轉化為紅磷的熱化學方程式:__________________________。則對應下
列化學反應過程中的能量變化圖,能正確反映出由白磷轉化為紅磷的是_____________。

(2)(8分)有右圖裝置:回答下列問題:
①裝置A是_______池,B是_______池。
②裝置A中的Zn極是_______極,Cu極上
的電極反應方程式為:__________________。
③鋅與鐵組成的合金在潮濕的空氣中,
鋅被腐蝕而另一種金屬被保護,這種保護方法叫
做_______,正極反應式為__________________ 。
![]() ④裝置B中是濃度均為
④裝置B中是濃度均為![]() 的NaCl、CuSO
的NaCl、CuSO![]() 混合溶液,溶液體積為500mL。當裝置A中Zn棒質量減少32.5g時,C
混合溶液,溶液體積為500mL。當裝置A中Zn棒質量減少32.5g時,C![]() 上質量增加____________g;
上質量增加____________g;
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com