
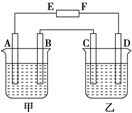
 在如圖中,E和F分別為電源兩極;甲燒杯中盛有100mL 0.2mol?L-1 AgNO3溶液,乙燒杯中盛有100mL 0.15mol?L-1 CuCl2溶液,A、B、C、D均為石墨電極,如果電解一段時間后,發現B極增重1.08g,則
在如圖中,E和F分別為電源兩極;甲燒杯中盛有100mL 0.2mol?L-1 AgNO3溶液,乙燒杯中盛有100mL 0.15mol?L-1 CuCl2溶液,A、B、C、D均為石墨電極,如果電解一段時間后,發現B極增重1.08g,則| 0.01mol |
| 0.1L |
| ||


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
| A、某物質的名稱為3,3-二甲基丁烷 |
| B、CH3-CH=CH-C≡C-CF3分子結構中6個碳原子可能在一條直線上 |
| C、某物質的名稱為2-乙基-1-丁烯 |
| D、1mol甲基(-CH3)中所含電子數為9mol |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、二氧化硅的分子式:SiO2 | ||
B、2-乙基丁烷: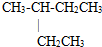 | ||
C、次氯酸的電子式: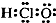 | ||
D、質子數為53,中子數為78的碘原子:
|
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、同溫同壓下,相同體積的物質,它們的物質的量必相等 |
| B、任何條件下,等質量的一氧化二氮(N2O)和二氧化碳所含的分子數必相等 |
| C、1L一氧化碳所體一定比1L氧氣質量小 |
| D、等體積、等物質的量濃度的鹽酸和醋酸(CH3COOH)中所含的H+數一定相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、體積:④<①<②<③ |
| B、密度:①<④<③<② |
| C、質量:④<①<③<② |
| D、氫原子數:②<④<③<① |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| 時間(min) | 1 | 2 | 3 | 4 | 5 |
| 氫氣體積(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com