
| ||
| ||
| ||
| ||
| 4 |
| 35 |
| ||
| ||


 寒假天地重慶出版社系列答案
寒假天地重慶出版社系列答案科目:高中化學 來源:2013-2014學年湖北省武漢市高三二月調研測試理科綜合化學試卷(解析版) 題型:選擇題
鋰的化合物用途廣泛。Li3N是非常有前途的儲氫材料;LiFePO4、Li2FeSiO4等可以作為電池的正級材料。回答下列問題:
(1)將鋰在純氮氣中燃燒可制得Li3N,其反應的化學方程為?????????????????????? 。
(2)氮化鋰在氫氣中加熱時可得到氨基鋰(LiNH2),其反應的化學方程式為:Li3N+2H2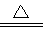 LiNH2+2LiH,氧化產物為?????????? (填化學式)。在270℃時,該反應可逆向發生放出H2,因而氮化鋰可作為儲氫材料,儲存氫氣最多可達Li3N質量的?????? %(精確到0.1)。
LiNH2+2LiH,氧化產物為?????????? (填化學式)。在270℃時,該反應可逆向發生放出H2,因而氮化鋰可作為儲氫材料,儲存氫氣最多可達Li3N質量的?????? %(精確到0.1)。
(3)將Li2CO3、FeC2O4·2H2O和SiO2粉末均勻混合,在800℃的氬氣中燒結6小時制得Li2FeSiO4,寫出反應的化學方程式?????????????????????????????????????????? ,制備Li2FeSiO4的過程必須在惰性氣體氛圍中進行,其原因是??????????????????? 。
(4)將一定濃度磷酸二氫銨、氯化鋰混合溶液作為電解液,以鐵棒為陽極,石墨為陰極,電解析出LiFePO4沉淀,陽極的電極反應式為???????????????????????????????? 。
(5)磷酸亞鐵鋰電池充放電過程中,發生LiFePO4與Li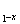 FePO4之間的轉化,電池放電時負極發生的反應為Li
FePO4之間的轉化,電池放電時負極發生的反應為Li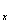 C6-
C6-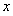 e—
e—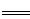
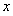 Li++6C,寫出電池放電時反應的化學方程式?????????????????????? 。
Li++6C,寫出電池放電時反應的化學方程式?????????????????????? 。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年山東省新泰市高三上學期階段化學試卷(解析版) 題型:填空題
鈉及其化合物具有廣泛的用途。
 (1)工業上可利用反應Na(1)+ KCl(1)
K(g)+ NaCl(1)來治煉金屬鉀,此反應利用了鈉的還原性及___
_____,
(1)工業上可利用反應Na(1)+ KCl(1)
K(g)+ NaCl(1)來治煉金屬鉀,此反應利用了鈉的還原性及___
_____,
寫出鈉與TiCl4反應冶煉Ti的化學方程式______________ _______。
(2)用Na2CO3熔融鹽作電解質,CO、O2為原料組成的新型電池的研究取得了重大突破。該電池示意圖如圖:
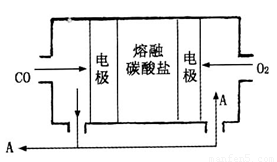
負極電極反應式為________________,為了使該燃料電池長時間穩定運行,電池的電解質組成應保持穩定,電池工作時必須有部分A物質參加循環。A物質的化學式為______________。
(3)Li-SOCl2電池可用于心臟起搏器。該電池的電極材料分別為鋰和碳,電解液是
LiAlCl4-SOCl2。電池的總反應可表示為: 4Li + 2SOCl2 =4LiCl + S + SO2。
請回答下列問題:
①電池的負極材料為 ,發生的電極反應為 ;
②電池正極發生的電極反應為 ;
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com