
【題目】下列各組的兩種物質在溶液中的反應,可用同一離子方程式表示的( )
A.氫氧化鈉與鹽酸;氫氧化銅與鹽酸
B.BaCl2溶液與Na2SO4溶液;Ba(OH)2溶液與H2SO4溶液
C.Na2CO3溶液與硝酸溶液;CaCO3溶液與硝酸溶液
D.石灰石與硝酸反應;石灰石與鹽酸
【答案】D
【解析】
A.氫氧化鈉與鹽酸的離子方程式為H++OH-=H2O;而氫氧化銅與鹽酸的離子方程式為Cu(OH)2+2H+=Cu2++2H2O,故不可用同一離子方程式表示,A不合題意;
B.BaCl2溶液與Na2SO4溶液的離子方程式為Ba2++![]() =BaSO4↓;Ba(OH)2溶液與H2SO4溶液的離子方程式為2H++Ba2++
=BaSO4↓;Ba(OH)2溶液與H2SO4溶液的離子方程式為2H++Ba2++![]() +2OH-=BaSO4↓+2H2O,故不可用同一離子方程式表示,B不合題意;
+2OH-=BaSO4↓+2H2O,故不可用同一離子方程式表示,B不合題意;
C.Na2CO3溶液與硝酸溶液的離子方程式為![]() ;CaCO3溶液與硝酸溶液的離子方程式為CaCO3+2H+=Ca2++H2O+CO2↑,故不可用同一離子方程式表示,C不合題意;
;CaCO3溶液與硝酸溶液的離子方程式為CaCO3+2H+=Ca2++H2O+CO2↑,故不可用同一離子方程式表示,C不合題意;
D.石灰石與硝酸反應的離子方程式為CaCO3+2H+=Ca2++H2O+CO2↑;石灰石與鹽酸的離子方程式為CaCO3+2H+=Ca2++H2O+CO2↑,故可用同一離子方程式表示,D符合題意;
故答案為:D。


科目:高中化學 來源: 題型:
【題目】工廠化驗員檢驗某含有KBrO3、KBr及惰性物的樣品。化驗員稱取了該固體樣品1.000 g,加水溶解后配成100 mL溶液X。
Ⅰ. 取25.00 mL溶液X,加入稀硫酸,然后用Na2SO3將BrO![]() 還原為Br-;
還原為Br-;
Ⅱ. 去除過量的SO![]() 后調至中性;
后調至中性;
Ⅲ. 加入K2CrO4作指示劑,用0.100 0 mol·L-1AgNO3標準溶液滴定Br-至終點,消耗 AgNO3標準溶液11.25 mL;
Ⅳ. 另取25.00 mL溶液X,酸化后加熱,再用堿液調至中性,測定過剩Br-,消耗上述AgNO3標準溶液3.75 mL。
已知:①25 ℃時,Ag2CrO4(磚紅色)的Ksp=1.12×10-12,AgBr(淺黃色)的Ksp=5.0×
10-15;
②Ⅳ中酸化時發生反應:BrO![]() +5Br-+6H+=== 3Br2+3H2O
+5Br-+6H+=== 3Br2+3H2O
請回答:
(1)步驟Ⅰ中,反應的離子方程式為________________________________。
(2)步驟Ⅲ中,滴定終點的現象為_____________________________________________。
(3)步驟Ⅳ中,加熱的目的是________________________。
(4)計算試樣中KBrO3質量分數。(寫出計算過程,結果保留3位有效數字)_______________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有關下列四組實驗描述不正確的是
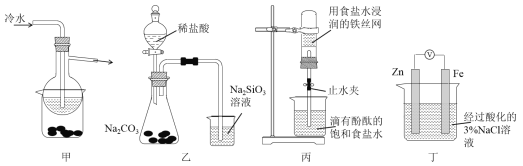
A. 加熱甲裝置中的燒杯可以分離SiO2和NH4Cl
B. 利用裝置乙可證明非金屬性強弱:Cl>C>Si
C. 打開丙中的止水夾,一段時間后,可觀察到燒杯內溶液上升到試管中
D. 向丁中鐵電極區滴入2滴鐵氰化鉀溶液,一段時間后,燒杯中不會有藍色沉淀生成
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,向20mL0.2mol·L-1H2X溶液中滴加0.2mol·L-1NaOH溶液,在不同pH環境下不同形態的粒子組成分數如圖所示,下列說法正確的是
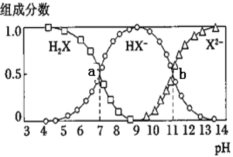
A.水的電離程度:b點小于點a
B.將等物質的量的NaHX、Na2X溶于水中,所得溶液pH恰好為11
C.常溫下的Ka(HY)=1.1×10-10,將少量H2X溶液加入到足量NaY溶液中,發生的反應為:H2X+Y-=HY+HX-
D.常溫下,反應X2-+H2OHX-+OH-的平衡常數對數值1gK=-11
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】a、b、c、d、e五種短周期元素的原子半徑與原子序數的關系如下圖,下列說法錯誤的是( )
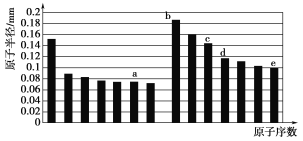
A. a、e兩種元素的氣態氫化物的沸點相比,前者較高
B. c、e兩種元素的離子半徑相比,前者較小
C. 由a與d兩種元素組成的化合物不能與任何酸反應,但能與強堿反應
D. c的氧化物能溶于b的氫氧化物的水溶液和e的氫化物的水溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知,四邊形![]() 內接于
內接于![]() ,
,![]() ,連接
,連接![]() 、
、![]() 交于點
交于點![]() .
.

(1)如圖![]() ,求證:
,求證:![]() ;
;
(2)如圖![]() ,過點
,過點![]() 作
作![]() 于點
于點![]() ,若
,若![]() ,求證:
,求證:![]() ;
;
(3)如圖![]() ,在(2)的條件下,作
,在(2)的條件下,作![]() ,
,![]() 交
交![]() 于點
于點![]() ,
,![]() 交
交![]() 于點
于點![]() ,且
,且![]() ,若
,若![]() ,
,![]() ,求
,求![]() 的半徑.
的半徑.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】SO2是大氣污染物之一,也是重要的化工原料。
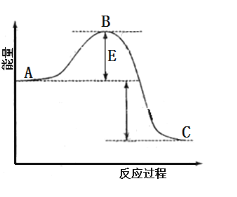
(1)某溫度下,反應![]()
![]() 的能量變化如圖。根據反應自發性判斷,反應在______(填“高溫”“低溫”或“任何溫度”)條件下可能有自發性,逆反應的活化能為______。
的能量變化如圖。根據反應自發性判斷,反應在______(填“高溫”“低溫”或“任何溫度”)條件下可能有自發性,逆反應的活化能為______。
(2)將0.1 mol O2和0.2 mol SO2通入一容積可變的容器中進行反應:![]() 。測得SO2的平衡轉化率隨溫度、壓強的變化如圖。
。測得SO2的平衡轉化率隨溫度、壓強的變化如圖。
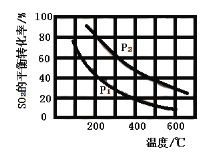
①![]() ______(填“>”“<”或“=”)
______(填“>”“<”或“=”)![]() 。
。
②若在300℃、壓強為![]() 時,反應達到平衡,容器容積恰好為10 L,則此狀態下反應的平衡常數K=____________。
時,反應達到平衡,容器容積恰好為10 L,則此狀態下反應的平衡常數K=____________。
③反應![]() 在
在![]() 時刻達到平衡后,在
時刻達到平衡后,在![]() 時刻速率發生如圖所示變化,此刻可能改變的反應條件可能是______(填標號)。
時刻速率發生如圖所示變化,此刻可能改變的反應條件可能是______(填標號)。
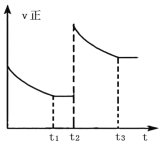
A.加壓B.向體系中再通入一定量SO2
C.升高溫度D.加催化劑
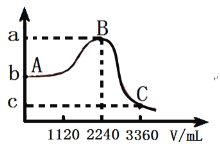
(3)常溫下,向1L![]() 的水溶液中緩慢通入SO2氣體(忽略溶液體積的變化),該溶液的pH與通入SO2氣體的體積(標準狀況)的關系如圖,則
的水溶液中緩慢通入SO2氣體(忽略溶液體積的變化),該溶液的pH與通入SO2氣體的體積(標準狀況)的關系如圖,則![]() _____;
_____;![]() _____;
_____;![]() _____。已知:常溫下,氫硫酸的
_____。已知:常溫下,氫硫酸的![]() 、
、![]() ,亞硫酸的
,亞硫酸的![]() 、
、![]() ;
;![]() 。
。
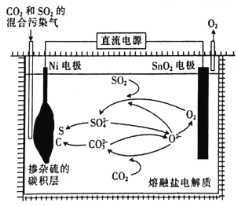
(4)用電解法處理CO2和SO2的混合污染氣的原理如圖所示,電解質為熔融碳酸鹽和硫酸鹽,通電一段時間后,Ni電極表面形成摻雜硫的碳積層,則與Ni電極相連的是電源的______(填“正極”或“負極”);陽極的電極反應式為________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】馬日夫鹽[Mn(H2PO4)2·H2O]主要用作磷化劑。以軟錳礦(主要成分為MnO2及少量的FeO、Al2O3和SiO2)為原料制備馬日夫鹽的主要工藝流程如圖:
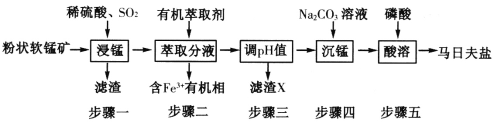
(1)按照無機物命名規律,馬日夫鹽[Mn(H2PO4)2·2H2O]的化學名稱為______。在反應中,Mn2+若再失去一個電子比Fe2+再失去一個電子難,從原子結構解釋其原因_______。
(2)“浸錳”過程中主要反應的離子方程式為_______。濾渣X主要成分為_________。檢驗“沉錳”已完成的實驗操作及現象是_________。步驟五產生馬日夫鹽晶體的化學方程式為_________。
(3)Fe3+的萃取率與溶液的pH和接觸時間之間的關系如圖,據此分析,萃取的最佳條件為__________。

(4)馬日夫鹽作防銹磷化劑的原因是利用其較強的酸性以及在防銹處理過程中生成了具有保護作用的FeHPO4,馬日夫鹽顯酸性的主要原因是__________(用相關化學用語回答)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com