
| A. | 黃銅(銅鋅合金)制作的銅鑼不易產生銅綠 | |
| B. | 生鐵比軟鐵芯(幾乎是純鐵)容易生銹 | |
| C. | 鐵質器件附有銅質配件,接觸處容易生鐵銹 | |
| D. | 銀質獎牌放置久了表面變暗 |
分析 A、銅鋅合金在電解質溶液中形成原電池反應,依據原電池電極反應分析判斷;
B、生鐵中含有碳,在電解質溶液中形成原電池反應,鐵做原電池的負極;
C、鐵和銅接觸處和電解質溶液會形成原電池反應,鐵做負極;
D、銀在空氣中被氧化發生化學腐蝕.
解答 解:A、銅鋅合金在電解質溶液中形成原電池反應,鋅做負極被腐蝕.正極被保護,所以不易形成銅綠;和電化學有關,故A不符合;
B、生鐵中含有碳,在電解質溶液中形成原電池反應,鐵做原電池的負極發生氧化反應被腐蝕;所以容易生銹,故B不符合;
C、鐵和銅接觸處和電解質溶液會形成原電池反應,鐵做負極發生氧化反應被腐蝕,故C不符合;
D、銀在空氣中被氧化發生化學腐蝕;和電化腐蝕無關,故D符合;
故選D.
點評 本題考查了化學腐蝕和電化腐蝕的實質分析,原電池的形成條件是解題關鍵,題目較簡單.


科目:高中化學 來源: 題型:選擇題
| A. | 因為H-F的鍵能大于H-CI,所以HF的沸點高于HCI | |
| B. | 因為HCIO4比HCIO中的氯元素的化合價高,所以HCIO4的氧化性強于HCIO | |
| C. | 因為N元素的非金屬性比P元素強,所以NH3的穩定性強于PH3 | |
| D. | 因為Fe的還原性強于Cu,所以Cu2+的氧化性強于Fe3+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 非金屬性X>Y>Z | |
| B. | 含氧酸的酸性H3ZO4>H2YO4>HXO4 | |
| C. | 元素的負化合價的絕對值按X、Y、Z變小 | |
| D. | 原子半徑:X>Y>Z |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | A原子的最外層電子數比B原子的最外層電子數少 | |
| B. | A原子的電子層數比B原子的電子層數多 | |
| C. | 1mol A從酸中置換H+生成的H2比1mol B從酸中置換H+生成的H2多 | |
| D. | 常溫時,A能從水中置換出氫,而B不能 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.11mol | B. | 0.22mol | C. | 0.16mol | D. | 0.1mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3CH2COOH | B. | HCOOCH2CH3 | C. | CH3COOCH3 | D. | CH3COCH2OH |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 先加入稀硝酸,沒有產生沉淀,然后再加硝酸鋇,產生白色沉淀,證明有SO42-存在 | |
| B. | 先加入硝酸鋇,產生白色沉淀,然后再加稀硝酸,沉淀不溶解,證明有SO42-存在 | |
| C. | 先加入稀鹽酸,沒有產生沉淀,然后再加氯化鋇,產生白色沉淀,證明有SO42-存在 | |
| D. | 先加入氯化鋇,產生白色沉淀,然后再加稀鹽酸,沉淀不溶解,證明有SO42-存 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
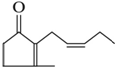 有機化合物A是人工合成的香料茉莉酮,其結構簡式如圖:
有機化合物A是人工合成的香料茉莉酮,其結構簡式如圖:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com