
測定硫酸銅晶體CuSO4、xH2O里的結晶水含量,造成x偏高的原因是
[ ]
A.晶體完全變成白色粉末,繼續加熱出現黑色物質CuO
B.坩堝未干燥就稱量
C.盛白色CuSO4粉末的坩堝置于空氣中冷卻后再稱量
D.坩堝內壁附有受熱不分解的惰性物質
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:閱讀理解
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
| O | 2- 7 |
查看答案和解析>>
科目:高中化學 來源: 題型:
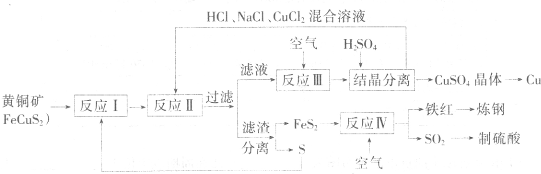
一種以黃銅礦和硫磺為原料制取銅和其他產物的新工藝,原料的綜合利用率較高。其主要流程如下:

注:反應Ⅱ的離子方程式為Cu2++CuS+4Cl—=2CuCl2-+S
請回答下列問題:
⑴反應Ⅰ的產物為(填化學式) ▲ 。
⑵反應Ⅲ的離子方程式為 ▲ 。
⑶一定溫度下,在反應Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸銅晶體,其原因是
▲ 。
⑷煉鋼時,可將鐵紅投入熔融的生鐵中,該過程中主要反應的化學方程式是 ▲ 。
⑸某硫酸廠為測定反應Ⅳ所得氣體中SO2的體積分數,取280mL(已折算成標準狀況)氣體樣品與足量Fe2(SO4)3溶液完全反應后,用濃度為0.02000 mol/L的K2Cr2O7標準溶液滴定至終點,消耗K2Cr2O7溶液25.00 mL 。
已知:Cr2O72-+ Fe2++ H+→Cr3++ Fe3++ H2O(未配平)
①SO2通入Fe2(SO4)3溶液,發生反應的離子方程式為 ▲ 。
②反應Ⅳ所得氣體中SO2的體積分數為 ▲ 。
查看答案和解析>>
科目:高中化學 來源:2013屆遼寧省沈陽市第二十中學高三高考領航考試(三)化學試卷(帶解析) 題型:填空題
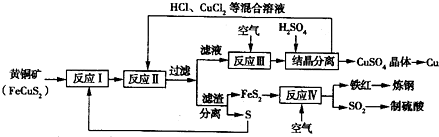
【化學——選修化學與技術】(15分)現有一種以黃銅礦和硫磺為原料制取銅和其他產物的新工藝,原料的綜合利用率較高。其主要流程如下:
注:反應Ⅱ的離子方程式為Cu2++CuS+4Cl—=2[CuCl2]-+S
請回答下列問題:
(1)從黃銅礦冶煉粗銅的傳統工藝是將精選后的富銅礦砂與空氣在高溫下煅燒,使其轉變為銅。這種方法的缺點是 _____________________ ________、___________________________________ 。
(2)反應Ⅰ的產物為(填化學式) ___________________ 。
(3)反應Ⅲ的離子方程式為 ____________________________________________________ 。
(4)一定溫度下,在反應Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸銅晶體,其原因是 ___________
(5)黃銅礦中Fe的化合價為+2,對于反應:8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2,下列有關該反應的說法正確的是 ___________________ (填字母)。
8Cu+4FeO+2Fe2O3+16SO2,下列有關該反應的說法正確的是 ___________________ (填字母)。
| A.反應中被還原的元素只有氧 | B.反應生成的SO2直接排放會污染環境 |
| C.SO2既是氧化產物又是還原產物 | D.當有8mol銅生成時,轉移電子數目為100NA |
查看答案和解析>>
科目:高中化學 來源:2012-2013學年遼寧省沈陽市高三高考領航考試(三)化學試卷(解析版) 題型:填空題
【化學——選修化學與技術】(15分)現有一種以黃銅礦和硫磺為原料制取銅和其他產物的新工藝,原料的綜合利用率較高。其主要流程如下:

注:反應Ⅱ的離子方程式為Cu2++CuS+4Cl—=2[CuCl2]-+S
請回答下列問題:
(1)從黃銅礦冶煉粗銅的傳統工藝是將精選后的富銅礦砂與空氣在高溫下煅燒,使其轉變為銅。這種方法的缺點是 _____________________ ________、___________________________________ 。
(2)反應Ⅰ的產物為(填化學式) ___________________ 。
(3)反應Ⅲ的離子方程式為 ____________________________________________________ 。
(4)一定溫度下,在反應Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸銅晶體,其原因是 ___________
(5)黃銅礦中Fe的化合價為+2,對于反應:8CuFeS2+21O2 8Cu+4FeO+2Fe2O3+16SO2,下列有關該反應的說法正確的是 ___________________ (填字母)。
8Cu+4FeO+2Fe2O3+16SO2,下列有關該反應的說法正確的是 ___________________ (填字母)。
A.反應中被還原的元素只有氧 B.反應生成的SO2直接排放會污染環境
C.SO2既是氧化產物又是還原產物 D.當有8mol銅生成時,轉移電子數目為100NA
(6)某硫酸廠為測定反應Ⅳ所得氣體中SO2的體積分數,取280mL(已折算成標準狀況)氣體樣品與足量Fe2(SO4)3溶液完全反應后,用濃度為0.02000 mol/L的K2Cr2O7標準溶液滴定至終點,消耗K2Cr2O7溶液25.00 mL 。
已知:Cr2O72-+ Fe2++ H+→Cr3++ Fe3++ H2O(未配平)
①SO2通入Fe2(SO4)3溶液,發生反應的離子方程式為 ____________________________________ 。
②反應Ⅳ所得氣體中SO2的體積分數為________________________________________________ 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com