
【題目】Cl2及其化合物在生產、生活中具有廣泛的用途.將氯氣溶于水能形成氯氣﹣氯水體系.
完成下列填空:
(1)氯原子最外層電子的電子排布式是__.與電子排布式相比,軌道表示式增加了對核外電子運動狀態中__描述.
(2)氫、氯、氧三種元素各能形成一種簡單陰離子,按離子半徑由大到小的順序排列這些離子__.
(3)氯氣﹣氯水體系中,存在多個含氯元素的平衡關系,請分別用平衡方程式表示:__.已知HClO的殺菌能力比ClO﹣強,氯處理飲用水時,在夏季的殺菌效果比在冬季差,可能原因是__(一種原因即可).
(4)在氯水中,下列關系正確的是__(選填編號).
a c(HClO)+c(ClO﹣)=c(H+)﹣c(OH﹣)
b c(H+)=c(ClO﹣)+c(Cl﹣)+c(OH﹣)
c c(HClO)<c(Cl﹣)
d c(Cl﹣)<c(OH﹣)
(5)ClO2是一種更高效、安全的消毒劑,工業上可用ClO2與水中的MnCl2在常溫下反應,生成MnO2和鹽酸,以除去水中Mn2+,寫出該反應的化學方程式(需配平)__.有人認為產物MnO2和鹽酸會繼續反應生成氯氣,這種認識對嗎?__(填“對”或“錯”),說明理由__.
【答案】3s23p5 自旋方向 Cl﹣、O2﹣、H﹣ Cl2(aq)+H2O![]() HClO+H++Cl﹣、HClO
HClO+H++Cl﹣、HClO![]() H++ClO﹣、Cl2(g)
H++ClO﹣、Cl2(g)![]() Cl2(aq) 夏季溫度高,HClO易分解,殺菌效果比在冬季差 bc 2ClO2+5MnCl2+6H2O=5MnO2+12HCl 錯 MnO2和濃鹽酸加熱的條件下才能反應
Cl2(aq) 夏季溫度高,HClO易分解,殺菌效果比在冬季差 bc 2ClO2+5MnCl2+6H2O=5MnO2+12HCl 錯 MnO2和濃鹽酸加熱的條件下才能反應
【解析】
(1)氯是17號元素,其最外層電子的電子排布式為![]() ,若用軌道表示式來描述,則可以描述其電子的自旋方向;
,若用軌道表示式來描述,則可以描述其電子的自旋方向;
(2)![]() 相當于光禿禿的質子,
相當于光禿禿的質子,![]() 填滿了前兩層電子,而
填滿了前兩層電子,而![]() 填滿了前三層電子,半徑由大到小為
填滿了前三層電子,半徑由大到小為![]() ;
;
(3)首先氯氣存在溶解—揮發平衡,即![]() ,其次氯氣還能和水發生可逆反應,即
,其次氯氣還能和水發生可逆反應,即![]() ,而
,而![]() 是一個弱酸,存在電離平衡
是一個弱酸,存在電離平衡![]() ; 夏季和冬季最大的區別在溫度,我們知道
; 夏季和冬季最大的區別在溫度,我們知道![]() 受熱易分解,因此殺菌效果變差;
受熱易分解,因此殺菌效果變差;
(4)a.溶液中存在質子守恒![]() ,若要a項成立除非
,若要a項成立除非![]() ,但是二者不可能相等,a項錯誤;
,但是二者不可能相等,a項錯誤;
b.該項即溶液中存在的質子守恒,b項正確;
c.氯氣和水反應得到等量的![]() 和
和![]() ,
,![]() 是強酸可以完全電離,因此溶液中
是強酸可以完全電離,因此溶液中![]() 的量等于生成的
的量等于生成的![]() 的量,而
的量,而![]() 是弱電解質部分電離,因此剩余的
是弱電解質部分電離,因此剩余的![]() 的濃度將小于
的濃度將小于![]() 的濃度,c項正確;
的濃度,c項正確;
d.氯水呈酸性,因此溶液中的![]() 極低(室溫下
極低(室溫下![]() ),因此不可能出現
),因此不可能出現![]() 的情況,d項錯誤;
的情況,d項錯誤;
答案選bc;
(5)![]() 作氧化劑,
作氧化劑,![]() 作還原劑,二者發生氧化還原反應
作還原劑,二者發生氧化還原反應![]() ,該反應得到的鹽酸較稀,且沒有加熱,因此不太可能被
,該反應得到的鹽酸較稀,且沒有加熱,因此不太可能被![]() 繼續氧化變成氯氣,反應在這一步就停止了。
繼續氧化變成氯氣,反應在這一步就停止了。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】實驗室制取少量溴乙烷的裝置如圖所示。根據題意完成下列填空:
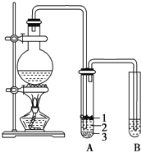
(1)圓底燒瓶中加入的反應物是溴化鈉、乙醇 和1:1的硫酸。配制體積比1:1的硫酸所用的儀器為 ________(選填編號)。
a 天平 b 量筒 c 容量瓶 d 燒杯
(2)寫出加熱時燒瓶中發生的主要反應的化學方程式 ___________________ 。
(3)將 生成物導入盛有冰水混合物的試管A中,冰水混合物的作用是________,試管A中的物質分為三層(如圖所示),產物在第____層。
(4)試管A中除了產物和水之外,還可能存在 ________ ,_________ (寫出結構簡式)。
(5)用濃硫酸進行實驗,若試管A中獲得的有機物呈棕黃色,除去其中雜質的最佳方法是 ___________(選填編號)。
a 蒸餾 b 氫氧化鈉溶液洗滌 c 用四氯化碳萃取 d 用亞硫酸鈉溶液洗滌
若試管B中的酸性高錳酸鉀溶液褪色,使之褪色的物質名稱是_________。
(6)實驗員老師建議把上述裝置中的儀器連接部分由橡膠管改成標準玻璃接口,其原因_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮元素的化合物在工農業以及國防科技中用途廣泛,但也會對環境造成污染,如地下水中硝酸鹽造成的氮污染已成為一個世界性的環境問題。
(1)神舟載人飛船的火箭推進器中常用肼(N2H4)作燃料。NH3與NaClO反應可得到肼(N2H4),該反應中被氧化與被還原的元素的原子個數之比為___。如果反應中有5mol電子發生轉移,可得到___ g肼。
(2)常溫下向25mL0.01mol/L稀鹽酸中緩緩通入5.6mLNH3(標準狀況,溶液體積變化忽略不計),反應后溶液中離子濃度由大到小的順序是___。在通入NH3的過程中溶液的導電能力___(填寫“變大”、“變小”或“幾乎不變”)。
(3)向上述溶液中繼續通入NH3,該過程中離子濃度大小關系可能正確的是___(選填編號)。
a.[Cl-]=[NH4+]>[H+]=[OH-] b.[Cl-]>[NH4+]=[H+]>[OH-
c.[NH4+]>[OH-]>[Cl-]>[H+] d.[OH-]>[NH4+]>[H+]>[Cl-]
(4)常溫下向25mL含HCl0.01mol的溶液中滴加氨水至過量,該過程中水的電離平衡(填寫電離平衡移動情況)___。當滴加氨水到25mL時,測得溶液中水的電離度最大,則氨水的濃度為___mol·L-1。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 均是短周期元素,它們在元素周期表中的相對位置如圖所示,其中
均是短周期元素,它們在元素周期表中的相對位置如圖所示,其中![]() 與
與![]() 形成的一種化合物能使品紅溶液褪色,下列說法正確的是( )
形成的一種化合物能使品紅溶液褪色,下列說法正確的是( )

A.![]() 與
與![]() 形成的兩種常見化合物中含有的化學鍵類型全部相同
形成的兩種常見化合物中含有的化學鍵類型全部相同
B.可用![]() 溶液除去
溶液除去![]() 單質中混有的
單質中混有的![]() 單質
單質
C.簡單氫化物的熱穩定性:![]()
D.化合物![]() 和
和![]() 中,陽離子半徑均大于陰離子半徑
中,陽離子半徑均大于陰離子半徑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】與下列事實對應的化學用語錯誤是( )
A.純堿溶液能清洗油污:CO32﹣+H2OHCO3﹣+OH﹣
B.配制FeSO4溶液時加入適量的鐵粉:Fe3++Fe→2Fe2+
C.含1molNaOH和1molNa2CO3的混合溶液中滴入含1.5molHCl的稀鹽酸:2OH﹣+CO32﹣+3H+→HCO3﹣+2H2O
D.NH4Al(SO4)2溶液中滴入Ba(OH)2溶液至SO42﹣恰好沉淀完全:2Ba2++4OH﹣+Al3++2SO42﹣→2BaSO4↓+AlO2﹣+2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有兩種氣態單質![]() 和
和![]() ,已知
,已知![]() 和
和![]() 所含的原子個數相等,分子數之比為
所含的原子個數相等,分子數之比為![]() 。
。![]() 和
和![]() 的原子核內質子數都等于中子數,
的原子核內質子數都等于中子數,![]() 原子
原子![]() 層電子數是
層電子數是![]() 層的3倍。
層的3倍。
(1)![]() 、
、![]() 的元素符號分別為_______。
的元素符號分別為_______。
(2)![]() 中的
中的![]() 值為_______。
值為_______。
(3)![]() 的能層數目為_______。
的能層數目為_______。
(4)![]() 、
、![]() 形成的一種氣態化合物與水反應能生成由
形成的一種氣態化合物與水反應能生成由![]() 、
、![]() 形成的另一種氣態化合物,寫出該反應的化學方程式:_______。
形成的另一種氣態化合物,寫出該反應的化學方程式:_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為探究銅與稀硝酸反應的氣態產物中是否含NO2,進行如下實驗.
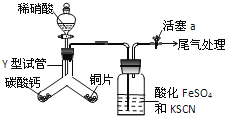
已知:FeSO4+NO→[Fe(NO)]SO4,該反應較緩慢,待生成一定量[Fe(NO)]2+時突顯明顯棕色.
(1)實驗前需檢驗裝置的氣密性,簡述操作__.
(2)實驗開始時先將Y形試管向盛有碳酸鈣的支管傾斜,緩慢滴入稀硝酸,該實驗操作的目的是__;銅片和稀硝酸反應的化學方程式為__.
(3)洗氣瓶中加入KSCN溶液的目的及原理是__;本實驗只觀察到洗氣瓶中出現了棕色,寫出尾氣處理的化學方程式__.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式與所述事實相符且正確的是
A.NaHS水解反應:HS-+H2O![]() H3O++S2-
H3O++S2-
B.Fe(OH)2與稀硝酸反應:2H++Fe(OH)2=Fe2++2H2O
C.Na2CO3水溶液中存在平衡:CO32-+H2O![]() HCO3-+OH-
HCO3-+OH-
D.BaSO4的水溶液導電性極弱:BaSO4![]() Ba2++SO42-
Ba2++SO42-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某一元弱酸(用HA表示)在水中的電離方程式是:HA![]() H++A-,回答下列問題:
H++A-,回答下列問題:
(1)向溶液中加入適量NaA固體,以上平衡將向________(填“正”、“逆”)反應方向移動,理由是________ 。
(2)若向溶液中加入適量NaCl溶液,以上平衡將向______(填“正”、“逆”)反應方向移動,溶液中c(A-)將________(填“增大”、“減小”或“不變”),溶液中c(OH-)將________(填“增大”、“減小”或“不變”)。
(3)在25 ℃下,將a mol·L-1的氨水與0.01 mol·L-1的鹽酸等體積混合,反應平衡時溶液中c(NH4+)=c(Cl-),則溶液顯_______性(填“酸”、“堿”或“中”);用含a的代數式表示NH3·H2O的電離常數Kb=______ 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com