
【題目】填寫下列空白:
(1)將等物質的量的NH3和CH4混合,混合氣體中NH3與CH4的質量比為____________。
(2)要使NH3與CH4含相同數目的H原子,則NH3和CH4的物質的量之比為__________。
(3)標準狀況下,密度為0.75 g·L-1的NH3與CH4組成的混合氣體中,NH3的體積分數為__________,該混合氣體對氫氣的相對密度為________。
(4)已知a g A和b g B恰好完全反應生成0.2 mol C和d g D,則C的摩爾質量為__________________。
(5)同溫同壓下,已知O2的密度為ρg/L,則CO2的密度為__________。
(6)現有下列三種氣體:①32 g CH4;②約含有6.02×1023個HCl分子的氯化氫氣體;③標準狀況下33.6 LO2。請按物理量由小到大的順序排列:a.質量________(填序號,下同);b.分子數目________c.相同狀況下氣體的體積________。
【答案】17:164:380%8.45(a+b-d)g/mol11ρ/8①②③②③①②③①
【解析】
(1).將等物質的量的NH3和CH4混合,設NH3與CH4的物質的量均為1mol,則m(NH3)=1mol×17g/mol=17g,m(CH4)=1mol×16g/mol=16g,所以混合氣體中NH3與CH4的質量比為17:16,故答案為:17:16;
(2).要使NH3與CH4含有相同數目的H原子,設NH3和CH4的物質的量分別為amol、bmol,則有amol×3=4mol×b,a:b=4:3,故答案為:4:3;
(3).標準狀況下,混合氣體的平均摩爾質量為0.75 g·L-1×22.4L/mol=16.8g,設氨氣的體積分數為x,有17x+16(1-x)=16.8,解得x=0.8,即氨氣的體積分數為80%;相同條件下,該混合氣體對氫氣的相對密度等于其摩爾質量之比即![]() =8.4,故答案為:80%;8.4;
=8.4,故答案為:80%;8.4;
(4).已知a g A和b g B恰好完全反應生成0.2 mol C和d g D,由質量守恒可知C的質量為m(C)=(a+b-d)g,則C的摩爾質量為M(C)=![]() =5(a+b-d)g/mol,故答案為:5(a+b-d)g/mol;
=5(a+b-d)g/mol,故答案為:5(a+b-d)g/mol;
(5).同溫同壓下,氣體的密度之比等于其摩爾質量之比,設CO2的密度為a g/L,則![]() =
=![]() =
=![]() ,解得a=
,解得a=![]() g/L,故答案為:11ρ/8;
g/L,故答案為:11ρ/8;
(6).現有下列三種氣體:①32 g CH4的物質的量為32g÷16g/mol=2mol;②約含有6.02×1023個HCl分子的氯化氫氣體,其物質的量為![]() =1mol,質量為1mol×36.5g/mol=36.5g;③標準狀況下33.6 LO2的物質的量為33.6L÷22.4L/mol=1.5mol,質量為1.5mol×32g/mol=48g,則a.三種物質的質量由小到大的順序為①②③,b.物質的分子個數之比等于其物質的量之比,則分子數目由小到大的順序為②③①,c. 相同狀況下氣體的體積之比等于其物質的量之比,則氣體的體積由小到大的順序為②③①,故答案為:①②③;②③①;②③①。
=1mol,質量為1mol×36.5g/mol=36.5g;③標準狀況下33.6 LO2的物質的量為33.6L÷22.4L/mol=1.5mol,質量為1.5mol×32g/mol=48g,則a.三種物質的質量由小到大的順序為①②③,b.物質的分子個數之比等于其物質的量之比,則分子數目由小到大的順序為②③①,c. 相同狀況下氣體的體積之比等于其物質的量之比,則氣體的體積由小到大的順序為②③①,故答案為:①②③;②③①;②③①。


科目:高中化學 來源: 題型:
【題目】濃度均為0.01mol·L-1、體積均為V1L的兩種一元酸HX和HY的水溶液,加水稀釋至體積為VL,測得兩溶液pH隨lg![]() 變化的情況如圖所示,下列說法錯誤的是
變化的情況如圖所示,下列說法錯誤的是
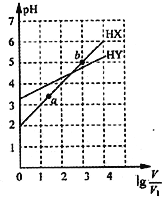
A. HY為一元弱酸 B. 將兩種溶液無限稀釋,由水電離產生的c(H+)相等
C. lg![]() =3時,升高溫度,
=3時,升高溫度,![]() 增大 D. HX 的電離程度:b>a
增大 D. HX 的電離程度:b>a
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】廣泛用于紡織工業的連二亞硫酸鈉(Na2S2O4),俗稱保險粉,是一種強還原劑,可溶于水,但不溶于乙醇,在堿性介質中穩定。
Ⅰ.工業上制備連二亞硫酸鈉的流程如下:

請回答下列問題:
(1)步驟①中的化學方程式為___________________________________;
(2)步驟②中沉淀為_________________________________(填化學式);
(3)步驟③中加入NaCl 固體的作用是______________________________,分離出保險粉方法為_______、洗滌、干燥,洗滌所用試劑是___________________________。
Ⅱ.工業上也可用右圖裝置電解NaHSO3溶液制Na2S2O4。
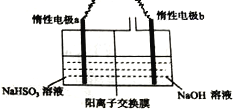
(1)惰性電極a連接電源的_________(填“正極”或“負極”),其電極反應式為________________;
(2)若不加隔膜,則得不到連二亞硫酸鈉,其原因是____________________________。
Ⅲ.探究Na2S2O4的性質:
某課題小組常溫下測定0.050 molL-1Na2S2O4溶液在空氣中的pH變化如下圖所示;
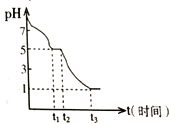
(1)0-t1段主要生成HSO3-,根據pH變化圖,寫出0- t1發生反應的離子方程式為______________;
(2)若t1時溶液中Na2S2O4全部被氧化成NaHSO3,此時溶液中c(SO32-)-c(H2SO3) =__________ molL-1(填具體數值,不考慮溶液體積變化)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:在常溫下,苯(C6H6)為一種無色、透明的液體,毒性較高,易揮發,易燃,有腐蝕性,沸點為80.1℃,難溶于水,易溶于有機溶劑,可作為有機溶劑;碘(I2)為紫黑色晶體,易升華,易凝華,熔點113.5℃,沸點184.3℃,加熱時碘升華為紫色蒸氣,冷卻后凝華成紫黑色固體。實驗室常用苯來提取碘水中的碘,具體操作如下:

①向碘的水溶液中加入萃取劑苯,轉移到分液漏斗中,塞上玻璃塞,充分振蕩放氣后(如圖1);
②將分液漏斗置于鐵架臺的鐵圈上靜置(如圖2);
③當分液漏斗中的液體分成清晰的兩層后,經“合適的操作”將兩層液體進行分離;
④將分離出的碘和苯的混合液轉移到儀器A中,加入少量沸石進行蒸餾以分離苯和碘(如圖3)。
請回答下列問題:
(1)分液漏斗在使用前必須進行的操作是_______。
(2)步驟③中“合適的操作”的名稱是________。
(3)步驟④中采用水浴加熱而不直接加熱的原因是________________;圖3中有多處明顯的錯誤:a.冷卻水進出方向錯誤.b.___________________。
(4)錐形瓶置于冰水中的目的是____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于第三周期從左到右的主族元素,下列說法中不正確的是( )
A.原子半徑逐漸減小
B.電子層數逐漸增多
C.最高正化合價逐漸增大
D.元素的非金屬性逐漸增強
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】全釩氧化還原電池是一種新型可充電池,不同價態的含釩離子作為正極和負極的活性物質,分別儲存在各自的酸性電解液儲罐中。其結構原理如圖所示,該電池放電時,右槽中的電極反應為:V2+-e-=V3+,下列說法正確的是

A. 放電時,右槽發生還原反應
B. 放電時,左槽的電極反應式:VO2++2H++e-=VO2++H2O
C. 充電時,每轉移1mol電子,n(H+)的變化量為1mol
D. 充電時,陰極電解液pH升高
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】煤氣中主要的含硫雜質有H2S以及COS(有機硫),煤氣燃燒后含硫雜質會轉化成SO2從而引起大氣污染,因此煤氣中H2S的脫出程度已成為煤氣潔凈度的一個重要指標。請回答下列問題:
(1)H2S在水溶液中的電離方程式為___________。
(2)脫除煤氣中COS的方法有Br2的KOH溶液氧化法、H2還原法、水解法等。
①COS的分子結構與CO2相似,COS的結構式為___________。
②Br2的KOH溶液將COS氧化為硫酸鹽的離子方程式為______________。
③已知:H2、COS、H2S、CO的燃燒熱依次為285kJ/mol、299kJ/mol、586kJ/mol、283kJ/mol;H2還原COS發生的反應為H2(g)+COS(g)=H2S(g)+CO(g),該反應的ΔH=_________kJ/mol。
④用活性α-Al2O3催化COS水解反應為COS(g)+H2O(g) ![]() CO2(g)+H2S(g) ΔH<0,相同流量且在催化劑表面停留相同時間時,不同溫度下COS的轉化率(未達到平衡)如圖1所示;某溫度下,COS的平衡轉化率與n(H2O)/n(COS)的關系如圖2所示。
CO2(g)+H2S(g) ΔH<0,相同流量且在催化劑表面停留相同時間時,不同溫度下COS的轉化率(未達到平衡)如圖1所示;某溫度下,COS的平衡轉化率與n(H2O)/n(COS)的關系如圖2所示。

由圖1可知,催化劑活性最大時對應的溫度約為______,COS的轉化率在后期下降的原因是_______________________________________。由圖2可知,P點時平衡常數K=______(保留2位有效數字)。Q點轉化率高于P點的原因是__________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在氯水中存在多種分子和離子,它們在不同的反應中表現各自的性質,下列實驗現象和結論一 致且正確的是
A. 加入有色布條,褪色,說明溶液中有 Cl2 存在
B. 溶液呈現黃綠色,且有刺激性氣味,說明有 Cl2 存在
C. 先加入鹽酸酸化,再加入硝酸銀溶液產生白色沉淀,說明有 Cl-存在
D. 新制氯水放置數天后酸性將減弱
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com