
| A. | Na2SO4=Na2++SO42- | B. | MgCl2=Mg2++Cl- | ||
| C. | HNO3=H++3NO- | D. | Ba(OH)2=Ba2++2OH- |
分析 A.鈉離子帶有一個正電荷;
B.電荷不守恒;
C.硝酸根離子符號錯誤;
D.Ba(OH)2是強電解質完全電離出鋇離子和氫氧根離子.
解答 解:A.鈉離子帶有一個正電荷,則其電離方程式為:Na2SO4=2Na++SO42-,故A錯誤;
B.氯化鎂在溶液中電離出一個鎂離子和兩個氯離子,則電離方程式為:MgCl2=Mg2++2Cl-,故B錯誤;
C.硝酸根離子符號錯誤,電離方程式為:HNO3=H++NO3-,故C錯誤;
D.Ba(OH)2是強電解質完全電離出鋇離子和氫氧根離子,則電離方程式為:Ba(OH)2=Ba2++2OH-,故D正確.
故選D.
點評 本題考查電離方程式的書寫知識,注意強電解質在溶液中能完全電離,弱電解質部分電離,離子團在電離方程式中不能拆開,強酸的酸式根離子要拆開,弱酸的酸式根離子不能拆開,題目難度不大.


科目:高中化學 來源: 題型:解答題
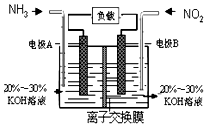 空氣質量與我們的健康息息相關,目我國通過檢測6項污染物的質量濃度來計算空氣質量指數(AQI),SO2、NO2、和CO是其中3項中的污染物.
空氣質量與我們的健康息息相關,目我國通過檢測6項污染物的質量濃度來計算空氣質量指數(AQI),SO2、NO2、和CO是其中3項中的污染物.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
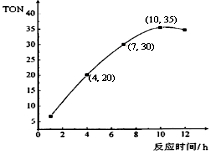 甲醇和CO2可直接合成DMC:2CH3OH(g)+CO2 (g)?CH3OCOOCH3 (g)+H2O(g),但甲醇轉化率通常不會超過1%,制約該反應走向工業化生產.
甲醇和CO2可直接合成DMC:2CH3OH(g)+CO2 (g)?CH3OCOOCH3 (g)+H2O(g),但甲醇轉化率通常不會超過1%,制約該反應走向工業化生產.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
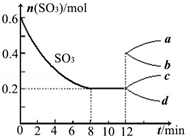 在一個2L的密閉容器中投入反應物,發生反應2SO3(g)?2SO2(g)+O2(g)△H>0,其中SO3的變化如圖所示:
在一個2L的密閉容器中投入反應物,發生反應2SO3(g)?2SO2(g)+O2(g)△H>0,其中SO3的變化如圖所示:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | “胃得樂”(主要成分為碳酸鎂)是一種抗酸藥) | |
| B. | 鴉片、嗎啡、海洛因等這些物質屬于毒品 | |
| C. | 青霉素能抑制細菌細胞壁的生長,致使細菌因細胞破裂而死亡 | |
| D. | “阿司匹林”是一種重要的抗生素 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一定條件下水由氣態變為液態 | |
| B. | 高溫高壓條件下使石墨轉化為金剛石 | |
| C. | 有序排列的火柴散落 | |
| D. | CO點燃時生成CO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 任何溫度下反應均難以自發進行 | B. | 任何溫度下反應均可以自發進行 | ||
| C. | 僅常溫下反應可以自發進行 | D. | 僅高溫下反應可以自發進行 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
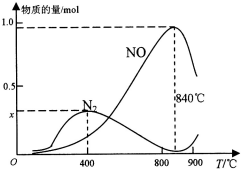 氨催化氧化是硝酸工業的基礎,按要求回答下列問題:
氨催化氧化是硝酸工業的基礎,按要求回答下列問題:| 化學鍵 | N-H |  | O-H | O=O |
| E/(kJ•mol-1) | x | y | m | n |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com