
�ĺ�ˮ����ȡ�V����������@���V����Ҫ��Դ����������ȡ�V���^�����漰�ĎN���|���ܶȷe������(j��)�����W��֪�R�ش����Ўׂ����}��
|
���| |
CaCO3 |
MgCO3 |
Ca(OH)2 |
Mg(OH)2 |
|
�ܶȷe |
2.8��10�C9 |
6.8��10�C6 |
5.5��10�C6 |
1.8��10�C11 |
(1)�ڏĺ�ˮ����ȡ�V�r�������õ�ؐ��(��Ҫ�ɷ���̼���})�����J�� (��ܡ����ܡ�)��ؐ����ĥ�ɷ�ĩֱ��Ͷ�뺣ˮ�У������� ���������ֱ��Ͷ�룬����ؐ������̎����ԇ�������W����ʽ ��
(2)ijͬ�W�ڌ���җl����ģ�Mԓ���a�^�̣�������ҟoʯ�ң��������ß��A���棬���J�� (����ԡ������ԡ�)�õ�Mg(OH)2���ڼ�ԇ���r���`�����A��Һ���뺣ˮ�У���˼����һ�£����ڵõ��Ļ���wϵ�м����^���ğ��A��Һ�����X���� (��ܡ����ܡ�)��Mg2+�D����Mg(OH)2������������ (���x�ӷ���ʽ��ʾ)��
(3)��֪��ˮ���V�x�ӝ�Ȟ�1.8��10�C3mol��L�C1���tҪʹ�V�x�Ӯa����������Һ��PH��͑��� ��
(1)����(1��)�� ؐ����ĥ�ɷ�ĩ����CaCO3��CaCO3���ܽ�ȱ�MgCO3���ܽ��С�����Ԍ���ֱ��Ͷ�뺣ˮ�в��ܮa��MgCO3(2��)�� CaCO3  CaO + CO2��(2��)��
(2)����(1��)��
CaO + CO2��(2��)��
(2)����(1��)��
��(1��)�� CO32�C + Mg2+ = MgCO3��MgCO3 + 2OH�C = Mg(OH)2 + CO32�C(4��) (3)10(2��)
��������
ԇ�}������(1)ؐ����ĥ�ɷ�ĩ����CaCO3��CaCO3���ܶȷe��MgCO3���ܶȷeС�����Ԍ���ֱ��Ͷ�뺣ˮ�в��ܮa��MgCO3������ؐ���џ���CaO��CaOͶ�뺣ˮ�����ɵ�Ca(OH)2ʹ��ˮ�е�Mg2+�D����Mg(OH)2������(2)NaOH��x����OH�C���cMg2+��������Mg(OH)2������Mg(OH)2���ܶȷeMgCO3���ܶȷe������ͨ�^�c���A������MgCO3�����D����Mg(OH)2������MgCO3 + 2OH�C = Mg(OH)2 + CO32�C��(3)Ksp[Mg(OH)2]=c(Mg2+)��c2(OH�C)=1.8��10�C3��c2(OH�C)=1.8��10�C11�������c(OH�C)=1��10�C4����pH=10��
���c�������������D�����ܶȷe�����PӋ�㡢�x�ӷ���ʽ�ĕ�����



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�

| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�
| ���| | CaCO3 | MgCO3 | Ca��OH��2 | Mg��OH��2 |
| �ܶȷe | 2.8��10-9 | 6.8��10-6 | 5.5��10-6 | 1.8��10-11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ���W���܈��W���˽��n�˸߶���(�x��4)��2009��2010�W�ꡡ��19�ڡ�����175�� �˽��n�˰�(�x��4) �}�ͣ�058
�ĺ�ˮ����ȡ�V����������@���V����Ҫ��Դ���±������V�^�����漰�ĎN���|���ܶȷe������(j��)�����W��֪�R�ش����І��}��
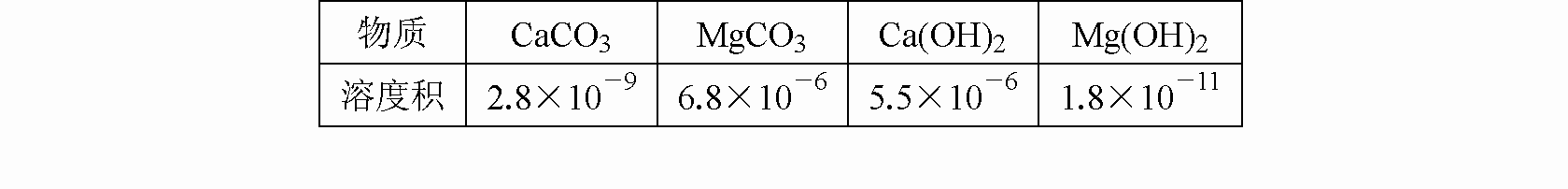
(1)�ĺ�ˮ���ᵽ�V�r���������õ�ؐ��(��Ҫ�ɷ���̼���})�����J���ܷ�ؐ����ĥ�ɷ�ĩ��ֱ��Ͷ�뺣ˮ��ȥ�@�ú����VԪ�صĻ����________(��ܡ���)����������________���������ֱ��Ͷ�룬����ؐ�����̎������Ͷ�뺣ˮ�У�ԇ�������Pؐ��̎���^�����漰�ķ����Ļ��W����ʽ��________��
(2)ijͬ�W�ڌ���җl����ģ�Mԓ���a�^�̣�������ҟoʯ�ң��������ü��A���棬���J��ɷ�õ�Mg(OH)2������________(��ܡ���)���ڼ�ԇ���r���`�����A��Һ���뺣ˮ�У���˼����һ�£����ڵõ��Ļ���wϵ�м����^���ğ��A��Һ�����X�����ܷ�Mg2+�D����Mg(OH)2������________(��ܡ���)��������________��
(3)�����£���֪ij�غ�ˮ���V�x�ӵĝ�Ȟ�1.8��10��3 mol/L��Ҫʹ�V�x�Ӯa����������Һ��pHֵ��͑���________��
�鿴�𰸺ͽ���>>
����ʡ��(li��n)�W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com