
| A. | 物質的量是一個基本物理量,表示物質所含粒子的多少 | |
| B. | 1mol氫中含有2mol氫原子和2mol電子 | |
| C. | 1molH2O的質量等于NA 個H2O 分子的質量總和 | |
| D. | 硫酸的摩爾質量是98g |
分析 A.物質的量是一個基本物理量,表示含有一定數目粒子集體的物理量;
B.物質的量是表示微觀粒子的物理量需要指明微粒種類;
C.1molH2O的質量等于NA個H2O物質的量為1molH2O的質量的總和;
D.摩爾質量的單位為g/mol.
解答 解:A.“物質的量是一個基本物理量”是對的,但物質的量不是表示物質所含“粒子的多少”,而是表示物質所含“一定數目粒子的集合體”的多少,故A錯誤;
B.“1 mol氫”沒有指出具體微粒是什么,故B錯誤;
C.1 mol H2O中含NA個水分子,1 mol H2O的質量就等于NA個H2O分子質量的總和,故C正確;
D.硫酸的摩爾質量為98g/mol,故D錯誤;
故選C.
點評 本題考查了物質的量的應用,題目難度不大,明確摩爾質量與質量、物質的量與微粒數之間的關系為解答關鍵,試題側重基礎知識的考查,有利于提高學生的靈活應用能力.


科目:高中化學 來源:2016-2017學年河北省高二上第一次月考化學試卷(解析版) 題型:選擇題
下列事實不能用勒夏特列原理解釋的是( )
A.向氯水中加食鹽不利于氯氣的溶解
B.棕紅色NO2加壓后顏色先變深后變淺
C.SO2催化氧化成SO3的反應,往往需要使用催化劑
D.高壓有利于合成氨的反應
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省唐山市高二上10月月考化學試卷 (解析版) 題型:選擇題
下列說法中正確的是( )
A.凡是放熱反應都是能自發進行的反應,而吸熱反應都是非自發進行的反應
B.自發反應一定是熵增加的反應,非自發反應一定是熵減小或不變的反應
C.熵增加且放熱的反應一定是自發反應
D.非自發反應在任何條件下都不能發生
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3 Cl2+6 FeI2═2FeCl3+4 FeI3 | B. | Cl2+FeI2═FeCl2+I2 | ||
| C. | Co2O3+6 HCl═2CoCl2+Cl2↑+3H2O | D. | 2Fe3++2I-═2Fe2++I2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| X | Y | ||
| Z | W |
| A. | Y元素的氣態氫化物易液化,是因為其分子間能形成氫鍵 | |
| B. | X元素最高價氧化物分子的比例模型為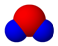 | |
| C. | Z單質與X元素最高價氧化物、Y單質都能反應,體現氧化性 | |
| D. | W的單質在地殼含量豐富,工業上可通過電解它的無水鹽來制備 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cs顯+3價,I、Cl均顯-1價 | |
| B. | 在CsICl2溶液中通入SO2氣體,有硫酸生成 | |
| C. | Cs顯+1價,Cl顯+1價,I顯-3價 | |
| D. | 在CsICl2溶液中通入Cl2,有單質碘生成 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
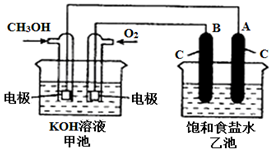 甲醇是一種可再生能源,具有廣泛的開發和應用前景.如圖是用甲醇燃料電池電解飽和食鹽水的裝置示意圖.已知甲池的總反應式為:2CH3OH+3O2+4KOH═2K2CO3+6H2O.
甲醇是一種可再生能源,具有廣泛的開發和應用前景.如圖是用甲醇燃料電池電解飽和食鹽水的裝置示意圖.已知甲池的總反應式為:2CH3OH+3O2+4KOH═2K2CO3+6H2O.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com