
短周期主族元素X 、Y 、Z、W的原子序數依次增大,X原子核外最外層電子數是次外層的2倍,Y的氟化物YF3分子中各原子均達到8電子穩定結構,Z是同周期中原子半徑最大的元素,W的最高正價為+7價.下列說法正確的是( )
A.簡單離子半徑大小順序:rW>rZ>rY
B.元素W的氧化物對應水化物的酸性比Y 的強
C.X與Y形成的原子晶體X3Y4的熔點可能比金剛石高
D.X與W形成的化合物和Z與W形成的化合物的化學鍵類型相同
科目:高中化學 來源:2016屆山西省高三上12月月考化學試卷(解析版) 題型:選擇題
a molNa2O2和b molNaHCO3固體混合后,在密閉容器中加熱到250℃,使其充分反應,當排出氣體為兩種氣體時, a:b不可能為
A.3:4 B.4:5 C.2:3 D.3:2
查看答案和解析>>
科目:高中化學 來源:2015-2016年陜西西藏民族學院附屬中學高一上期末化學卷(解析版) 題型:選擇題
某溫度下將Cl2通入KOH溶液里,反應后得到KCI、KC1O、KC1O3的混合溶液,經測定ClO- 與ClO3-的物質的量濃度之比為11:1,則C12與KOH反應時,被還原的氯元素和被氧化的氯元素的物質的量之比為
A.1:3 B.4:3 C.2:1 D.3:l
查看答案和解析>>
科目:高中化學 來源:2016屆吉林省高三上第四次摸底考試化學試卷(解析版) 題型:選擇題
某同學組裝了如圖所示的電化學裝置,則下列說法正確的是
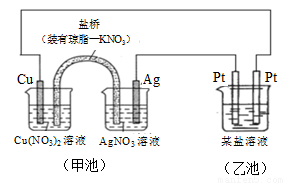
A.圖中甲池為原電池裝置,Cu電極發生還原反應
B.實驗過程中,甲池左側燒杯中NO3- 的濃度不變
C.若甲池中Ag電極質量增加5.4 g時,乙池某電極析出1.6 g金屬,則乙中的某鹽溶液可能是AgNO3溶液
D.若用銅制U形物代替“鹽橋”,工作一段時間后取出U形物稱量,質量會減小
查看答案和解析>>
科目:高中化學 來源:2016屆江蘇省高三上學期第二次質檢化學試卷(解析版) 題型:填空題
目前正在研究和已經使用的儲氫合金有鎂系合金、稀土系合金等。
(1)工業上用電解熔融的無水氯化鎂獲得鎂。其中氯化鎂晶體脫水是關鍵工藝之一,一種氯化鎂晶體脫水的方法是:先將MgCl2·6H2O轉化為MgCl2·NH4C1·nNH3(銨鎂復鹽),然后在700℃脫氨得到無水氯化鎂,脫氨反應的化學方程式為 ____________。
(2)儲氫材料Mg(AlH4)2在110~200℃的反應為:Mg(AlH4)2=MgH2+2Al+3H2↑。生成2.7gAl時,產生的H2在標準狀況下的體積為______________L。
(3)采用球磨法制備Al與LiBH4的復合材料,并對Al-LiBH4體系與水反應產氫的特性進行下列研究:
①下圖為25℃水浴時每克不同配比的Al-LiBH4復合材料與水反應產生H2體積隨時間變化關系圖。由下圖可知,下列說法正確的是_______________(填字母)。

a.25℃時,純鋁與水不反應
b.25℃時,純LiBH4與水反應產生氫氣
c.25℃時,Al-LiBH4復合材料中LiBH4含量越高,1000s內產生氫氣的體積越大
②下圖為25℃和75℃時,Al-LiBH4復合材料[w(LiBH4)=25%]與水反應一定時間后產物的X-射線衍射圖譜(X-射線衍射可用于判斷某晶態物質是否存在,不同晶態物質出現衍射峰的衍射角不同)。

從圖中可知,25℃時Al-LiBH4復合材料中與水完全反應的物質是______________(填化學式)。
(4)儲氫還可借助有機物,如利用環己烷和苯之間的可逆反應來實現脫氫和加氫:

①某溫度下,向恒容密閉容器中加入環己烷,起始濃度為a mol·L-1,平衡時苯的濃度為b mol·L-1,該反應的平衡常數K=_______________。
②一定條件下,下圖裝置可實現有機物的電化學儲氫(忽略其它有機物)。生成目標產物的電極反應式為_______________。

查看答案和解析>>
科目:高中化學 來源:2014-2015學年山西省孝義市高一下學期升級考試化學試卷(解析版) 題型:選擇題
下列實驗能達到目的的是
A.用可見光束照射以區別溶液和膠體
B.用萃取分液的方法出去酒精中的水
C.通過盛有酸性高錳酸鉀的洗氣瓶除去甲烷中的乙烯
D.只滴加氨水鑒別NaCl MgCl2 AlCl3 Na2SO4 四種無色溶液
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山東省滕州市高一上學期12月月考化學試卷(解析版) 題型:選擇題
NA為阿伏加德羅常數,下列敘述正確的是
A.28gCO和N2混合氣體中含有原 子總數為2NA
子總數為2NA
B.在1L1mol.L-1的氨水中含有NA個NH3分子
C.標準狀況下,11.2LNO和11.2LO2混合后氣體分子數為NA
D.1mol Fe分別與足量Cl2 、 S反應,Fe失去電子數都為2NA
查看答案和解析>>
科目:高中化學 來源:2015-2016學年遼寧省高一上學期期末考試化學試卷(解析版) 題型:填空題
氯氣的制取按照傳統的方法,一般采用濃鹽酸與MnO2共熱來制備氯氣,但是這種方法制過程中存在缺陷。某學習小組采用新的方法來制備氯氣并進行性質實驗。
Ⅰ.實驗儀器及藥品:
a.實驗儀器:玻璃片、表面皿(頂部貼有濕潤的藍色石蕊試紙和干燥的石蕊試紙)、膠頭滴管等
b.實驗藥品:KMnO4晶體、濃HCl、KBr溶液、淀粉溶液、KI溶液、FeSO4溶液、NaOH溶液、酚酞、KSCN溶液、AgNO3溶液、濕潤的藍色石蕊試紙和干燥的石蕊試紙。
Ⅱ.實驗方法及圖示:
①在玻璃片上分別滴加KBr溶液、FeSO4溶液、NaOH稀溶液、KI溶液、AgNO3溶液。
②在KI溶液中滴加一滴淀粉溶液
③FeSO4溶液中滴加一滴KSCN溶液
④NaOH稀溶液中滴加一滴酚酞溶液
⑤在以上溶液分布的中心放置一塊KMnO4晶體,然后滴加2-3滴濃鹽酸,迅速蓋上表面皿。并觀察實驗現象。
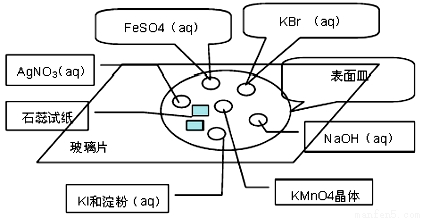
(1)該反應實驗原理:2KMnO4+ 16HCl =2KCl +2MnCl2 +5Cl2↑+ 8H2O
該反應中氧化劑與還原劑的物質的量之比為 ;
(2)實驗時反應一段時間后可以觀察到KBr溶液由無色變為 色,其離子反應方程式為 ;
(3)滴有KSCN溶液的FeSO4溶液呈 色,其離子反應方程式為 、 ;
(4)滴加淀粉溶液的KI溶液呈 色,濕潤的藍色石蕊試紙的變化為 ,干燥的石蕊試紙的變化為 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年陜西省高二上診斷檢測化學試卷(解析版) 題型:選擇題
下圖是電解CuCl2溶液的裝置,其中c、d為石墨電極,則以下有關此電解池的判斷正確的是( )

A.a為負極、b為正極
B.a為陽極、b為陰極
C.電解過程中,d電極質量增加
D.電解過程中,氯離子濃度不變
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com