
【題目】某同學在常溫下設計以下實驗流程探究Na2S2O3的化學性質。下列說法正確的是

A. 實驗①說明Na2S2O3溶液中水電離的c(OH-)=10-8mol·L-1
B. Na2S2O3溶液pH=8的原因用離子方程式表示為S2O32-+2H2O![]() H2S2O3+2OH-
H2S2O3+2OH-
C. 生成的沉淀B可能是BaSO3或BaSO4,要進一步確認還需加入稀硝酸驗證
D. 實驗②說明Na2S2O3具有還原性
【答案】D
【解析】
根據鹽類的水解的規律和氧化還原反應的規律進行分析解答。
A.Na2S2O3的溶液pH=8,說明S2O32-水解,水的電離受到了促進,由水電離的c(OH-)![]() 10-6 mol·L-1,故A錯誤;
10-6 mol·L-1,故A錯誤;
B.S2O32-水解是分步進行的,S2O32-+H2O![]() HS2O3-+OH-,故B錯誤;
HS2O3-+OH-,故B錯誤;
C.兩個錯誤點(1)氯水足量,沉淀中不可能有BaSO3(2)BaSO3與硝酸發生氧化還原反應生成BaSO4,不能加硝酸驗證,故C錯誤;
D.S2O32-+5H2O+4Cl2+2Ba2+=2BaSO4↓+8Cl-+10H+ ,S元素的化合價升高,說明Na2S2O3具有還原性,故D選項正確;
正確答案:D。


 暑假銜接培優教材浙江工商大學出版社系列答案
暑假銜接培優教材浙江工商大學出版社系列答案 欣語文化快樂暑假沈陽出版社系列答案
欣語文化快樂暑假沈陽出版社系列答案科目:高中化學 來源: 題型:
【題目】金屬銦主要用于生產液晶顯示器和平板屏幕。從LCD廢料(主要成分是含銦、錫的氧化物)中回收銦的工藝流程如下:
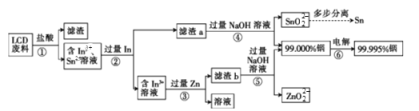
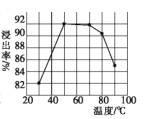
(1)步驟①中用鹽酸酸浸時浸出率隨溫度變化關系如圖所示,則最適宜的溫度是___________,溫度升高浸出率下降的原因是__________
(2)酸浸時銦的氧化物轉化成In3+的離子方程式是__________
(3)提純粗銦的方法和銅的精煉原理相似,則粗銦為__________(填“陰極”或“陽極”),寫出陰極的電極反應式: ______________________________
(4)步驟④中所發生氧化還原反應的氧化劑是__________(填化學式),步驟⑤中所發生氧化還原反應的氧化產物與還原產物系數之比是__________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氟化鋰(LiF)難溶于水,可用于核工業、光學玻璃制造等。以透鋰長石(含Li2O、Al2O3、SiO2)為原料制備氟化鋰的工藝流程如下:
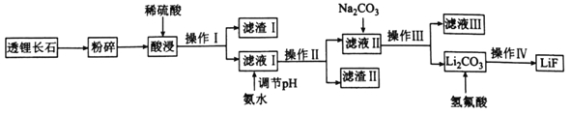
回答下列問題:
(1)濾液I中含有的金屬離子有________,濾渣I的一種用途是________________。
(2)濾渣Ⅱ是目前應用最廣泛的無機阻燃劑,寫出生成濾渣Ⅱ的離子方程式:________________。常溫下,若向濾液I中滴加氨水調節pH=5時,溶液中c(Al3+)=________mol·L-1,則溶液中A13+________(填“是”或“否”)沉淀完全(已知Ksp[Al(OH)3]=2.0×10-33,且溶液中的離子濃度小于1.0×10-5mol·L-1時沉淀完全)。
(3)操作Ⅳ包括________________、________________和干燥。
(4)寫出Li2CO3與氫氟酸反應的化學方程式:________________________,該反應不能在玻璃容器中進行的原因是________________________(用化學方程式表示)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】石棉是過去常用的保溫、絕熱、防火材料,但現已確認為致癌物質,并正在開發它的代用品。石棉的組成可用化學式CaMg3(SiO3)4。表示,其中Si的化合價是 ( )
A. +2 B. -2 C. +4 D. -4
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用吸附了H2的碳納米管等材料制作的二次電池的原理如圖所示。下列說法正確的是( )

A. 放電時,負極的電極反應為:H2-2e-=2H+
B. 充電時,陽極的電極反應為:Ni(OH)2+OH--e-=NiO(OH)+H2O
C. 充電時,將電池的碳電極與外電源的正極相連
D. 放電時,OH-向鎳電極作定向移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以硅孔雀石[主要成分為CuCO3·Cu(OH)2、CuSiO3·2H2O,含SiO2、FeCO3、Fe2O3等雜質]為原料制備CuCl2的工藝流程如下:

已知: SOCl2+H2O![]() SO2↑+2HCl↑,下列說法不正確的是
SO2↑+2HCl↑,下列說法不正確的是
A. “酸浸” 時應該用鹽酸溶解硅孔雀石粉
B. “氧化”時發生反應的離子方程式為:Cl2+2Fe2+![]() 2Fe3++2Cl-
2Fe3++2Cl-
C. “調pH”時,pH需控制在堿性區域,保證鐵元素全部以Fe(OH)3形式除去
D. “加熱脫水”時,加入SOCl2的目的是生成的HCl抑制CuCl2的水解
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學反應中,反應混合物A、B、C的物質的量濃度(c)與時間(t)關系如下所表示

下列說法錯誤的是( )
A. 該反應的化學方程式為2A![]() 4B+C B. 逆反應是放熱反應
4B+C B. 逆反應是放熱反應
C. 4min時A的轉化率約為31% D. 4~6min時,反應處于動態平衡
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在2A(g)+B(g)![]() 3C(g)+4D(g)反應中,表示該反應的反應速率最快的是
3C(g)+4D(g)反應中,表示該反應的反應速率最快的是
A. v(A)=0.5 mol/(L·min) B. v(B)=0.1 mol/(L·s)
C. v(C)=0.8 mol/(L·min) D. v(D)=1 mol/(L·min)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com