
【題目】向2L密閉容器中加入一定量的固體A和氣體B,發生反應A(s)+2B(g)![]() D(g)+E(g)△H=QkJ·mol-1。在T1℃時,反應進行到不同時間測得各物質的物質的量如表:
D(g)+E(g)△H=QkJ·mol-1。在T1℃時,反應進行到不同時間測得各物質的物質的量如表:
物質的量(mol) 時間(min) | 0 | 10 | 20 | 30 | 40 | 50 |
B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
(1)T℃時,該反應的平衡常數K=___________。
(2)30min后,只改變某一條件,反應重新達到平衡,根據表中的數據判斷改變的條件可能是______(填字母編號)。
a.通入一定量的B
b.加入一定量的固體A
c.適當縮小容器的體積
d.升高反應體系溫度
e.同時加入0.2mol B、0.1molD、0.1mol E
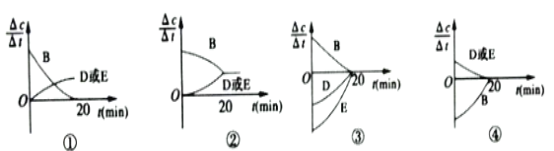
(3)對于該反應,用各物質的反應速率與時間的關系曲線表示如下,示意圖中的___________(填序號)正確。
(4)容器的體積和溫度T1℃不變,向該容器中加入1.60molB、0.20molD、0.20molE和0.4molA,達到平衡后,與表格中20分鐘時各物質的濃度完全相同,投入固體A的物質的量n的取值范圍是___________。
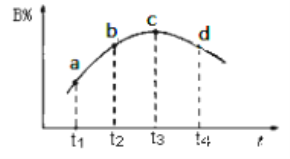
(5)若該密閉容器絕熱,實驗測得B的轉化率隨溫度變化如圖所示。由圖可知,Q_________0(填“大于”或“小于),c點v正__________v逆(填“大于”、“小于”或“等于”)。
【答案】0.25 ae ④ n>0.3 小于 等于
【解析】
(1)根據表格中的數據,在20min反應達到平衡,A(s)+2B(g)![]() D(g)+E(g)
D(g)+E(g)
起始(mol) 2.00 0 0
變化(mol) 1.00 0.50 0.50
平衡(mol) 1.00 0.50 0.50
根據平衡常數的定義,K=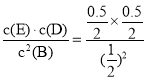 =0.25;
=0.25;
(2)a、通入一定量的B,平衡向正反應方向進行,BDE都增大,故a符合題意;
b、A為固體,濃度視為常數,增加固體A,平衡不移動,故b不符合題意;
c、反應前后氣體系數之和相等,縮小容器的體積,氣體壓強增大,平衡不移動,故c不符合題意;
d、改變溫度,平衡發生移動,BDE不會都增大,故d不符合題意;
e、同時加入0.2molB、0.1molD、0.1molE,相當于在原來的基礎增大壓強,平衡不移動,物質的量都增大,故e符合題意;
答案選ae;
(3)①化學平衡為動態平衡,即B的反應速率不能為0,故①不符合題意;
②B的系數與D和E系數不相等,即達到平衡時B的速率與D、E的反應速率不能相等,故②不符合題意;
③D和E變化速率相同,故③不符合題意;
④DE速率相同,圖像表示逆向進行,B的反應速率增大,DE反應速率減小,故④符合題意;
答案選④;
(4)由提供的數據可知,與表格中20min時各物質的濃度完全相同時,生成D、E的量為(0.5-0.2)mol=0.3mol,A的量要夠轉化,A的量不小于0.3mol,即n>0.3mol;
(5)根據圖像,c點達到平衡,隨著溫度的升高,B的轉化率減小,根據勒夏特列原理,正反應方向為放熱反應,即Q<0,c點為平衡,即正反應速率等于逆反應速率。


 每日10分鐘口算心算速算天天練系列答案
每日10分鐘口算心算速算天天練系列答案科目:高中化學 來源: 題型:
【題目】C1O2是常用的自來水消毒劑。
I.已知實驗室可用亞氯酸鈉固體與氯氣反應制備ClO2:2NaClO2+C12 =2C1O2+2NaCl,裝置如下圖所示:

(1)圓底燒瓶內發生反應的化學方程式是:__________。
(2)已知常溫常壓下,ClO2和Cl2是氣體,在下列溶劑中溶解性如下表所示:
ClO2 | Cl2 | |
水 | 極易溶于水 | 溶 |
CCl4 | 難溶 | 溶 |
B、C、E裝置中的試劑依次是_________(填序號)。
a.NaOH溶液 b.濃硫酸 c.飽和食鹽水 d.CCl4 e.飽和石灰水
II.使用C1O2在給自來水消毒的過程中會產生有害的副產物亞氯酸根(ClO2-),可用Fe2+將其去除。已知ClO2-與Fe2+在pH=5~7的條件下能快速反應,最終形成紅褐色沉淀,而ClO2-則被還原成Cl-。
(3)Fe2+消除ClO2-的離子方程式為_______。
(4)實際向自來水中加入Fe2+的量要高于理論值,原因是(結合離子方程式解釋)___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】四元軸烯t,苯乙烯b及立方烷c的結構簡式如下,下列說法正確的是
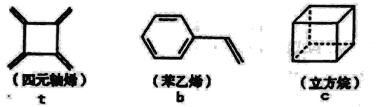
A.b的同分異構體只有t和c兩種B.t和b能使酸性KMnO4溶液褪色而c不能
C.t、b、c的二氯代物均只有三種D.b中所有原子-定不在同-個平面上
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,用0.0500 mol·L-1H2C2O4溶液滴定 25.00 mL0.l000mol·L-1NaOH溶液所得滴定曲線如圖。下列說法正確的是()
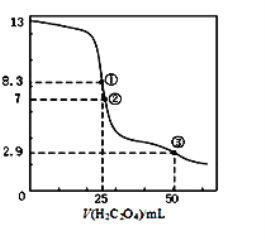
A.點①所示溶液中:c(H+)+c(H2C2O4)+c(HC2O4-)=c(OH-)
B.點②所示溶液中:c(HC2O4-)+c(C2O42-)=c(Na+)
C.點③所示溶液中:c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
D.滴定過程中可能出現:c(Na+)>c(C2O42-)=c(HC2O4-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.硫酸工業中廢渣稱為硫酸渣,其成分為SiO2、Fe2O3、Al2O3、MaO。某學習小組的同學設計以下方案,進行硫酸渣中金屬元素的提取實驗。

已知:溶液pH=3.7時,Fe3+已經沉淀完全;一水合氨其飽和溶液中c(OH-)約為1×10-3mol·L-1。
(1)寫出A與氫氧化鈉溶液反應的離子方程式:______________________________。
(2)上述流程中兩次使用試劑①,推測試劑①應該是____________(填字母)
A.氫氧化鈉 B.氧化鋁 C.氨水 D.水
(3)H中溶質是______________。(填化學式)
(4)溶液D到固體E過程中需要控制溶液pH=13,如果pH過小,可能導致的后果是______________ 。
(4)計算溶液F中c(Mg2+)=______________ (25℃時,氫氧化鎂的Ksp=5.6×10-12)
II.某化學興趣小組用下圖所示裝置進行電化學原理的實驗探究。
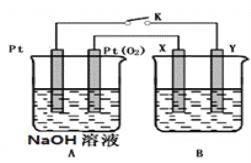
(1)A裝置為乙醇燃料電池,若X、Y均是銅,電解質溶液為NaOH溶液,電池工作一段時間,X極附近生成磚紅色沉淀,查閱資料得知是Cu2O,試寫出該電極發生的電極反應式為________________________。
(2)若B電池的電解質溶液為500mL1.0mol/L的NaCl溶液,X、Y皆為惰性電極,當電池工作一段時間斷開電源K,Y電極有560mL(標準狀況)無色氣體生成(假設電極產生氣體完全溢出,溶液體積不變)此時B電池溶液的pH=____________,要是該溶液恢復到原來的狀態,需加入____________(填物質并注明物質的量)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)由N2、NO、CO2組成的混合氣體中,三種成分的體積分數之比為1:2:1,則三種成分的質量比為________。
(2)等質量的鈉和鎂分別與足量的稀硫酸反應,放出氣體的體積(同溫同壓)之比為________。
(3)同溫同壓下,某容器充滿CO2重122 g,充滿NO氣體重115 g,現充滿某氣體B重123 g,則該氣體的相對分子質量為_____。
(4)有15 g A物質和10.5 g B物質恰好完全反應生成7.2 g C物質、1.8 g D物質和0.3 mol E物質,則E物質的摩爾質量是_____g·mol-1。
(5)標準狀況下,10 mL N2氣體恰好與30 mL H2完全反應生成20 mL氣體A,則A的分子式為_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值。下列說法正確的是( )
A.56gN2與CO的混合物中原子總數是4NA
B.0.1mol/L的硫酸溶液中含H+的數目為0.2 NA
C.3mol單質Fe完全燃燒轉變為Fe3O4,Fe得到8NA個電子
D.標準狀況下,22.4LH2O所含的氧原子數目為NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)甲醇一空氣燃料電池(DMFC)是一種高效能、輕污染的車載電池,其工作原理如圖甲所示,該電池中正極的電極反應式為_____。
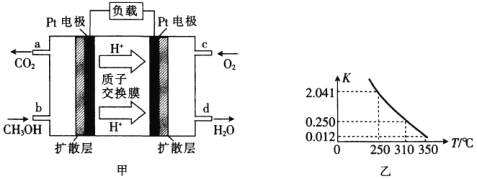
(2)工業上合成甲醇一般采用下列反應:![]() ,
,![]() ,圖乙是該反應在不同溫度下的化學平衡常數(K):
,圖乙是該反應在不同溫度下的化學平衡常數(K):
①由圖中數據判斷a_______0(填“>”“=”或“<”)。
②某溫度下,將2molCO和6molH2充入2L的恒容密閉容器中,充分反應達到平衡后,測得c(CO)=0.5mol·L-1,則此時的溫度為________℃。
(3)T℃時,在恒容密閉容器中發生反應:![]() ,各物質的濃度變化如圖丙所示:
,各物質的濃度變化如圖丙所示:
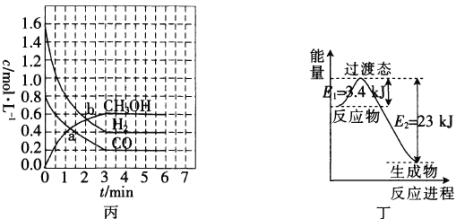
①反應從0min到3min之間,CH3OH的反應速率為________________。
②CO在0~1min和1~3min時平均反應速率[平均反應速率分別以v(0~1),v(1~3)表示]的大小為_____________________________。
(4)目前工業上有一種方法是用CO2和H2在230℃、催化劑條件下轉化生成甲醇蒸氣和水蒸氣。圖丁表示恒壓容器中0.5molCO2和1.5molH2反應時轉化率達80%的能量變化示意圖。寫出該反應的熱化學方程式:_________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】元素周期表中釕(Ru)與鐵相鄰位于鐵的下一周期,某釕光敏太陽能電池的工作原理如下圖所示,圖中RuII*表示激發態。下列說法正確的是

A. 電池工作時,直接將太陽能轉化為電能
B. 理論上,n(被還原的I3-):n(被氧化的Ru II*)=1:2
C. 在周期表中,釕位于第五周期第ⅧB族
D. 電池工作時,正極的電極反應式為Ru3++e-=Ru2+
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com