
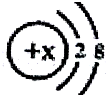 當x=8時,該粒子符號為O2-;當x=11時,該粒子符號為Na+;當x=13時,寫出該粒子的硝酸鹽的化學式為:Al(NO3)3.
當x=8時,該粒子符號為O2-;當x=11時,該粒子符號為Na+;當x=13時,寫出該粒子的硝酸鹽的化學式為:Al(NO3)3.分析 (1)根據當質子數=核外電子數,為原子;當質子數>核外電子數,為陽離子;當質子數<核外電子數,為陰離子;
(2)向15g蒸餾水加入無水硫酸銅粉末,充分攪拌并過濾,得到一定質量的藍色五水合硫酸銅晶體和8.4g濾液,此溫度下無水硫酸銅的溶解度為40g,可以計算出濾液中硫酸銅的質量;
(3)根據難溶的物質在一定條件下可轉化成更難溶的物質來分析化學反應.
解答 解:(1)某簡單粒子的結構示意圖可表示為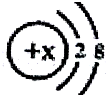 :當X=8時,質子數=8,核外電子數=10,質子數<核外電子數,為氧離子,粒子的符號為O2-;
:當X=8時,質子數=8,核外電子數=10,質子數<核外電子數,為氧離子,粒子的符號為O2-;
當X=11時,質子數=11>核外電子數=10,為鈉離子,其離子符號為:Na+;
當X=13時,質子數=13,核外電子數=10,質子數>核外電子數,為鋁離子;與硝酸根化合形成的化合物為硝酸鋁,鋁元素顯+3價,硝酸根顯-1價,其化學式為:Al(NO3)3,
故答為:O2-;Na+;Al(NO3)3;
(2)向15g蒸餾水加入無水硫酸銅粉末,充分攪拌并過濾,得到一定質量的藍色五水合硫酸銅晶體和8.4g濾液,此溫度下無水硫酸銅的溶解度為40g,設濾液中含硫酸銅的質量為x,則 $\frac{40}{100+40}=\frac{x}{8.4}$,x=2.4g
則濾液中含水的質量為8.4g-2.4g=6g,
故五水合硫酸銅晶體(CuSO4•5H2O)中含水的質量為15g-6g=9g,則含硫酸銅的質量為9g×=16g,
此無水硫酸銅的質量是2.4g+16g=18.4g,
故答案為:18.4g;
(3)由難溶的物質在一定條件下可轉化成更難溶的物質,在成有氯化銀沉淀的試管中加入碘化鉀溶液,振蕩后可觀察到白色沉淀逐漸變為黃色沉淀,是因為AgI比AgCl更難溶,其反應為AgCl+KI═AgI↓+KCl,
故答案為:AgCl+KI═AgI↓+KCl,AgI比AgCl更難溶.
點評 本題考查學生利用信息來判斷反應的發生,掌握五水合硫酸銅晶體的成分、溶解度的含義,抓住習題中的信息利用物質的溶解性來分析反應是解答的關鍵.


 優加精卷系列答案
優加精卷系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
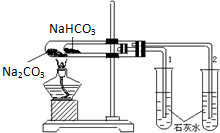 實驗室利用如圖所示裝置進行Na2CO3和NaHCO3熱穩定性對比實驗.請回答:
實驗室利用如圖所示裝置進行Na2CO3和NaHCO3熱穩定性對比實驗.請回答:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A | B | C | D | |
| 正極 | Zn | Ag | C | Cu |
| 負極 | Cu | Cu | Zn | Zn |
| 電解質溶液 | CuCl2 | H2SO4 | CuSO4 | FeCl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
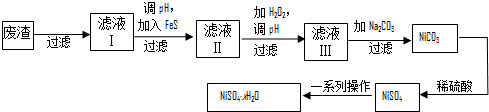
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2O2加入H218O中:2Na2O2+2H218O=4Na++4OH-+18O2↑ | |
| B. | 0.01mol/L NH4Al(SO4)2溶液與0.02mol/L Ba(OH)2溶液等體積混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3•H2O | |
| C. | 向Ca(HCO3)2溶液中加入澄清石灰水:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| D. | 向FeI2溶液中通入少量Cl2:2Fe2++Cl2=2Fe3++2Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com