
【題目】在某溫度時,密閉容器中進行反應:X(g)+4Y(g)![]() 2Z(g)+3R(g),其中X、Y、Z、R的起始濃度依次為0.1、0.4、0.2、0.3(單位均為mol·L-1,下同),則達平衡時,各物質的濃度不可能的是
2Z(g)+3R(g),其中X、Y、Z、R的起始濃度依次為0.1、0.4、0.2、0.3(單位均為mol·L-1,下同),則達平衡時,各物質的濃度不可能的是
A.c(X)=0.15B.c(Z)=0.3C.c(Y)=0.9D.c(R)=0.6
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化學 來源: 題型:
【題目】在一密閉容器中,反應:aA(g) ![]() bB(g) 達平衡后,保持溫度不變,將容器體積增大一倍,當達到新的平衡時,B的濃度是原來的60%,下列說法正確的是( )
bB(g) 達平衡后,保持溫度不變,將容器體積增大一倍,當達到新的平衡時,B的濃度是原來的60%,下列說法正確的是( )
A. 平衡向逆反應方向移動了B. 物質A的轉化率減少了
C. 物質B的質量分數增加了D. a>b
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗測得0.5 mol·L1CH3COONa溶液、0.5 mol·L1 CuSO4溶液以及H2O的pH隨溫度變化的曲線如圖所示。下列說法正確的是

A. 隨溫度升高,純水中c(H+)>c(OH)
B. 隨溫度升高,CH3COONa溶液的c(OH)減小
C. 隨溫度升高,CuSO4溶液的pH變化是Kw改變與水解平衡移動共同作用的結果
D. 隨溫度升高,CH3COONa溶液和CuSO4溶液的pH均降低,是因為CH3COO、Cu2+水解平衡移動方向不同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】芬太尼類似物L具有鎮痛作用。它的合成方法如下:

已知:
I、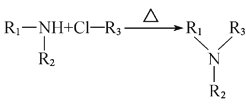 +HCl
+HCl
II、![]()
![]()
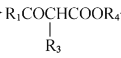 +R2OH;
+R2OH;
III、 (
(![]() 為氫或烴基)
為氫或烴基)
回答下列問題:
(1)A是一種烯烴,化學名稱為______,其分子中最多有__________個原子共面。
(2) B中官能團的名稱為_____、_____。②的反應類型為________
(3)③的化學方程式為________
(4)碳原子上連有4個不同的原子或基團時,該碳稱為手性碳。指出F的結構簡式中手性碳原子并用星號(*)標出F中的手性碳________。G的結構簡式為________。
(5)已知④有一定的反應限度,反應進行時加入吡啶(一種有機堿),其作用是________。
(6)參照上述合成路線,寫出以環已烯(![]() )和乙醇為起始原料經三步制備化合物
)和乙醇為起始原料經三步制備化合物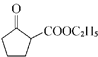 的合成路線________。
的合成路線________。
(已知:![]() 其他試劑任選)
其他試劑任選)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按要求填空。
(1)有下列各組物質:
(A)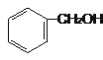 和
和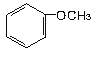 ;(B)CH2=CH-CH=CH2和CH3-CH2-C=CH;(C)
;(B)CH2=CH-CH=CH2和CH3-CH2-C=CH;(C) ;(D)
;(D)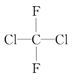 和
和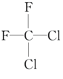 ;(E)甲烷和新戊烷
;(E)甲烷和新戊烷
其中____組兩物質互為同系物;_______組兩物質互為同分異構體;______組兩物質互為同一物質;A組第一個物質的名稱是:_________。
(2)寫出1,3﹣丁二烯與Br2的CCl4溶液發生1,4﹣加成后的產物的結構簡式:___________。
(3)寫出由甲苯生成TNT(2,4,6﹣三硝基甲苯)的方程式:____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖電化學原理可用于治理水中硝酸鹽的污染,下列說法不正確的是
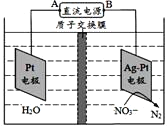
A. A為電源正極
B. 在Pt電極上發生氧化反應
C. 陰極電極反應式為2NO3-+6H2O+10e-=N2+12OH
D. 質子從Pt電極移向Ag-Pt電極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗小組依據甲烷燃燒的反應原理,設計如圖a所示的電池裝置:
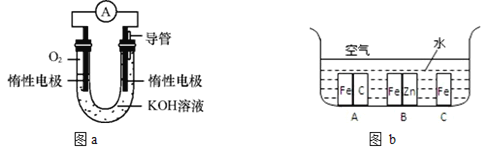
(1)該電池的能量轉化形式為____________。
(2)該電池正極的電極反應為____________。
(3)工作一段時間后,測得溶液的pH______,該電池總反應的化學方程式為_________。
(4)在生產生活中,金屬腐蝕所帶來的損失非常嚴重,所以防止金屬腐蝕已經成為科學研究和技術領域的重大問題。興趣小組的同學在實驗室對金屬腐蝕進行了探究。如圖b所示,鐵處于A、B、C三種不同的環境中,鐵被腐蝕的速率由大到小的順序是(填序號)_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國科研人員提出了由CO2和CH4轉化為高附加值產品CH3COOH的催化反應歷程。該歷程示意圖如下。

下列說法不正確的是
A. 生成CH3COOH總反應的原子利用率為100%
B. CH4→CH3COOH過程中,有C―H鍵發生斷裂
C. ①→②放出能量并形成了C―C鍵
D. 該催化劑可有效提高反應物的平衡轉化率
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】無色的混合氣體甲,可能含NO、CO2、NO2、NH3、N2中的幾種,將100mL甲氣體依次通過下圖實驗的處理,結果得到酸性溶液,幾乎無氣體剩余,則甲氣體的組成為
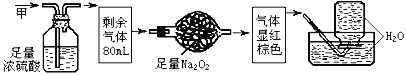
A.NH3、NO2、N2B.NH3、NO、CO2
C.NH3、NO2、CO2D.NO、CO2、N2
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com