
【題目】室溫下,下列各組離子在指定溶液中一定能大量共存的是
①pH=0的溶液:Na+、I-、NO3-、SO42-、
②pH=12的溶液中:![]() 、Na+、NO3-、S2-、
、Na+、NO3-、S2-、![]()
③水電離的H+濃度c(H+)=10-12 mol·L-1的溶液中:Cl-、![]() 、
、![]() 、
、![]() 、
、![]()
④加入Mg能放出H2的溶液中:Mg2+、![]() 、Cl-、K+、
、Cl-、K+、![]()
⑤使石蕊變紅的溶液中:Fe2+、![]() 、Na+、
、Na+、![]()
⑥中性溶液中:Fe3+、Al3+、![]() 、Cl-、
、Cl-、
A.②④B.只有②C.①②⑤D.①②⑥
【答案】A
【解析】
①酸性環境下,硝酸根離子會與碘離子發生氧化還原反應,故①錯誤;
②pH=12的溶液中,CO32-、Na+、NO3-、S2-、SO32-可以共存,故②正確;
③水電離的H+濃度c(H+)=10-12 mol·L-1的溶液中可能為酸性溶液,也可能為堿性溶液,CO32-、SO32-在酸性情況下生成CO2、SO2;NH4+在堿性環境下生成一水合氨,故③錯誤;
④加入Mg能放出H2的溶液,為酸性溶液,Mg2+、NH4+、Cl-、K+、SO42-可以共存,故④正確;
⑤使石蕊變紅的溶液,為酸性溶液,Fe2+與NO3-發生氧化還原反應,故⑤錯誤;
⑥Al3+、Fe3+會水解使溶液呈酸性,在中性溶液中不能大量存在,故⑥錯誤;
因此②④正確,答案選A。


科目:高中化學 來源: 題型:
【題目】已知水的電離方程式是H2O![]() H++ OH-。下列敘述正確的是( )
H++ OH-。下列敘述正確的是( )
A.升高溫度,KW增大,pH不變
B.向水中加入少量硫酸,c(H+)增大,KW不變
C.向水中加入氨水,平衡向逆反應方向移動,c(OH-)降低
D.向水中加入少量固體CH3COONa,平衡向逆反應方向移動,c(H+)降低
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋁是地殼中含量最多的金屬元素,它性能穩定,供應充足,鋁—空氣電池具有能量密度高、工作原理簡單、成本低、無污染等優點。鋁—空氣電池工作原理示意圖如圖:
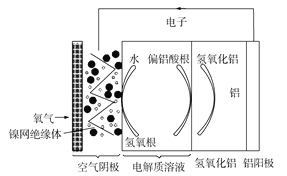
下列說法錯誤的是( )
A.若是堿性電解質溶液中,則電池反應的離子方程式為:4Al+3O2+4OH=4![]() +2H2O
+2H2O
B.若是中性電解質溶液中,則電池反應的方程式為:4Al+3O2+6H2O=4Al(OH)3
C.如果鋁電極純度不高,在堿性電解質溶液中會產生氫氣
D.若用該電池電解氯化鈉溶液(石墨作電極),當負極減少5.4g時,陽極產生6.72L氣體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定條件下,對于A2(g)+3B2(g)![]() 2AB3(g)反應來說,下列所表示的化學反應速率中最大的是
2AB3(g)反應來說,下列所表示的化學反應速率中最大的是
A. v(A2)=0.8mol·L-1·s-1 B. v(A2)=40mol·L-1·min-1
C. v(AB3)=1.0mol·L-1·s-1 D. v(B2)=1.2mol·L-1·s-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關說法不正確的是( )
A. 水合銅離子的模型如圖所示,1個水合銅離子中有4個配位鍵
水合銅離子的模型如圖所示,1個水合銅離子中有4個配位鍵
B. CaF2晶體的晶胞如圖所示,每個CaF2晶胞平均占有4個Ca2+
CaF2晶體的晶胞如圖所示,每個CaF2晶胞平均占有4個Ca2+
C. H原子的電子云圖如圖所示,H原子核外的大多數電子在原子核附近運動
H原子的電子云圖如圖所示,H原子核外的大多數電子在原子核附近運動
D. 金屬Ag的原子堆積模型如圖所示,該金屬晶體為最密堆積,每個Ag原子的配位數均為12
金屬Ag的原子堆積模型如圖所示,該金屬晶體為最密堆積,每個Ag原子的配位數均為12
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】北京大學和中國科學院的化學工作者合作,已成功研制出堿金屬與C60形成的石墨夾層離子化合物。將石墨置于熔融的鉀或氣態的鉀中,石墨吸收鉀而形成稱為鉀石墨的物質,其組成可以是C8K、C12K、C24K、C36K、C48K、C60K等等。在鉀石墨中,鉀原子把價電子交給石墨層,但在遇到與金屬鉀易反應的其他物質時還會收回。下列分析中正確的是( )

A. 題干中所舉出的6種鉀石墨,屬于同素異形體
B. 若某鉀石墨的原于分布如圖一所示,則它所表示的是C24K
C. 若某鉀石墨的原子分布如圖二所示,則它所表示的是C12K
D. 另有一種灰色的鉀石墨C32K,其中K的分布也類似圖中的中心六邊形,則最近兩個K原子之間的距離為石墨鍵長的4![]() 倍
倍
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定條件下,在密閉容器中,發生可逆反應2NO2(g) ![]() 2NO(g) +O2(g),達到平衡狀態的標志是:
2NO(g) +O2(g),達到平衡狀態的標志是:
A.單位時間生成n mol O2,同時生成2n mol NO
B.用NO2、NO、O2表示反應速率之比為2:2:1的狀態
C.NO2、NO、O2的物質的量之比為2:2:1的狀態
D.混合氣體的顏色不再改變的狀態
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在t℃下,某反應達到平衡,平衡常數K=c(NO)c(SO3)/c(NO2)c(SO2)。恒容時,溫度升高,NO濃度減小。下列說法正確的是( )
A.該反應的焓變為正值B.恒溫下增大壓強,反應體系的顏色加深
C.升高溫度,逆反應速率減小D.該反應化學方程式為NO+SO3![]() NO2+SO2
NO2+SO2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,向Na2CO3溶液中滴入鹽酸,混合溶液的pH與離子濃度變化的關系如圖所示。已知:lgX=lg 或lg
或lg ,下列敘述正確的是( )
,下列敘述正確的是( )

A.曲線m表示pH與lg 的變化關系
的變化關系
B.當溶液呈中性時,c(Na+)=c(HCO3-)+2c(CO32-)
C.Ka1(H2CO3)=1.0×10-6.4
D.25℃時,CO32-+H2OHCO3-+OH-的水解常數為1.0×10-7.6
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com