
【題目】在反應X+2Y=R+2M中,已知R和M的摩爾質量之比為22:9,當1.6 gX與Y完全反應后,生成4.4 gR,則 在此反應中,Y與R的化學式量之比為:
A.32: 18 B.16:11 C.8:11 D.16:9
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】對于反應X(g)+Y(s)=2Z(g) ,下列條件不能改變化學反應速率的是
A. 升高溫度 B. 加入催化劑 C. 再加入一定量的Y D. 擴大容器體積
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于反應A(g)+3B(g)![]() 2C(g),下列各數據表示不同條件下的反應速率,其中反應進行得最快的是( )
2C(g),下列各數據表示不同條件下的反應速率,其中反應進行得最快的是( )
A.v(A)=0.01 mol/(Ls) B.v(C)=1.0mol/(Lmin)
C.v(B)=0.60mol/(Lmin) D.v(B)=0.04 mol/(Ls)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在25℃時,2L的密閉容器中A、B、C三種氣體的初始濃度和平衡濃度如下表:
物質 | A | B | C |
初始濃度/mol·L-1 | 1.0 | 2.0 | 0 |
2min時,平衡濃度/mol·L-1 | 0.4 | 0.2 | 1.2 |
請填寫下列空白:
(1)該反應方程式可表示為: ;反應達平衡時,A的轉化率為___________。
(2)從反應開始到達化學平衡,生成C的平均反應速率為 ;25℃時,反應的化學平衡常數K值(數值)為_____________。
(3)能判斷該反應已達到化學平衡狀態的依據是__________。
a.容器內壓強不變
b.混合氣體的密度不變
c.3v正(B)=2v逆(C)
d.c(A)=c(C)
e.混合氣體的平均相對分子質量不變
(4)若已知該反應為放熱反應,下圖表示由于條件改變而引起反應速度和化學平衡的變化情況:
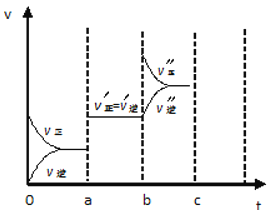
a 點時改變的條件可能是 ;b點時改變的條件可能是 。
(5)如果上述反應起始是按“1 mol A+3 mol B”充入,達平衡時C的濃度為a mol/L;維持容器體積和溫度不變,按下列方法改變起始物質的量,達到平衡時C的濃度仍為a mol/L的是 (填序號)
①2 mol A+6 mol B ②2mol C ③4mol C ④0.5 mol A+1.5mol B+1 mol C
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【化學一選修3:物質結構與性質】X、Y、Z、W四種元素的部分信息如下表所示。
元素 | X | Y | Z | W |
相關 信息 | 短周期元素,最高化合價為 +7價 | 基態原子中,電子占據的最高能層符號為L,最高 能級上只有兩個自旋方向相同的電子 | 核外電子共有15種運動狀態 | 能與X形成兩種常見化合物WX2、WX3,酚遇WX3溶液能發生顯色反應 |
回答下列問題:
(1) W的基態原子電子排布式為____, X、Y、Z三種元素電負性由大到小的順序為___(用具體的元素符號填寫)。
(2)化合物YX4、ZX3、ZX5 (氣態或液態時)中,中心原子的軌道類型不是sp3雜化的是________(填化學式,下同),分子構型是正四面體的是______, 屬于極性分子的是____。
(3)已知WX3的熔點:306℃,沸點:319℃,則WX3的晶體類型為____,Y與氫元素能形成YnH2n+2 (n為正整數)的一系列物質,這一系列物質沸點的變化規律以及影響的因素是______________。
(4)Z可形成多種含氧酸,如H3ZO4、HZO3、H3ZO3等,其中酸性最強的是______(填化學式)。
(5)W元素的單質晶體在不同溫度下有兩種堆積方式,晶胞分別如下圖所示。在面心立方晶胞中W原子的配位數為___;若W的原子半徑為r cm,阿伏加德羅常數為NA,則其體心立方晶體的密度可表示為_____gcm-3。
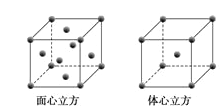
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在容積可變的密閉容器中存在如下反應:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0,下列分析中不正確的是( )
CO2(g)+H2(g) ΔH<0,下列分析中不正確的是( )

A. 圖Ⅰ研究的是t0時升高溫度對反應速率的影響
B. 圖Ⅱ研究的是t0時增大壓強(縮小容積)或使用催化劑對反應速率的影響
C. 圖Ⅲ研究的是催化劑對化學平衡的影響,且甲使用了催化劑
D. 圖Ⅲ研究的是溫度對化學平衡的影響,且乙的溫度較高
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】發展以煤制乙烯、丙烯、丁烯等低碳烯烴,部分替代石油化工產品的道路是我國保障能源安全戰略的重要措施。間接法是先由煤制合成氣(組成為H2、CO和少最的CO2)制備甲醇或二甲醚(CH3OCH3),其主要過程包括以下四個反應:
甲醇合成反應:
①CO(g)+2H2(g)![]() CH3OH(g) △H1=-90.1 kJmol-1
CH3OH(g) △H1=-90.1 kJmol-1
②CO2(g)+3H2(g)![]() CH3OH(g) +H2O(g) △H2=-49.0kJmol-1
CH3OH(g) +H2O(g) △H2=-49.0kJmol-1
水煤氣變換反應:
③CO(g)+ H2O(g)![]() CO2(g)+ H2(g) △H3=-41.1kJmol-1
CO2(g)+ H2(g) △H3=-41.1kJmol-1
二甲醚合成反應:
④2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H4=-24.5kJmol-1
CH3OCH3(g)+H2O(g) △H4=-24.5kJmol-1
回答下列問題:
(1)分析上述反應(均可逆),發生反應④對于CO轉化率的影響是_______(填“增大”、“減小”或“無影響”,其理由是__________。
(2)在二個體積均為1.0L的恒容密閉容器中發生上述二甲醚合成反應④。實驗數據見下表:
容器編號 | 溫度(℃) | 起始物質的量(mol) | 平衡物質的量(mol) | |||
CH3OH(g) | CH3OCH3(g) | H2O(g) | CH3OCH3(g) | H2O(g) | ||
a | 387 | 0.20 | 0 | 0 | 0.080 | 0.080 |
b | 387 | 0.40 | 0 | 0 | ||
c | 207 | 0.20 | 0 | 0 | 0.090 | 0.090 |
①387℃時,反應④的化學平衡常數K=__________。
②達到平衡時,容器b中CH3OH的轉化率為________。
③達到平衡時,容器c中CH3OCH3的體積分數為________。
(3)由H2和CO可直接制備二甲醚:2CO2(g)+4H2(g)=CH3OCH(g)+H2O(g) ΔH=__________;為提高反應物的轉化率,根據化學反應原理,理論上應采取的措施是________(填序號)。
A.高溫高壓 B.低溫低壓 C.高溫低壓 D.低溫高壓
(4)有研究者用Cu-Zn-Al和Al2O3作催化劑,壓強為5.0 MPa的條件下,由合成氣[![]() =2]直接制備二甲醚,結果如下圖所示.已知:選擇性=
=2]直接制備二甲醚,結果如下圖所示.已知:選擇性=![]() ×100%。則有圖可知二甲醚的選擇性達最大值時對應的溫度是____________。
×100%。則有圖可知二甲醚的選擇性達最大值時對應的溫度是____________。

(5)2016年,我國的兩個科研團隊在合成氣直接制備低碳烯烴(nCO+2nH2![]() CnH2n+nH2O)的研究中連續取得重大突破,論文分別發表在《德國應用化學》(2016.03.16)、《Nature》(2016.10.06)雜志上。
CnH2n+nH2O)的研究中連續取得重大突破,論文分別發表在《德國應用化學》(2016.03.16)、《Nature》(2016.10.06)雜志上。![]() =2時,前者在400℃,1MPa的條件下,CO轉化率為11%,低碳烯烴選擇性達74%;后者在250℃,0.1~0.5MPa的條件下,CO轉化率為31.8%,低碳烯烴選擇性為60.8%,則其中低碳烯烴的產率較大者的值為_________。
=2時,前者在400℃,1MPa的條件下,CO轉化率為11%,低碳烯烴選擇性達74%;后者在250℃,0.1~0.5MPa的條件下,CO轉化率為31.8%,低碳烯烴選擇性為60.8%,則其中低碳烯烴的產率較大者的值為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CuCl2廣泛應用于工業生產,溶于水形成綠色溶液。CuCl晶體呈白色,露置于潮濕空氣中易被氧化,實驗室用圖所示的實驗儀器及藥品來制備純凈、干燥的氯氣并與粗銅(含雜質鐵)反應制備氯化銅(鐵架臺、鐵夾及酒精燈省略)。
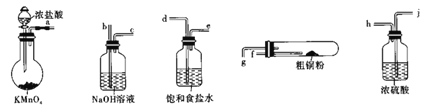
(1)完成上述實驗,氣流方向連接各儀器接口的順序是________a→______、____→______、_____→______、 _________→________;反應時,盛粗銅粉的試管中現象是_______________。
(2)實驗完畢,取試管中的固體有鹽酸溶解后,欲提純氯化銅,請簡述實驗方案:_________________。(室溫,Fe(OH))3 沉淀完全的pH為3.2)
(3)向制得的氯化銅溶液中通入SO2,加熱一段時間既可制得CuCl,寫出該反應的離子方式:_______。
(4)已知:ⅰ.CuCl的鹽酸溶液能吸收CO形成Cu(CO)Cl·H2O
ⅱ.保險粉(Na2S2O4)和KOH的混合溶液能吸收氧氣。
某同學利用如圖所示裝置,測定某混合氣體中H2、CO、SO2和O2的百分組成
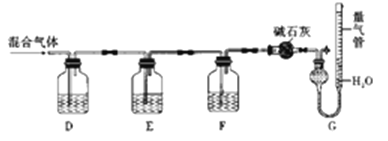
①D瓶測定__________;F洗氣瓶中盛放的試劑是__________________。
②E瓶中發生反應的離子方程式為____________________。
③為了準確讀取G中量氣管的數據,讀數時除了視線與凹液面最低處相平以外,還要注意__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列鑒別方法不可行的是( )
A.用水鑒別乙醇、甲苯和溴苯
B.用燃燒法鑒別乙醇、苯和四氯化碳
C.用碳酸鈉溶液鑒別乙醇、乙酸和乙酸乙酯
D.用酸性高錳酸鉀溶液鑒別苯、環已烯和環已烷
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com