
【題目】將4.74gK2SO4·Al2(SO4)3·nH2O的樣品溶于水,配制成250ml溶液,取出20ml溶液,與濃度為0.064mol/L的氯化鋇溶液25ml恰好完全反應生成沉淀.則K+的物質的量濃度為多少? n值為多少?
__________________、____________________
【答案】 C(K+)=0.04mol/L n=24
【解析】25ml 0.064mol/L的氯化鋇溶液中含有n(Ba2+)= 0.064mol/L×0.025L=0.0016mol,則反應的n(SO42-)=0.0016mol,因此4.74gK2SO4·Al2(SO4)3·nH2O的樣品中n(SO42-)=0.0016mol×![]() =0.02mol,因此K2SO4·Al2(SO4)3·nH2O的物質的量為0.005mol,M[K2SO4·Al2(SO4)3·nH2O]=
=0.02mol,因此K2SO4·Al2(SO4)3·nH2O的物質的量為0.005mol,M[K2SO4·Al2(SO4)3·nH2O]= ![]() =948g/mol,因此n=
=948g/mol,因此n=![]() =24,
=24,
c(K+)=![]() =0.04 mol/L,故答案為:c(K+)=0.04 mol/L;n=24。
=0.04 mol/L,故答案為:c(K+)=0.04 mol/L;n=24。


科目:高中化學 來源: 題型:
【題目】世界上絕大部分鹵素都存在于海洋。海水呈微堿性,海水曬鹽可以得到粗鹽和鹵水,對粗鹽和鹵水進一步加工可以得到氯氣、溴以及其他一些重要的化工產品。
完成下列填空:
(1)工業上用電解飽和食鹽水的方法獲取氯氣。寫出陰極的電極反應式_______________,該反應為________(選填“氧化”、“還原”)反應。若轉移5mol電子,生成氯氣______L(標準狀況下)。
(2)工業上從鹵水獲取溴,涉及到“氧化”、“提取”等步驟。“氧化”時先在鹵水中加入硫酸酸化,然后再通入氯氣,硫酸酸化可以提高氯氣的利用率,原因是________________。在“提取”過程中,用空氣把溴吹出,然后用碳酸鈉溶液吸收,這時溴轉化為Br-和BrO3-,同時有CO2生成,寫出反應的化學方程式________________________________。
(3)用上述方法制得的液溴常溶有少量氯氣,除去氯氣的方法是_____________。
(4)足量氯氣與鐵反應生成氯化鐵,足量碘與鐵反應生成碘化亞鐵。運用原子結構和元素周期律簡要說明導致產物中鐵元素價態不同的原因__________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】石蠟油(17個碳原子以上的液態烷烴混合物)的分解實驗裝置如圖所示(部分儀器已省略)。在試管①中加入石蠟油和氧化鋁(催化石蠟分解);試管②放在冷水中,試管③中加入溴水。

實驗現象:
試管①中加熱一段時間后,可以看到試管內液體沸騰;
試管②中有少量液體凝結,聞到汽油的氣味,往液體中滴加幾滴高錳酸鉀酸性溶液顏色褪去。根據實驗現象回答下列問題:
(1) 裝置A的作用是______________________________;
(2) 試管①中發生的主要反應有:
C17H36![]() C8H18+C9H18C8H18
C8H18+C9H18C8H18![]() C4H10+C4H8
C4H10+C4H8
丁烷可進一步裂解,除得到甲烷和乙烷外,還可以得到另兩種有機物,它們的結構簡式為_________和________,這兩種有機物混合后在一定條件下可聚合成高分子化合物,其反應類型屬于______反應。其可能結構為______(填序號)

(3)寫出試管③中反應的一個化學方程式_____________________________,該反應的類型為__________反應。
(4)試管②中的少量液體的組成是____________(填序號)
A.甲烷B.乙烯C.液態烷烴D.液態烯烴
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I.下表是A、B兩種有機物的有關信息:
A | B |
①分子填充模型為: ②能使溴的四氯化碳溶液褪色; ③其產量是衡量石油化工水平的標志。 | ①由C、H、O三種元素組成,是廚房中的常見調味劑; ②水溶液能使紫色石蕊試液變紅。 |
根據表中信息回答下列問題:
(1)關于A的下列說法中,不正確的是__________(填標號)。
a.分子里含有碳碳雙鍵 b.分子里所有的原子共平面 c.結構簡式為CH2CH2
(2)A與氫氣發生加成反應后生成物質C,與C在分子組成和結構上相似的有機物有一大類,它們的通式為CnH2n+2。當n=__________時,這類有機物開始出現同分異構體。
(3)B與乙醇反應的化學方程式為 ____________________,反應類型為____________________。
(4)以A為原料可直接生產一種高分子化合物,該高分子化合物的結構簡式為__________。
II.糖類、油脂和蛋白質是人體需要的重要營養素。
(5)下列說法正確的是__________(填標號)。
a.糖類、油脂、蛋白質都是僅由C、H、O三種元素組成的
b.糖類、油脂、蛋白質都是高分子化合物
c.油脂有油和脂肪之分,都屬于酯
(6)淀粉和纖維素的化學式都是(C6H10O5)n,它們__________(選“是,,或“不是”)同分異構體,淀粉水解的最終產物是__________(寫名稱)。
(7)重金屬鹽能使人體中毒,這是由于它使人體內的蛋白質發生了__________(選“鹽析”或“變性”)作用。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】熔觸的金屬錫在300℃左右能直接與氯氣作用生成四氯化錫。四氯化錫的熔點-33℃,沸點114℃,遇潮濕空氣水解。某學習小組用以下裝置制取少量四氯化錫。回答下列問題:
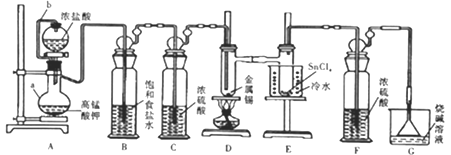
(1)儀器組裝完畢,為檢查裝置的氣密性,將裝置G中漏斗改為導管且管口浸沒于水中,后續操作是__________,說明氣密性良好。
(2)儀器a的名稱是__________;設計連接管b的目的是_______________。
(3)裝置B、F的作用分別是______________、____________。
(4)裝置A中反應的離子方程式為______________,排盡裝置中的空氣后才能點燃D處的酒精燈,判斷裝置中的空氣已排盡的現象是_____________;D中加熱的作用之一是加快氯氣與金屬錫反應,另一作用是__________。
(5)四氯化錫遇潮濕空氣時有白色煙霧產生,同時生成白色固體(SnO2·xH2O),該反應的化學方程式為_____________。
(6)實驗結束后,若制得SnCl4的質量為2.61g,Cl2的轉化率為80%,則消耗KmnO4的質量為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】圖表法、圖像法是常用的科學研究方法。
下表列出原子序數依次增大的短周期元素中四種元素性質的一些數據:
性質 元素 | A | B | C | D |
原子半徑(10-10 m) | 0.37 | 0.77 | 0.74 | 0.99 |
最高價態 | +1 | +4 | - | +7 |
最低價態 | -1 | -4 | -2 | -1 |
用所給元素試回答下列問題:
(1)比元素A原子序數大28的元素,其基態原子的核外電子排布式為___________。
(2)元素A、B、C可形成一種相對分子質量為60的一元羧酸分子,則一個該分子中共含有________個σ鍵,________個π鍵。
(3)如圖是研究部分元素的氫化物的沸點變化規律的圖像,折線c可以表達出第________族元素氫化物的沸點的變化規律。(2分)
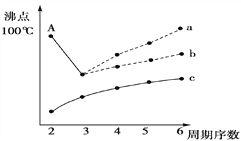
不同同學對某主族元素的氫化物的沸點的變化趨勢畫出了兩條折線——折線a和折線b,你認為正確的是________,理由是__________________________________(2分)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在25℃時,將氣體X、Y放入密閉容器中發生反應生成Z,5min后達到平衡。其初始濃度和平衡濃度如下表:下列說法錯誤的是
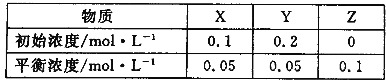
A.該反應可表示為 X+3Y![]() 2Z
2Z
B.反應達到平衡時,X的轉化率為50%
C.前5min 以Y表示的平均反應速率為υ(Y)= 0.01 mol·L-1·min-1
D.增大壓強使平衡向生成Z的方向移動
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,將某一元酸HX和NaOH溶液等體積混合,兩種溶液的濃度和混合后所得溶液的pH如下表:
試驗編號 | HX的物質的量濃度(mol/L) | NaOH的物質的量濃度(mol/L) | 混合溶液的PH |
甲 | 0.2 | 0.2 | PH=a |
乙 | c1 | 0.2 | PH=7 |
丙 | 0.2 | 0.2 | PH>7 |
丁 | c2 | c3 | PH=10 |
請回答:
(1)不考慮其他組的實驗結果,單從甲組情況分析,若a________7(填“>”“<”或“=”),則HX為強酸;若a________7(填“>”“<”或“=”),則HX為弱酸.
(2)在乙組混合溶液中離子濃度c(X-)與c(Na+)的大小關系是________.
A.前者大 B.后者大 C.二者相等 D.無法判斷
(3)丙溶液中離子濃度由大到小的順序是_____________________________.
(4)丁組實驗所得混合溶液中由水電離出的c(OH-)=________mol/L.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com