
將a mol Na2O2與b mol NaHCO3固體混合物在密閉容器中加熱至250℃,讓其充分反應(設Na2O2先與NaHCO3分解出的CO2反應,將CO2消耗后,才與H2O反應).
(1)當a與b按不同比值進行反應時,分析剩余固體和排出氣體的成分,完成下表中空白處:
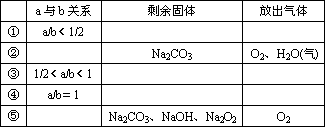
(2)當氣體為H2O(氣)和O2且兩者物質的量相同時,求原混合物中Na2O2與NaHCO3的物質的量之比是多少?
科目:高中化學 來源:河南省新鄉市2009-2010學年高一上學期期末考試化學試卷 題型:013
|
將15 mL 2 mol·L-1 Na2 CO3溶液逐滴加入到40 mL,0.5 mol·L-1 MCln鹽溶液中,恰好將溶液中的Mn+離子完全沉淀為碳酸鹽,則MCln中n值是 | |
| [ ] | |
A. |
4 |
B. |
3 |
C. |
2 |
D. |
1 |
查看答案和解析>>
科目:高中化學 來源:內蒙古赤峰市平煤高中2011屆高三第一次學情測試化學試題 題型:058
硫化鈉和碳酸鈉為原料、采用下述裝置制備硫代硫酸鈉,制備反應可表示為:
2Na2S+Na2CO3+4SO2![]() 3Na2S2O3+CO2
3Na2S2O3+CO2

(1)實驗時,打開K1,關閉K2,最后洗氣瓶中發生反應的離子方程式是________.
(2)錐形瓶內溶液pH小于7時會導致產品分解,因此實驗過程中需要控制錐形瓶內溶液的pH.
①反應過程中,錐形瓶中溶液pH將________(填“增大”、“減小”或“保持不變”).
②測量錐形瓶中溶液pH時,用注射器吸取溶液樣品比直接打開錐形瓶中瓶塞取樣,除操作簡便外,還具有的優點是________________.
③若實驗過程中測得溶液pH已接近于7.此時應該進行的操作是_____________.
(3)已知:2Na2 S2O3+I2=2NaI+Na2 S4O6.實驗結束后進行相關處理,可即獲得Na2 S2O3 5H2O晶體.為測量其純度,取晶體樣品m g,加水溶解后,滴入幾滴淀粉溶液,用0.010 mol/L碘水滴定到終點時,消耗碘水溶液v mL,則該樣品純度是________.
(4)制取硫代硫酸鈉的另一種方法是直接將硫粉和亞硫酸鈉、水混合共熱制取.為探究制取硫代硫酸鈉最佳條件(溶液pH、亞硫酸鈉濃度、反應溫度、硫粉質量),設計如下對比實驗(每次實驗時亞硫酸鈉質量均為63 g,反應時間為30 min):

①實驗1、2的目的是探究亞硫酸鈉濃度對亞硫酸鈉轉化率的影響,則a=________
②若還要探究溶液pH、反應溫度、硫粉質量對亞硫酸鈉轉化率的影響,除實驗1、2外,至少還需進行________次對比實驗
③實驗表明:亞硫酸鈉轉化率不受硫粉質量多少的影響.為什么?
答:________________.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com