
【題目】25 ℃時,已知下列三種金屬硫化物的溶度積常數(Ksp)分別為Ksp(FeS)=6.3×10-18;Ksp(CuS)=1.3×10-36;Ksp(ZnS)=1.6×10-24。下列關于常溫時的有關敘述正確的是( )
A. 硫化鋅、硫化銅、硫化亞鐵的溶解度依次增大
B. 將足量的ZnSO4晶體加入到0.1 mol·L-1的Na2S溶液中,Zn2+的濃度最大只能達到1.6×10-23mol·L-1
C. 除去工業廢水中含有的Cu2+,可采用FeS固體作為沉淀劑
D. 向飽和FeS溶液中加入FeSO4溶液后,混合液中c(Fe2+)變大、c(S2-)變小,Ksp(FeS)變大
【答案】C
【解析】
A、因為Ksp(CuS)=1.3×10-36< Ksp(ZnS)=1.6×10-24< Ksp(FeS)=6.3×10-18,所以溶解度CuS <ZnS<FeS,故A錯誤;
B、原硫化鈉溶液中硫離子增大濃度為:c(S2-)=0.1 mol·L-1,所以鋅離子最小濃度為:c(Zn2+)=![]() mol/L=1.6
mol/L=1.6![]() 10-23mol/L,故B錯誤;
10-23mol/L,故B錯誤;
C、因為Ksp(CuS)=1.3×10-36< Ksp(FeS)=6.3×10-18,硫化銅的溶解度小于硫化亞鐵的,所以除去工業廢水中含有的Cu2+,可采用FeS 固體作為沉淀劑,所以C選項是正確的;
D、向飽和的FeS 溶液中加入FeSO4溶液后,混合液中c(Fe2+)變大、c(S2-)變小,溫度不變,所以Ksp(FeS)不變,故D錯誤。
故答案選C。


科目:高中化學 來源: 題型:
【題目】在“測定1mol氣體體積”的實驗中,我們通常選擇的測量氣體是氫氣,反應是鎂和稀硫酸反應。圖中的A、B、C三部分能組成氣體摩爾體積測定裝置:

(1)C裝置的名稱是___________________。
(2)A、B、C裝置接口的連續順序是_________________。
(3)該裝置正確連接后怎樣做氣密性檢查?_________________。
(4)本實驗中有兩次針筒抽氣,需要記錄的是第____次抽出氣體的體積。
(5)下表是某同學記錄的實驗數據:溫度:25℃,氣壓:101.3kPa
實驗次數 | 鎂帶質量(g) | 硫酸體積(mL) | C瓶讀數(mL) | 抽出氣體的體積(mL) |
1 | 0.115 | 10.0 | 124.8 | 7.0 |
2 | 0.110 | 10.0 | 120.7 | 6.2 |
計算兩次實驗1mol氫氣的體積的平均值=____L(保留一位小數,鎂的相對原子質量為24.3)。
(6)已知實驗溫度下,1mol氫氣的體積的理論值為24.5L,實驗誤差=____%(保留三位有效數字)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列編號代表元素周期表中的一部分元素,用化學式或元素符號回答下列問題:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
一 | ||||||||
二 | ⑥ | ⑩ | ||||||
三 | ① | ③ | ⑤ | ⑦ | ⑨ | |||
四 | ② | ④ | ⑧ |
(1)①、③、⑤的最高價氧化物的水化物堿性最強的是_______(填化學式,下同)。
(2)②、③、④形成的簡單陽離子半徑由大到小的順序是______________。
(3)①和⑧的最高價氧化物對應的水化物化學式為________和________。①和⑧兩元素形成的化合物的化學式為________,該化合物的溶液與元素⑦的單質反應的離子方程式為_______________________。
(4)⑦、⑧、⑩三種元素形成的氣態氫化物最穩定的是________(填化學式,下同),三種元素非金屬性由強到弱的順序為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用熔融堿焙燒工藝可從鋁熱法生產金屬鉻的鉻渣(Al、Al2O3、Cr2O3等)中浸出鉻和鋁,為實現鉻和鋁的再生利用。其工作流程如下:
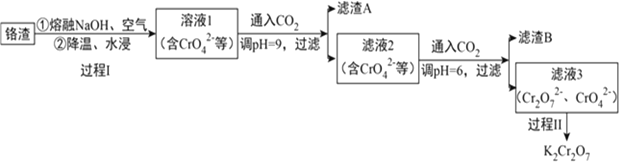
(1)鋁熱法冶煉金屬鉻,是利用了金屬鋁的__________(填“氧化性”或“還原性”)。
(2)溶液1中的陰離子有CrO42-、______、_______。
(3)過程I,在Cr2O3參與的反應中,若生成0.4molCrO42-,消耗氧化劑的物質的量是_______。
(4)通入CO2調節溶液pH實現物質的分離。
①濾渣A煅燒得到Al2O3,再用電解法冶煉Al。冶煉Al的化學方程式是____________________。
②濾渣B受熱分解所得物質可以循環利用,B是__________。
③已知:2CrO42-+2H+ ![]() Cr2O72-+H2O K=4.0×1014濾液3中Cr2O72-的濃度是0.04mol/L,則CrO42-的濃度是__________mol/L。
Cr2O72-+H2O K=4.0×1014濾液3中Cr2O72-的濃度是0.04mol/L,則CrO42-的濃度是__________mol/L。
(5)過程II的目的是得到K2Cr2O7粗品。下表是不同溫度下化合物的溶解度(g/100gH2O)
化合物名稱 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ |
NaCl | 35.7 | 36.0 | 36.6 | 373 | 38.4 |
KCl | 28.0 | 34.2 | 40.1 | 45.8 | 51.3 |
K2Cr2O7 | 4.7 | 12.3 | 26.3 | 45.6 | 73.0 |
Na2Cr2O7 | 163 | 183 | 215 | 269 | 376 |
結合表中數據分析,過程II的操作是:向濾液③中加入稀鹽酸和KCl固體后,_____________,過濾,得到K2Cr2O7粗品。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】無水四氯化錫(SnCl4)是一種用途廣泛的錫化工中間體,實驗室可用熔融的錫(熔點231℃)與Cl2反應制備SnCl4,裝置如圖所示,請回答下列問題:
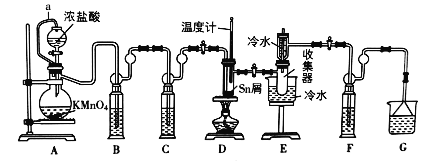
已知,SnCl4在潮濕的空氣中極易水解生成SnO2xH2O。
物質 | 顏色、狀態 | 熔點/℃ | 沸點/℃ |
SnCl2 | 無色晶體 | 246 | 652 |
SnCl4 | 無色液體 | -33 | 114 |
(1)導管a的作用是______,裝置A中發生反應的化學方程式為______。
(2)裝置B、C、F、G中盛放的最佳試劑依次為______(填序號,試劑可重復使用),
①飽和Na2CO3溶液②NaOH溶液③濃H2SO4④飽和NaCl溶液⑤H2O
(3)點燃酒精燈前需要進行的一步操作是______。
(4)若撤去裝置C,則D中發生的主要副反應化學方程式為______。
(5)得到的產物中常含有SnCl2,某實驗小組用碘氧化法滴定分析產品中SnCl4的含量(Sn2++I2=Sn4++2I-)。準確稱取該樣品mg放入錐形瓶中,用少量濃鹽酸溶解,再加水稀釋,淀粉溶液作指示劑,用0.1molL-1碘標準溶液滴定至終點時錐形瓶內溶液顏色變化是______,若消耗標準液20.00mL,則產品中SnCl4的質量含量為______(用含m的代數式表示)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用純凈的CaCO3與100 mL稀鹽酸反應制取CO2,實驗過程記錄如圖所示(CO2的體積已折算為標準狀況下的體積)。下列分析正確的是( )
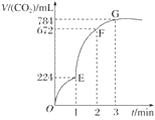
A. OE段表示的平均速率最快
B. EF段,用鹽酸表示該反應的平均反應速率為0.04 mol·L-1·min-1
C. OE、EF、FG三段中,該反應用二氧化碳表示的平均反應速率之比為2∶6∶7
D. G點表示收集的CO2的量最多
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業生產苯乙烯是利用乙苯的脫氫反應如下,針對上述反應,在其它條件不變時,下列說法正確的是( )

A. 加入適當催化劑,可以提高苯乙烯的產量
B. 在保持體積一定的條件下,充入較多的乙苯,可以提高乙苯的轉化率
C. 僅從平衡移動的角度分析,工業生產苯乙烯選擇恒壓條件優于恒容條件
D. 加入乙苯至反應達到平衡過程中,混合氣體的平均相對分子質量不斷增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CuCl廣泛應用于化工和印染等行業。某研究小組用粗銅(含雜質Fe) 為原料制備CuCl2·2H2O晶體,再用CuCl2·2H2O晶體制備CuCl。
(1)制備CuCl2·2H2O晶體:
① B裝置中發生反應的化學方程式是_________________
② 裝置C中粗銅粉末(含雜質Fe)與氣體充分反應時的生成物是______________
③ 反應完成后,將C中的固體用稀鹽酸完全溶解,再調節pH值除雜,經一系列操作便可獲得CuCl2·2H2O晶體。溶解C中生成物固體時,有時會加入少量雙氧水,目的是__________
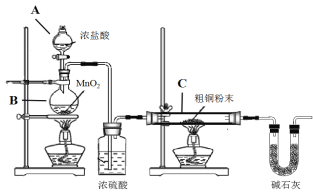
(2)制取CuCl,為了制取CuCl采用如圖所示裝置進行實驗(夾持儀器略):

已知:![]()
④儀器X的名稱是__________
⑤實驗操作的先后順序是a→__________________________→e(填操作的編號)。
a.檢查裝置的氣密性后加入藥品 b.熄滅酒精燈,冷卻
c.在“氣體入口”處通入干燥HCl d.點燃酒精燈,加熱
e.停止通入HCl,然后通入N2
⑥裝置F中NaOH溶液的作用是___________________。
⑦ 反應結束后,取出CuCl產品進行實驗,發現其中含有少量的CuCl2或CuO雜質。請分析產生CuCl2雜質的原因是__________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】酸堿質子理論認為:凡能給出質子的分子或離子都是酸,凡能結合質子的分子或離子都是堿。按照這個理論,下列屬于兩性物質的微粒是( )
①H2O ②CN- ③HS- ④CH3COOH ⑤H2PO![]() ⑥OH-
⑥OH-
A.①②⑤B.③④⑥C.①③⑤D.②④
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com