
| A. | ②③⑦⑧⑨⑩ | B. | ①②③⑤⑧⑨ | C. | ②⑤⑥⑦⑧ | D. | ②④⑦⑧⑩ |
分析 ①根據Cl2參加反應后的價態來分析;
②Na2O和Na2O2均由2個陽離子和1個陰離子構成;
③NO2氣體中存在平衡:2NO2?N2O4;
④Al3+是弱堿陽離子,在溶液中會水解;
⑤一個氫氧化鐵膠粒是多個氫氧化鐵的聚集體;
⑥求出6.0g SiO2晶體的物質的量,然后根據1mol二氧化硅中4molSi-O鍵來分析;
⑦CH5+為10電子微粒;
⑧2.8g N2和2.8g CO的物質的量均為0.1mol,且兩者中均含14個電子;
⑨蔗糖溶液中除了蔗糖分子,還含水分子;
⑩標準狀況下,乙醇為液態.
解答 解:①由于Cl2參加反應后的價態不能確定,故1mol氯氣反應后轉移的電子數無法確定,故錯誤;
②Na2O和Na2O2均由2個陽離子和1個陰離子構成,故1mol混合物中含3mol離子即3NA個,故正確;
③標準狀況下,44.8L NO與22.4LO2混合后生成2molNO2,但NO2氣體中存在平衡:2NO2?N2O4,故混合后氣體中分子總數小于2NA,故錯誤;
④Al3+是弱堿陽離子,在溶液中會水解,故溶液中的鋁離子的個數小于2NA個,故錯誤;
⑤一個氫氧化鐵膠粒是多個氫氧化鐵的聚集體,故所得的氫氧化鐵膠粒的個數小于2NA個,故正確;
⑥求出6.0g SiO2晶體的物質的量,而1mol二氧化硅中4molSi-O鍵,故0.1mol二氧化硅中含0.4mol硅氧鍵即0.4NA個,故正確;
⑦CH5+為10電子微粒,故1mol中含10mol電子即10NA個,故正確;
⑧2.8g N2和2.8g CO的物質的量均為0.1mol,且兩者中均含14個電子,故0.1mol兩者中均含1.4mol電子即1.4NA個,故正確;
⑨蔗糖溶液中除了蔗糖分子,還含水分子,故溶液中的分子個數大于0.6NA個,故錯誤;
⑩標準狀況下,乙醇為液態,故不能根據氣體摩爾體積來計算其物質的量和分子個數,故錯誤.
故選C.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:解答題
 ⑥CH2=CHCH3和CH2=CH2;
⑥CH2=CHCH3和CH2=CH2;查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
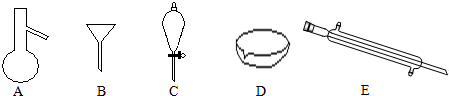
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Al2(SO4)3與NaOH | B. | NaHSO4與Ba(OH)2 | C. | Na2CO3與HCl | D. | NaAlO2與H2SO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬鈉與水反應:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 用氫氧化鋇溶液中和硫酸溶液:Ba2++OH-+H++SO42-═H2O+BaSO4↓ | |
| C. | 氯化鋁溶液中加入過量的氨水 Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 在澄清石灰水中通入過量的CO2:OH-+CO2═HCO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 原混合溶液中只存在Na+、Fe3+、SO42-,不可能存在K+、CO32- | |
| B. | 由實驗(1)無法推斷原混合溶液中是否含有SO42- | |
| C. | 由實驗(2)無法推斷原混合溶液中是否含有Fe3+ | |
| D. | 由實驗(3)可推斷原混合溶液中存在Fe2+ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com