
【題目】消除氮氧化物、二氧化硫等物質造成的污染是目前研究的重要課題。
(1)工業上常用活性炭還原一氧化氮,其反應為:2NO(g)+C(s) ![]() N2(g)+CO2(g)。向容積均為1 L的甲、乙、丙三個恒容恒溫容器中分別加入足量的活性炭和一定量的NO,測得各容器中n(NO)隨反應時間t的變化情況如下表所示:
N2(g)+CO2(g)。向容積均為1 L的甲、乙、丙三個恒容恒溫容器中分別加入足量的活性炭和一定量的NO,測得各容器中n(NO)隨反應時間t的變化情況如下表所示:
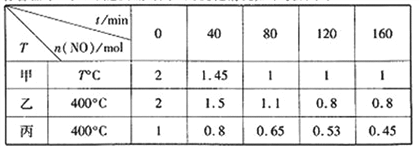
甲容器反應溫度T℃______400℃(填“>”“<”或“=”);乙容器中,0~40min內平均反應速率v(CO2)=_____;丙容器中達平衡后NO的物質的量為_________mol。
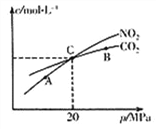
(2)活性炭還原NO2的反應為:2NO2(g)+2C(s) ![]() N2(g)+2CO2(g),在恒溫條件下,1 mol NO2和足量活性炭發生該反應,測得平衡時NO2和CO2的物質的量濃度與平衡總壓的關系如右上圖所示:
N2(g)+2CO2(g),在恒溫條件下,1 mol NO2和足量活性炭發生該反應,測得平衡時NO2和CO2的物質的量濃度與平衡總壓的關系如右上圖所示:
①A、B、C三點中NO2的轉化率最高的是_________點(填“A”或“B”或“C”)。
②計算C點時該反應的壓強平衡常數KP=_______MPa
 (Kp是用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數)。
(Kp是用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數)。
(3)燃煤煙氣脫硫常用如下方法。
方法①:用生物質熱解氣(主要成分CO、CH4、H2)將SO2在高溫下還原成單質硫。涉及的部分反應如下:
2CO(g)+SO2(g)=S(g)+2CO2(g) △H1=8.0 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H3=-483.6 1kJ·mol-1
則H2(g)還原SO2(g)生成S(g)和H2O(g)的熱化學方程式為_______________________。
方法②:用氨水將SO2轉化為NH4HSO3,再氧化成(NH4)2SO4。
實驗測得NH4HSO3溶液中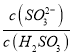 =15,則溶液的pH為________;向該溶液中加氨水使溶液呈中性時,
=15,則溶液的pH為________;向該溶液中加氨水使溶液呈中性時, 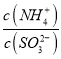 =________。(已知:H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7)
=________。(已知:H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7)
【答案】 > 6.25×10-3mol/(L·min) 0.4 A 4 2H2(g)+SO2(g)=S(g)+2H2O(g) △H=90.4kJ/mol 5 3
【解析】(1)甲達到平衡要80min,比乙達到平衡所需時間短,故T℃>400℃;乙容器中,0~40min內平均反應速率v(CO2)=v(NO)/2=![]() ;先根據乙求出400℃時的平衡常數
;先根據乙求出400℃時的平衡常數
2NO(g)+C(s) ![]() N2(g)+CO2(g)
N2(g)+CO2(g)
n始/mol 2
n變/mol 1.2 0.6 0.6
n平/mol 0.8 0.6 0.6
c平/mol/L 0.8 0.6 0.6
![]()
丙平衡時
2NO(g)+C(s) ![]() N2(g)+CO2(g)
N2(g)+CO2(g)
n始/mol 1
n變/mol 2x x x
n平/mol 1-2x x x
c平/mol/L 1-2x x x
 x=0.3mol,丙容器中達平衡后NO的物質的量為(1-0.3×2)mol=0.4mol;
x=0.3mol,丙容器中達平衡后NO的物質的量為(1-0.3×2)mol=0.4mol;
(2)①由方程式可知隨壓強的增大,平衡逆向移動,故A、B、C三點中NO2的轉化率最高的是A點,A點壓強最低;②C點時
2NO2(g)+2C(s) ![]() N2(g)+2CO2(g),
N2(g)+2CO2(g),
n始/mol 1
n變/mol 2x x 2x
n平/mol 1-2x x 2x
P平/MP 20×2/5 20×1/5 20×2/5
1-2x=2x,x=0.25
該反應的壓強平衡常數KP= MPa;
MPa;
(3)由2CO(g)+SO2(g)=S(g)+2CO2(g) △H1=8.0 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ·mol-1
2H2(g)+O2(g)=2H2O(g) △H3=-483.6 1kJ·mol-1
得 △H3+△H1-△H2=-483.6 1kJ·mol-1+8.0 kJ·mol-1-566.0kJ·mol-1=90.4kJ/mol ,故則H2(g)還原SO2(g)生成S(g)和H2O(g)的熱化學方程式為2H2(g)+SO2(g)=S(g)+2H2O(g) △H=90.4kJ/mol ;Ka1×Ka2=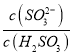 c(H+)2=1.5×10-2×1.0×10-7,c(H+)=10-5mol/L;則溶液的PH=5;NH4HSO3電荷守恒,c(NH4+ )+c(H+)=2c(SO32―)+c(HSO3-)+c(OH-),溶液呈中性,c(H+)=c(OH-),兩邊同除以(SO32―),
c(H+)2=1.5×10-2×1.0×10-7,c(H+)=10-5mol/L;則溶液的PH=5;NH4HSO3電荷守恒,c(NH4+ )+c(H+)=2c(SO32―)+c(HSO3-)+c(OH-),溶液呈中性,c(H+)=c(OH-),兩邊同除以(SO32―),  =2+
=2+ =2+c(H+)/ka2=3。
=2+c(H+)/ka2=3。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】標準狀況下,等質量的SO2與O2相比較,下列結論正確的是( )
A. 分子個數比為1:1 B. 原子個數比為3:4
C. 氧原子個數比為1:2 D. 體積比為2:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸鎂晶體(MgSO4·7H2O)是一種重要的化工原料。以菱鎂礦(主要成分是MgCO3,含少量FeCO3和不溶性雜質)為原料制取硫酸鎂晶體的流程如下:

(1)MgCO3溶于稀硫酸的離子方程式是_________________________。
(2)加入H2O2溶液的目的是____________________(用離子方程式表示)。
(3)已知:部分陽離子以氫氧化物形式沉淀時溶液的pH見下表:
陽離子 | Mg2+ | Fe2+ | Fe3+ |
開始沉淀 | 9.1 | 7.6 | 1.9 |
完全沉淀 | 11.1 | 9.7 | 3.2 |
“沉淀”步驟中,用氨水調節溶液pH的范圍是______________________________。
(4)“過濾”所得濾液中存在大量的陽離子有Mg2+、____________。
(5)“結晶”步驟中需蒸發濃縮濾液,使用的儀器有鐵架臺、酒精燈和_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】方鉛礦(主要成分是PbS,含少量ZnS、Fe、Ag)是提煉鉛及其化合物的重要礦物,其工藝流程如下:

回答下列問題:
(1)流程中“趁熱”過濾的原因是_____________,濾渣的主要成分是_________________。
(2)該工藝流程中可循環利用的物質是__________________。
(3)PbSO4與PbS在加熱條件下發生反應的化學方程式為_____________________。
(4)《藥性論》中有關鉛丹(Pb3O4)的描述是:“治驚悸狂走,嘔逆,消渴。”將PbO高溫焙燒可制得鉛丹,鉛丹中含有的PbO與Al2O3性質相似,可用氫氧化鈉溶液提純鉛丹,提純時發生反應的離子方程是_______________。
(5)以石墨為電極,電解Pb(NO3)2溶液制備PbO2,電解過程中陽極的電極反應式為____________;若電解過程中以鉛蓄電池為電源,當電解裝置中陽極增重23.9g時(忽略副反應),理論上蓄電池負極增重_____g。
(6)取一定量含有Pb2+、Cu2+的工業廢水,向其中滴加Na2S溶液,當PbS開始沉淀時,溶液中 =__________。(已知KSP(PbS)=3.4×10-28,Ksp(CuS)=1.3×10-36)
=__________。(已知KSP(PbS)=3.4×10-28,Ksp(CuS)=1.3×10-36)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銅及其化合物應用廣泛。
Ⅰ.氯化亞銅(CuCl)廣泛用于化工、印染、有機合成等行業。以海綿銅(主要成分是Cu和少量CuO)為原料,采用硝酸銨氧化分解技術生產氯化亞銅的工藝過程如下:

已知:CuCl難溶于醇和水,可溶于氯離子濃度較大的體系,在潮濕空氣中易氧化。
回答下列問題:
(1)步驟①中N元素被還原為最低價,則Cu溶解的離子方程式為________。
(2)步驟③中 (NH4)2SO3要適當過量,目的是使Cu2+充分還原速率和________,其主要反應的離子方程式為_________。已知NH4Cl、Cu2+的物質的量之比[n( NH4Cl )/n(Cu2+)]與Cu2+沉淀率的關系如右圖所示,當氯化銨用量增加到一定程度后Cu2+的沉淀率減少,原因是________。

Ⅱ.以氧缺位鐵酸銅(CuFe2O4-x)作催化劑,可利用太陽能熱化學循環法分解H2O制H2,其物質轉化如圖甲所示。

①氧缺位鐵酸銅(CuFe2O4-x)與水反應的化學方程式為________。
②若x=0.15,則1 mol CuFe2O4參與該循環過程理論上一次能制得標準狀況下的H2體積為________L。(標準狀況下)
③CuFe2O4可用電化學方法得到,其原理如圖乙所示,則陽極的電極反應式為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物G是一種醫藥中間體,常用于制備抗凝血藥。可以通過下圖所示的路線合成:

已知:RCOOH![]() RCOCl;D與FeCl3溶液能發生顯色。
RCOCl;D與FeCl3溶液能發生顯色。
請回答下列問題:
⑴B→C的轉化所加的試劑可能是__________,C+E→F的反應類型是_______。
⑵有關G的下列說法正確的是_________。
A.屬于芳香烴 B.能與FeCl3溶液發生顯色反應
C.可以發生水解、加成、氧化、酯化等反應 D.1mol G最多可以跟4mol H2反應
⑶E的結構簡式為_________。
⑷F與足量NaOH溶液充分反應的化學方程式為__________________________________。
⑸寫出同時滿足下列條件的E的同分異構體的結構簡式_______________。
①發生水解反應②與FeCl3溶液能發生顯色反應③苯環上有兩種不同化學環境的氫原子
⑹已知:酚羥基一般不易直接與羧酸酯化。而苯甲酸苯酚酯(![]() )是一種重要的有機合成中間體。試寫出以苯酚、甲苯為原料制取該化合物的合成路線流程圖(無機原料任用)。注:合成路線的書寫格式參照如下示例流程圖:_________________
)是一種重要的有機合成中間體。試寫出以苯酚、甲苯為原料制取該化合物的合成路線流程圖(無機原料任用)。注:合成路線的書寫格式參照如下示例流程圖:_________________
CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com