
【題目】氟及其化合物用途非常廣泛。回答下列問題:
(1)聚四氟乙烯商品名稱為“特氟龍”,可做不粘鍋涂層。它是一種準晶體,該晶體是一種無平移周期序、但有嚴格準周期位置序的獨特晶體。可通過____方法區分晶體、準晶體和非晶體。
(2)基態銻(Sb)原子價電子排布的軌道式為____。[H2F]+[SbF6]—(氟酸銻)是一種超強酸,存在[H2F]+,該離子的空間構型為______,依次寫出一種與[H2F]+具有相同空間構型和鍵合形式的分子和陰離子分別是_______、_________。
(3)硼酸(H3BO3)和四氟硼酸銨(NH4BF4)都有著重要的化工用途。
①H3BO3和NH4BF4涉及的四種元素中第二周期元素的第一電離能由大到小的順序_____(填元素符號)。
②H3BO3本身不能電離出H+,在水中易結合一個OH﹣生成[B(OH)4]﹣,而體現弱酸性。[B(OH)4]﹣中B原子的雜化類型為_____。
③NH4BF4(四氟硼酸銨)可用作鋁或銅焊接助熔劑、能腐蝕玻璃等。四氟硼酸銨中存在_______(填序號):
A 離子鍵 B σ鍵 C π鍵 D 氫鍵 E 范德華力
(4)SF6被廣泛用作高壓電氣設備絕緣介質。SF6是一種共價化合物,可通過類似于Born-Haber循環能量構建能量圖(見圖a)計算相聯系的鍵能。則S—F的鍵能為_______kJ·mol-1。

(5)CuCl的熔點為426℃,熔化時幾乎不導電;CuF的熔點為908℃,密度為7.1g·cm-3。
①CuF比CuCl熔點高的原因是_____________;
② 已知NA為阿伏加德羅常數。CuF的晶胞結構如上“圖b”。則CuF的晶胞參數a=__________nm (列出計算式)。
【答案】X—射線衍射 ![]() V型 H2O NH2- F>N>O>B sp3 AB 327 由兩者的熔點可知,CuCl是分子晶體,而CuF為離子晶體,CuF離子晶體的晶格能大于CuCl分子間范德華力
V型 H2O NH2- F>N>O>B sp3 AB 327 由兩者的熔點可知,CuCl是分子晶體,而CuF為離子晶體,CuF離子晶體的晶格能大于CuCl分子間范德華力 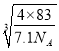 ×107
×107
【解析】
(1)通過X—射線衍射區分晶體、非晶體、準晶體;
(2)根據銻元素原子核外電子排布寫出基態銻(Sb)原子價電子排布的軌道式;用價層電子對互斥理論判斷[H2F]+的空間構型;用替代法書寫與[H2F]+具有相同空間構型和鍵合形式的分子和陰離子;
(3)①同周期主族元素自左而右原子半徑減小,第一電離能呈增大趨勢;
②[B(OH)4]﹣中B的價層電子對=4+1/2(3+1-4×1)=4,所以采取sp3雜化;
③NH4BF4(四氟硼酸銨)中含銨根離子和氟硼酸根離子,二者以離子鍵相結合;銨根離子中含3個σ鍵和1個配位鍵,氟硼酸根離子中含3個σ鍵和1個配位鍵;
(4)鍵能指氣態基態原子形成1mol化學鍵釋放的最大能量。由圖a可知,氣態基態S(g)和6F(g)原子形成SF6(g)釋放的能量為1962kJ,即形成6molS—F鍵釋放的能量為1962kJ,則形成1molS—F鍵釋放的能量為1962kJ÷6=327kJ,則S—F的鍵能為327kJ·mol-1;
(5)①CuCl是分子晶體,而CuF為離子晶體,CuF離子晶體的晶格能大于CuCl分子間范德華力,故CuF比CuCl熔點高;
②均攤法計算晶胞中Cu+、F-離子數,計算晶胞質量,晶胞質量=晶體密度×晶胞體積;
(1)從外觀無法區分三者,區分晶體、非晶體、準晶體最可靠的方法是X—射線衍射法。本小題答案為:X-射線衍射。
(2)銻為51號元素,Sb位于第五周期VA族,則基態銻(Sb)原子價電子排布的軌道式為![]() ;[H2F]+[SbF6]—(氟酸銻)是一種超強酸,存在[H2F]+,[H2F]+中中心原子F的價層電子對數為2+
;[H2F]+[SbF6]—(氟酸銻)是一種超強酸,存在[H2F]+,[H2F]+中中心原子F的價層電子對數為2+![]() =4,σ鍵電子對數為2,該離子的空間構型為V型,與[H2F]+具有相同空間構型和鍵合形式的分子為H2O、陰離子為NH2- 。本小題答案為:
=4,σ鍵電子對數為2,該離子的空間構型為V型,與[H2F]+具有相同空間構型和鍵合形式的分子為H2O、陰離子為NH2- 。本小題答案為:![]() ; V型 ;H2O ; NH2-。
; V型 ;H2O ; NH2-。
(3)①H3BO3和NH4BF4涉及的四種元素中第二周期元素是B、N、O、F四種元素,同周期元素從左向右第一電離能呈增大趨勢,N的2p能級半充滿較穩定,N的第一電離能大于O,則這四種元素第一電離能由大到小的順序為F>N>O>B。本小題答案為:F>N>O>B。
②[B(OH)4]﹣中B的價層電子對=4+1/2(3+1-4×1)=4,所以B采取sp3雜化。本小題答案為:sp3。
③NH4BF4(四氟硼酸銨)中含銨根離子和氟硼酸根離子,銨根離子中含3個σ鍵和1個配位鍵,氟硼酸根離子中含3個σ鍵和1個配位鍵,銨根離子和氟硼酸根離子以離子鍵相結合,則四氟硼酸銨中存在離子鍵、σ鍵、配位鍵。本小題答案為:AB。
(4)鍵能指氣態基態原子形成1mol化學鍵釋放的最大能量。由圖a可知,氣態基態S(g)和6F(g)原子形成SF6(g)釋放的能量為1962kJ,即形成6molS—F鍵釋放的能量為1962kJ,則形成1molS—F鍵釋放的能量為1962kJ÷6=327kJ,則S—F的鍵能為327kJ·mol-1。本小題答案為:327。
(5)①CuCl的熔點為426℃,熔化時幾乎不導電,CuCl是分子晶體,而CuF的熔點為908℃,CuF為離子晶體,CuF離子晶體的晶格能大于CuCl分子間范德華力,故CuF比CuCl熔點高。本小題答案為:由兩者的熔點可知,CuCl是分子晶體,而CuF為離子晶體,CuF離子晶體的晶格能大于CuCl分子間范德華力。
<>②晶胞中Cu+數目為8×1/8+6×1/2=4,F-數目為4,故晶胞質量=(4×64+4×19)g÷NA =(4×83)/NA g,根據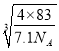 ×107nm。本小題答案為:
×107nm。本小題答案為: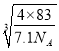 ×107。
×107。 

 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】電化學原理在防止金屬腐蝕、能量轉換等方面應用廣泛。
(1)①鋼鐵在海水中容易發生電化學腐蝕,正極反應式是__________。
②圖中,為減緩鋼閘門的腐蝕,材料B可以選擇__________(填“Zn”或“Cu”)。
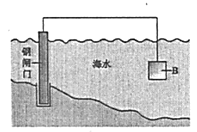
(2)如圖為鋼鐵防護模擬實驗裝置,則鐵做__________極,檢測鋼鐵保護效果的方法是:取少量鐵電極附近的溶液于試管中,_________,則說明保護效果好。

(3)氫氧燃料電池是一種新型的化學電源,其構造如圖所示:

a、b為多孔石墨電極,通入的氣體由孔隙中逸出,并在電極表面放電。
①a的電極反應式是_________;
②若電池共產生3.6g水,則電路中通過了_______mol的電子。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】儲氫材料是一類能可逆地吸收和釋放氫氣的材料。LaNi5合金、NaBH4、H3B-NH3、Mg2NiH4等都是潛在儲氫材料。回答下列問題:
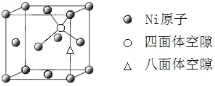
(1)基態Ni原子的核外電子排布式為____,有___________個未成對的電子;
(2)NaBH4中H為-1價,Na、B、H電負性由大到小的順序是_________。BH4-離子的立體構型為________,其中B的雜化軌道類型為_____。
(3)B2H6和NH3化合可以生成H3B-NH3,H3B-NH3加熱時發生反應:H3B-NH3=BN+3H2,緩慢釋放出H2。BN有類似于石墨的結構,B2H6、NH3和BN的沸點由高到低的順序為_________, 原因是___。
(4)X-射線衍射分析表明,Mg2NiH4 的立方晶胞的面心和頂點均被Ni原子占據,所有Mg原子的Ni配位數都相等。則Mg原子填入由Ni原子形成的_____空隙中(填“四面體”或“八面體”),其空隙占有百分率為_____。
(5)已知Mg2NiH4 晶體的晶胞參數為646.5 pm,液氫的密度為0.0708 g·cm-3。若以材料中氫的密度與液態氫密度之比定義儲氫材料的儲氫能力,則Mg2NiH4 的儲氫能力是液氫的___倍(列出計算式即可)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某抗結腸炎藥物的有效成分的合成路線如圖所示(部分試劑和反應條件已略去):
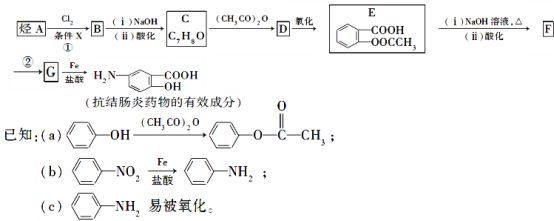
請回答下列問題:
(1)E中含有的官能團為__。
(2)②的反應類型是__。
(3)下列對抗結腸炎藥物的有效成分可能具有的性質推測不正確的是__(填字母)。
a.水溶性比苯酚的好,密度比苯酚的大
b.能發生消去反應
c.能發生加聚反應
d.既有酸性又有堿性
(4)①的反應方程式為__。
(5)符合下列條件的E的同分異構體有__種。寫出其中核磁共振氫譜中有四組峰的結構簡式:__。
a.與E具有相同的官能團且官能團不在同一側鏈上
b.水解產物之一能與氯化鐵溶液發生顯色反應
(6)連有烷基的苯環上再引入一個取代基時,常取代烷基鄰、對位上的氫原子,而連有羧基的苯環上再引入一個取代基時,常取代羧基間位上的氫原子。據此設計出以A為原料合成![]() 的路線(仿照題中抗結腸炎藥物的有效成分的合成路線進行答題)___。
的路線(仿照題中抗結腸炎藥物的有效成分的合成路線進行答題)___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法正確的是( )
A. 烷烴的通式為CnH2n+2,隨n值增大,碳元素的質量百分含量逐漸減小
B. 乙烯與溴加成反應的產物為溴乙烷
C. 1 mol苯恰好與3 mol氫氣完全加成,說明苯分子中有三個碳碳雙鍵
D. 當n=7,主鏈上有5個碳原子的烷烴共有5種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究性學習小組利用電化學方法處理石油煉制過程中產生的含H2S的廢氣。基本工藝是將H2S通入FeCl3溶液中,過濾后將濾液加入電解槽中電解,電解后的濾液可以循環利用。下列有關說法正確的是( )
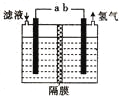
A.過濾得到的沉淀可能是FeS
B.與a極相連的電極反應式為Fe2+- e-= Fe3+
C.可以用Fe與外接電源a極相連
D.若有0.10mol電子轉移,則一定能得到1.12L H2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】美國藥物學家最近合成一種可能用于治療高血壓的有機物K,合成路線如下:
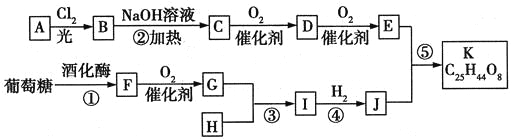
其中A屬于碳氫化合物,其中碳的質量分數約為83.3%;E的核磁共振氫譜中只有2組吸收峰。H常溫下呈氣態,是室內裝潢產生的主要污染物之一。G和H以1:3反應生成I。
試回答下列問題:
(1)A的分子式為:______________。
(2)寫出下列物質的結構簡式:D:____________;G:___________。
(3)反應①―⑤中屬于取代反應的有___________。
(4)反應①的化學方程式為_______________;反應④的化學方程式為_________________。
(5)E有多種同分異構體,符合“既能發生銀鏡反應又能發生水解反應”條件的E的同分異構體有_______種,寫出符合上述條件且核磁共振氫譜只有2組吸收峰的E的同分異構體的結構簡式:________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】丙烯酸酯類物質廣泛用于建筑、包裝材料等,丙烯酸是合成丙烯酸酯的原料之一。丙烯醇可用于生產甘油、塑料等。以丙烯醛為原料生產丙烯醇、丙烯酸的流程如圖所示:

已知:
①2CH2=CH-CHO+NaOH![]() CH2=CHCH2OH+CH2=CHCOONa
CH2=CHCH2OH+CH2=CHCOONa
②2CH2=CHOONa+H2SO4→2CH2=CHCOOH+Na2SO4
③有關物質的相關性質如表:
物質 | 丙烯醛 | 丙烯醇 | 丙烯酸 | 四氯化碳 |
沸點/℃ | 53 | 97 | 141 | 77 |
熔點/℃ | - 87 | - 129 | 13 | -22.8 |
密度/g·mL-3 | 0.84 | 0.85 | 1.02 | 1.58 |
溶解性(常溫) | 易溶于水和有機溶劑 | 溶于水和有機溶劑 | 溶于水和有機溶劑 | 難溶于水 |
(1)操作①需要連續加熱30min,所用裝置如圖所示。儀器L名稱是________。

(2)操作②使用的主要儀器是分液漏斗,在使用之前需進行的操作是 ___。
(3)操作④包括____、過濾、冰水洗滌、低溫吸干。
(4)操作⑤中,加熱蒸餾“下層液體”,分離出四氯化碳;再分離出丙烯醇(如圖),要得到丙烯醇應收集 ____(填溫度)的餾分。圖中有一處明顯錯誤,應改為____。

(5)測定丙烯醇的摩爾質量:準確量取amL丙烯醇于分液漏斗中,燒瓶內盛裝足量鈉粒。實驗前量氣管B中讀數為b mL,當丙烯醇完全反應后,冷卻至室溫、調平B、C液面,量氣管B的讀數為c mL。已知室溫下氣體摩爾體積為VL·mol-1。

調平B、C液面的操作是____;實驗測得丙烯醇的摩爾質量為____g·mol-1(用代數式表示)。如果讀數時C管液面高于B管,測得結果將____(填“偏大”“偏小”或“不變”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是恒溫條件下某化學反應的反應速率隨反應時間變化的示意圖。下列敘述與示意圖不相符合的是( )

A.反應達到平衡時,正反應速率和逆反應速率相等
B.該反應達到平衡狀態Ⅰ后,增大反應物濃度,平衡發生移動,達到平衡狀態Ⅱ
C.該反應達到平衡狀態Ⅰ后,減小反應物濃度,平衡發生移動,達到平衡狀態Ⅱ
D.同一種反應物在平衡狀態Ⅰ和平衡狀態Ⅱ時濃度不相等
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com