
 研究NO2、SO2、CO等大氣污染氣體的處理及利用的方法具有重要意義.
研究NO2、SO2、CO等大氣污染氣體的處理及利用的方法具有重要意義.分析 (1)a.隨反應:NO2(g)+SO2(g)?SO3(g)+NO(g)的進行,氣體的總的物質的量不變,壓強不變.
b.混合氣體顏色保持不變,說明二氧化氮的濃度不變.
c.隨反應進行NO和O2的物質的量之比發生變化.
d.每消耗1mol SO2的同時生成1mol NO都表示正反應速率.
(2)據三段式求出各物質的濃度以及化學平衡常數表達式計算化學平衡常數;
(3)氨氣是堿性氣體,可以和酸反應生成鹽;
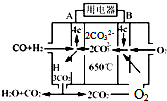
(4)碳酸鹽燃料電池中通氧氣的電極一定為正極,通入燃料的電極一定為負極,氧氣在該電極上發生還原反應;
(5)①根據二氧化碳氣體體積和溶液質量增加的量列方程組解出一氧化氮和二氧化氮的體積,從而得出其體積之比;
②根據過多的NO不能與Na2CO3溶液反應;
解答 解:(1)a.隨反應進行,氣體的物質的量不變,壓強不變,體系壓強保持不變,不能說明到達平衡狀態,故a錯誤;
b.混合氣體顏色保持不變,說明二氧化氮的濃度不變,說明到達平衡狀態,故b正確;
c.隨反應進行NO和O2的物質的量之比發生變化,NO和O2的物質的量之比保持不變,說明到達平衡狀態,故c正確;
d.每消耗1mol SO2的同時生成1mol NO都表示正反應速率,反應自始至終都按此比例進行,故d錯誤.
故選:bc;
(2)NO2(g)+SO2(g)?SO3(g)+NO(g)
起始物質的體積 a 2a 0 0
轉化物質的體積 x x x x
平衡物質的體積 a-x 2a-x x x
平衡時NO2與SO2體積比為1:6,即(1a-x):(2a-x)=1:6,故x=$\frac{4}{5}$a,故平衡常數K=$\frac{C(SO{\;}_{3})C(NO)}{c(NO{\;}_{2})C(SO{\;}_{2})}$=$\frac{x{\;}^{2}}{(a-x)(2a-x)}$=$\frac{\frac{16}{25}a{\;}^{2}}{\frac{1}{5}a×\frac{6}{5}a}$=$\frac{8}{3}$,
故答案為:$\frac{8}{3}$;
(3)氨氣是堿性氣體,可以和磷酸反應生成鹽,產生的鹽隨著酸的磷酸的量的多少而不同,可以產生磷酸銨,磷酸氫銨或是磷酸二氫銨,故答案為:(NH4)3PO4(或(NH4)2HPO4或NH4H2PO4);
(4)碳酸鹽燃料電池中通氧氣的電極一定為正極,通入燃料的電極一定為負極,氧氣在該電極上發生還原反應,故答案為:負;2CO2+O2+4e-=2CO32-;
(5)①設NO的物質的量是x,NO2的物質的量是y,則
x+$\frac{y-x}{2}$=$\frac{22.4}{22.4}$mol;
32x+24(y-x)=44
解得:x=$\frac{1}{4}$,y=$\frac{7}{4}$;即一氧化氮和二氧化氮的物質的量之比$\frac{1}{4}$:$\frac{7}{4}$=1:7,所以相同條件下,一氧化氮和二氧化氮的體積之比是1:7,故答案為:1:7.
②NO不能與Na2CO3溶液反應,所以對于含NO較多混合氣體無法完全吸收,故答案為:含NO較多混合氣體無法完全吸收.
點評 本題主要考查平衡狀態判斷、平衡常數、電極反應以及化學計算,注意平時知識的積累以及靈活應用是解題的關鍵,難度不大.


科目:高中化學 來源: 題型:填空題
 ;CaCl2
;CaCl2 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ba(OH)2溶液 | B. | NaOH溶液 | C. | KNO3溶液 | D. | AgNO3溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在標準狀況下,含4molHCl的濃鹽酸與足量的MnO2反應可生成22.4L氯氣 | |
| B. | 標準狀況下,2.24L H2O中含有H2O分子數為0.1NA | |
| C. | 1L 0.1mol/L NaHSO4溶液中含有的陽離子數目為0.1NA | |
| D. | 實驗室所制得的1.7g NH3中含有的電子數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 已知常溫下AgCl的溶解度遠大于AgBr,現將AgCl和AgBr的兩種飽和溶液等體積混合后,再加入足量濃AgNO3溶液,生成的AgCl沉淀多于AgBr沉淀 | |
| B. | Fe(OH)3溶于氫碘酸的離子方程式為:Fe(OH)3+3H+=Fe3++3H2O | |
| C. | 甲基橙呈黃色的溶液中,I-、Cl-、NO3-、Na+一定可以大量共存 | |
| D. | 已知甲烷的燃燒熱為890.3kJ•mol-1,則表示甲烷燃燒熱的熱化學方程式為: CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na投入足量鹽酸中:2Na+2H2O=2Na++2OH-+H2↑ | |
| B. | Cl2通入水中:Cl2+H2O=2H++Cl-+ClO- | |
| C. | 向Na2CO3溶液中加入少量鹽酸:CO32-+2H+=H2O+CO2↑ | |
| D. | NaHCO3溶液中加入過量澄清石灰水:Ca2++HCO3-+OH-=H2O+CaCO3↓ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com