
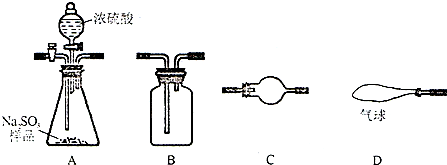
| 實驗裝置(填字母) | D | ||||||
| 裝置中所盛藥品(填序號) | ④ |
| m(Na2SO3) |
| m(總) |
| 實驗裝置(填字母) | C | A | B | C | C | ||
| 裝置中所盛藥品(填序號) | ③ | ① | ③ | ③ |
| 5g |
| 64g/mol |
| 315 |
| 32 |
| ||
| a |
| 315 |
| 32a |
| 315 |
| 32a |


科目:高中化學 來源: 題型:
| A、向Mg(HCO3)2溶液中加入過量的 NaOH溶液:Mg2++2HCO3-+4OH-=Mg(OH)2↓+2CO32-+2H2O |
| B、向亞硫酸鋇固體中加入稀硝酸:3BaSO3+2H++2NO3-=3BaSO4↓+2NO↑+H2O |
| C、在銀氨溶液中滴加過量稀硝酸:[Ag(NH3)2]++2H+=Ag++2NH4+ |
| D、向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-剛好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3?H2O+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:
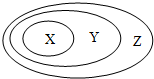 用如圖表示的一些物質或概念間的從屬關系中不正確的是( )
用如圖表示的一些物質或概念間的從屬關系中不正確的是( )| X | Y | Z | |
| A | 甘油 | 化合物 | 純凈物 |
| B | 電解質 | 離子化合物 | 化合物 |
| C | 膠 體 | 分散系 | 混合物 |
| D | 堿性氧化物 | 金屬氧化物 | 氧化物 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
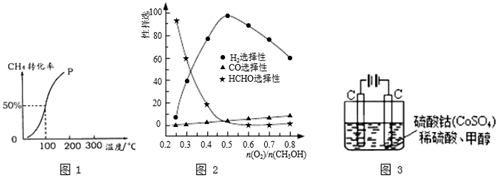
| 1 |
| 2 |
| c(H2) |
| c(CH3OH) |
| n(O2) |
| n(CH3OH) |
查看答案和解析>>
科目:高中化學 來源: 題型:
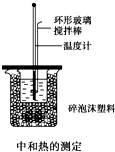 50mL 0.50mol/L鹽酸與50mL 0.55mol/L NaOH溶液在如圖所示的裝置中進行中和反應,通過測定反應過程中所放出的熱量可計算中和熱,回答下列問題:
50mL 0.50mol/L鹽酸與50mL 0.55mol/L NaOH溶液在如圖所示的裝置中進行中和反應,通過測定反應過程中所放出的熱量可計算中和熱,回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
| A、溶液中SO42-的濃度是0.3 mol/L |
| B、溶液中一定含有A13+和NH4+ |
| C、一定不存在Mg2+,可能存在A13+ |
| D、一定存在Cl- 可能含CO32- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com